EL AGONISTA SINTETICO DEL RECEPTOR GAMMA ACTIVADO POR PROLIFERADOR DE PEROXISOMAS, ROSIGLITAZONA, AUMENTA LOS NIVELES PLASMATICOS DE ADIPONECTINA EN PACIENTES CON DIABETES TIPO 2: CONSECUENCIAS CLINICAS
(especial para SIIC © Derechos reservados)
Recepción del artículo: 28 de noviembre, 2003
Aprobación: 0 de , 0000
 Conclusión breve
La rosiglitazona eleva en más de dos veces el nivel promedio de adiponectina en plasma. El tratamiento con rosiglitazona parece ser el único parámetro relacionado en forma independiente con las modificaciones en la adiponectina plasmática.
Conclusión breve
La rosiglitazona eleva en más de dos veces el nivel promedio de adiponectina en plasma. El tratamiento con rosiglitazona parece ser el único parámetro relacionado en forma independiente con las modificaciones en la adiponectina plasmática.
 Resumen
La adiponectina, una citoquina de adipocitos, tiene propiedades antiinflamatorias y antiaterogénicas. La administración de adiponectina a animales se asocia con reducción de la glucosa plasmática y aumento de la sensibilidad a la insulina. En el hombre, la concentración plasmática de adiponectina se ha relacionado con los principales componentes del síndrome metabólico. El receptor γ activado por proliferador de peroxisomas (PPAR)-γ es un factor transcripcional crucial que controla muchos genes de adipocitos. Investigamos si el nivel de adiponectina podía elevarse con el tratamiento con el agonista del PPAR-γ -rosiglitazona- en pacientes con diabetes tipo 2 reclutados para un estudio aleatorizado a doble ciego y controlado con placebo. El nivel promedio de adiponectina aumentó más dos veces (P = 0.0005) en el grupo asignado a rosiglitazona mientras que no se observaron cambios en el grupo placebo. El análisis de regresión lineal de multivariado mostró que el tratamiento con rosiglitazona fue el único parámetro relacionado en forma significativa con las modificaciones en la adiponectina plasmática. La terapia contribuyó con el 24% de la variabilidad en la concentración sérica de adiponectina luego del control de otros factores de confusión. En un estudio genético en una amplia cohorte de familias hipertensas, encontramos que el polimorfismo del gen de adiponectina se asocia con la sensibilidad a la insulina. El efecto de la adiponectina se modifica acorde a los genotipos PPAR-γ2, lo cual indica una interacción genética en la sensibilidad a la insulina. Estas observaciones sugieren que la mayor expresión de adiponectina puede contribuir con los beneficios anti-hiperglucémicos y posiblemente antiaterogénicos de los agonistas del PPAR-&gamma.
Clasificación en siicsalud
Resumen
La adiponectina, una citoquina de adipocitos, tiene propiedades antiinflamatorias y antiaterogénicas. La administración de adiponectina a animales se asocia con reducción de la glucosa plasmática y aumento de la sensibilidad a la insulina. En el hombre, la concentración plasmática de adiponectina se ha relacionado con los principales componentes del síndrome metabólico. El receptor γ activado por proliferador de peroxisomas (PPAR)-γ es un factor transcripcional crucial que controla muchos genes de adipocitos. Investigamos si el nivel de adiponectina podía elevarse con el tratamiento con el agonista del PPAR-γ -rosiglitazona- en pacientes con diabetes tipo 2 reclutados para un estudio aleatorizado a doble ciego y controlado con placebo. El nivel promedio de adiponectina aumentó más dos veces (P = 0.0005) en el grupo asignado a rosiglitazona mientras que no se observaron cambios en el grupo placebo. El análisis de regresión lineal de multivariado mostró que el tratamiento con rosiglitazona fue el único parámetro relacionado en forma significativa con las modificaciones en la adiponectina plasmática. La terapia contribuyó con el 24% de la variabilidad en la concentración sérica de adiponectina luego del control de otros factores de confusión. En un estudio genético en una amplia cohorte de familias hipertensas, encontramos que el polimorfismo del gen de adiponectina se asocia con la sensibilidad a la insulina. El efecto de la adiponectina se modifica acorde a los genotipos PPAR-γ2, lo cual indica una interacción genética en la sensibilidad a la insulina. Estas observaciones sugieren que la mayor expresión de adiponectina puede contribuir con los beneficios anti-hiperglucémicos y posiblemente antiaterogénicos de los agonistas del PPAR-&gamma.
Clasificación en siicsalud
 Artículos originales> Expertos del Mundo>
Artículos originales> Expertos del Mundo>
página www.siicsalud.com/des/expertos.php/20022
Especialidades
 Principal: Endocrinología y Metabolismo,
Principal: Endocrinología y Metabolismo,
 Relacionadas: Bioquímica, Farmacología, Medicina Farmacéutica,
Relacionadas: Bioquímica, Farmacología, Medicina Farmacéutica,
 Enviar correspondencia a:
Enviar correspondencia a:
Lee-Ming Chuang. 7 Chung-Shan South Road, Taipei, Taiwan..
Synthetic Peroxisome Proliferator-Activated Receptor-γ Agonist, Rosiglitazone, Increases Plasma Levels of Adiponectin in Type 2 Diabetic Patients: A Clinical Investigation.
 Abstract
Abstract
Adiponectin, an adipocytokine, exhibits anti-inflammatory and anti-atherogenic properties. Administration of adiponectin to animals reduces plasma glucose and increased insulin sensitivity. In human subjects, plasma levels of adiponectin have been linked with major components of metabolic syndrome. The peroxisome proliferators-activated receptor (PPAR)-γ is a key transcriptional factor that controls many adipocyte genes. We investigated whether the level of adiponectin could be increased by treatment with a PPAR-γ agonist, rosiglitazone, in type 2 diabetes patients recruited for a randomized double-blind placebo-controlled trial. The mean plasma adiponectin level was increased by more than twofold (P<0.0005) in the rosiglitazone group, whereas no change was observed in the placebo group. Multivariate linear regression analysis showed that rosiglitazone treatment was the single variable significantly related to the changes of plasma adiponectin. The treatment contributed to 24% of the variance in changes of plasma adiponectin after adjusting for other factors. In a genetic study based on a large hypertensive family cohort, we found that adiponectin gene polymorphism was associated with insulin sensitivity. The effect of adiponectin was modified by PPARγ2 genotypes, indicating a genetic interaction in insulin sensitivity. These observations suggest that increased adiponectin expression may contribute to the anti-hyperglycemic and putative anti-atherogenic benefits of PPAR-γ agonists.
EL AGONISTA SINTETICO DEL RECEPTOR GAMMA ACTIVADO POR PROLIFERADOR DE PEROXISOMAS, ROSIGLITAZONA, AUMENTA LOS NIVELES PLASMATICOS DE ADIPONECTINA EN PACIENTES CON DIABETES TIPO 2: CONSECUENCIAS CLINICAS
(especial para SIIC © Derechos reservados)
Artículo completo
Propiedades biológicas de la adiponectina
Ahora se sabe que el tejido adiposo participa activamente en la homeostasis de la energía y metabolismo y que no es simplemente un depósito del exceso de energía. Las citoquinas adipocitarias representan un grupo de factores biológicamente activos derivados del tejido adiposo que modulan funciones fisiológicas de otros tejidos (1). La adiponectina es una de estas citoquinas del adipocito que circula en plasma en concentraciones elevadas. Es una glucoproteína con estructura similar a la del colágeno y del C1q del complemento (2, 3). La adiponectina del hombre (también denominada apM1 o GBP-28) y su homólogo murino (adipoQ o ACR30) han sido identificadas (4-5). Los estudios in vitro demostraron que la adiponectina recombinante reduce la adhesión de monocitos inducida por el factor de necrosis tumoral (TNF)-α, la señalización del factor nuclear κB y la expresión de la molécula de adhesión intracelular-1, la molécula de adhesión celular endotelial-1 y la E-selectina en el endotelio (6, 7). Asimismo, reduce la producción del TNF-α en los macrófagos tratados con lipopolisacáridos (8). Se ha visto que la adiponectina también atenúa la acumulación de ésteres de colesterol y la expresión del gen del receptor de depuración clase A en macrófagos derivados de monocitos humanos cultivados (9). Estos hallazgos in vitro sugieren que la adiponectina es una molécula antiinflamatoria y antiaterogénica específica de adipocitos y de tejido adiposo que puede actuar como una conexión biológica entre la obesidad y los trastornos asociados con la obesidad, como arteriosclerosis. En modelos animales y en el hombre sólo se encontró adiponectina en las paredes de los vasos lesionados por catéteres pero no en las paredes de vasos intactos (9,10). En sujetos con obesidad, diabetes tipo 2 o enfermedad coronaria se encontraron niveles plasmáticos bajos de adiponectina (6,11,12). La concentración sanguínea de adiponectina se correlaciona en forma negativa con la glucosa en plasma, insulina, nivel de triglicéridos e índice de masa corporal (IMC) pero en forma positiva con los niveles plasmáticos del colesterol asociado con lipoproteínas de alta densidad (HDLc) (12). También encontramos una correlación similar en individuos con sobrepeso y obesidad (13). Si bien la asociación con la presión arterial aún es controvertida, recientemente encontramos una relación negativa independiente entre la presión arterial sistólica y la adiponectina en plasma (14). Así, los niveles de adiponectina se relacionan con todos los componentes principales del síndrome metabólico. Más aún, la concentración plasmática de adiponectina también se correlaciona en forma positiva con la disponibilidad de glucosa estimulada por insulina evaluada con clampeo euglucémico hiperinsulinémico (15). En forma conjunta, la evidencia sugiere que una concentración baja de adiponectina puede ser un nuevo marcador del síndrome de resistencia a la insulina. Los estudios en animales indican que la adiponectina exógena inhibe un amplio espectro de efectos metabólicos. La inyección de adiponectina en animales reduce la concentración de glucosa y de ácidos grasos libres en plasma, aumenta la β oxidación de ácidos grasos, disminuye la cantidad de triglicéridos en el músculo esquelético, mejora la sensibilidad a la insulina y desciende el peso corporal (16,18). Estos estudios sugieren que la adiponectina puede ser una molécula blanco en el tratamiento de la resistencia a la insulina y de la diabetes tipo 2. Adiponectina y receptor-γ activado por proliferador de peroxisomas
El receptor γ activado por proliferador de peroxisomas (PPAR)-γ es un factor transcripcional que induce diferenciación de adipocitos y controla muchos genes de adipocitos (19). Luego de la activación, los PPAR-γ forman heterodímeros con el receptor retinoico X, reclutan cofactores específicos y se unen a elementos de respuesta del ADN con lo cual se estimula la transcripción de múltiples genes. No sólo es un regulador principal de la diferenciación de adipocitos sino también un sensibilizante a la insulina in vivo. La rosiglitazona es un agonista PPAR-&gamma sintético ampliamente utilizado en el tratamiento de pacientes con diabetes tipo 2 ya que eleva la sensibilidad a la insulina (20). La expresión de adiponectina está regulada por el desarrollo y se activa hacia el cuarto día de la diferenciación de adipocitos en células 3T3-L1 de cultivo (2). Debido a que los PPAR-&gamma son reguladores primarios de la diferenciación adipocitarlheight240 heterodímeros con el receptor retinoico X, reclutan cofactores específicos y se unen a elementos de respuesta del ADN con lo cual se estimula la transcripción de múltiples genes. No sólo es un regulador principal de la diferenciación de adipocitos sino también un sensibilizante a la insulina in vivo. La rosiglitazona es un agonista PPAR-&gamma sintético ampliamente utilizado en el tratamiento de pacientes con diabetes tipo 2 yia realizamos un estudio in vitro para determinar si un agonista de PPAR-&gamma podría regular la expresión de adiponectina en adipocitos 3T3-L1 completamente diferenciados. Observamos que la expresión de ARNm de adiponectina en estado de equilibrio en células diferenciadas 3T3-L1 se incrementaba con la administración de rosiglitazona durante 24 horas (21). Para determinar si la rosiglitazona podría elevar el nivel de adiponectina en la práctica clínica, estudiamos los niveles plasmáticos de adiponectina en pacientes con diabetes tipo 2 tratados con rosiglitazona en el contexto de un estudio clínico (22). Diseño del estudio y métodos
El estudio consistió en el seguimiento de un ensayo en fase III, a doble ciego, controlado con placebo y en paralelo, de comparación de rosiglitazona (BRL 49653C) y terapia simultánea con sulfonilurea. Las características del estudio se muestran en la tabla 1.

Los enfermos con diabetes seleccionados ingresaron inicialmente en un estudio a simple ciego con placebo y sulfonilurea durante 4 semanas con la finalidad de establecer las características basales. Luego iniciaron la fase a doble ciego durante la cual fueron asignados a rosiglitazona (Avandia, 2 mg, dos veces por día) o placebo durante 6 meses. Durante este período, los enfermos fueron controlados en 8 visitas. Después de evaluar la seguridad y eficacia de la rosiglitazona (23), 30 sujetos (de los 38 reclutados) en el grupo de rosiglitazona y 34 (de 39 reclutados) en el grupo placebo fueron observados durante 6 meses y representaron la cohorte de este estudio. La edad promedio al inicio de la diabetes fue de 50 años. Los parámetros antropométricos (peso corporal, talla, presión arterial y frecuencia cardíaca) fueron determinados en momentos especificados. Se tomaron muestras de sangre en ayunas para valorar la concentración de glucosa, colesterol total y triglicéridos en un analizador automático (Hitachi 7250 Special; Hitachi, Tokyo, Japón). Los niveles séricos de insulina se conocieron con un inmunoensayo de micropartículas enzimáticas con el sistema AxSYM (Laboratorios Abbott, Dainabot, Tokyo, Japón). La concentración de hemoglobina glucosilada (HbA1c) se midió con el equipo DCA2000 (Bayer Sankyo, Tokyo, Japón). El modelo de la homeostasis (HOMA) se empleó para estimar el grado de resistencia a la insulina y la función de las células β con la siguiente fórmula:HOMA-IR= insulina / 22.5e-ln(glucosa)
HOMA β= 20 x insulina / (glucosa - 3.5)
>en la cual la insulina y glucosa se expresan en μU/ml y en mmol/l, respectivamente (24). Los niveles plasmáticos de adiponectina se conocieron con un ensayo inmunoenzimático (11). La adiponectina se expresa en μ/ml y no en unidades SI porque el peso molecular de la adiponectina no se ha establecido con precisión. Los análisis estadísticos se realizaron con el sistema Statistical Analysis System (Edición 6.12; SAS Institute, Cary, NC). Las diferencias en las características clínicas entre los grupos se evaluaron con la prueba t de Student. Se realizaron varios modelos de regresión de variables múltiples en los cuales la edad, sexo, cambios en el nivel de glucemia en ayunas, concentración de HbA1c, índice de resistencia a la insulina según HOMA, IMC y estado del tratamiento se consideraron variables independientes. El cambio en la concentración de adiponectina en plasma fue la variable dependiente. La magnitud de la variabilidad atribuible al tratamiento se indica como r2 o r2 parcial en los modelos. La rosiglitazona incrementa en forma significativa los niveles plasmáticos de adiponectina
Los pacientes tratados con rosiglitazona y los que recibieron placebo no difirieron en las características clínicas basales (tabla 2).
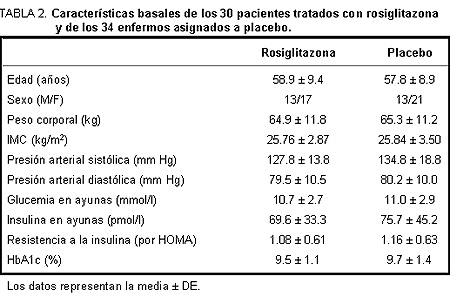
Tres meses después del tratamiento se detectaron diferencias significativas en la concentración plasmática promedio de adiponectina, glucemia en ayunas y concentración de HbA1c entre los dos grupos (datos no mostrados). Luego de 6 meses de tratamiento, los pacientes en el grupo de rosiglitazona presentaron un control de la glucemia sustancialmente mejor en términos de glucemia en ayunas y peso corporal en comparación con los sujetos del grupo placebo (tabla 3).

La resistencia a la insulina se redujo en el grupo de rosiglitazona luego de 6 meses pero la diferencia no fue significativa en comparación con el grupo placebo. La concentración de adiponectina en plasma aumentó más de dos veces en relación con los valores basales en los enfermos asignados a rosiglitazona mientras que se mantuvo casi sin cambios en los sujetos del grupo placebo (figura 1).

Figura 1. Media y EEM de los niveles de adiponectina en plasma al inicio y a los 3 y 6 meses de comenzado el tratamiento. Barras blancas, grupo placebo; barras negras, grupo con rosiglitazona. * P < 0.05; ** P < 0.01. (Reproducido con permiso)
El tratamiento con rosiglitazona durante 6 meses no se asoció con mayor aumento de la adiponectina en relación con los valores de los 3 meses, lo cual sugiere que el efecto de la rosiglitazona sobre los niveles de adiponectina se logran hacia el tercer mes. En los modelos de regresión lineal de múltiples variables en los que el cambio en el nivel de adiponectina se tomó como la variable dependiente y varios parámetros metabólicos como variables independientes encontramos que la modificación en la HbA1c, IMC y estado del tratamiento (uso de rosiglitazona o placebo) -aunque no la glucemia en ayunas y la resistencia a la insulina- se asociaron en forma significativa con la adiponectina luego del ajuste según edad y sexo. Sin embargo, ninguna de estas variables se mantuvo significativamente relacionada con la adiponectina, después del ajuste según el estado terapéutico (datos no mostrados). El análisis escalonado de regresión lineal de variables múltiples reveló que el tratamiento fue el único parámetro asociado con la modificación de la adiponectina plasmática (tabla 4) aunque el cambio en la resistencia a la insulina y el IMC se relacionaron en forma significativa con la modificación de la adiponectina antes del ajuste por tratamiento.
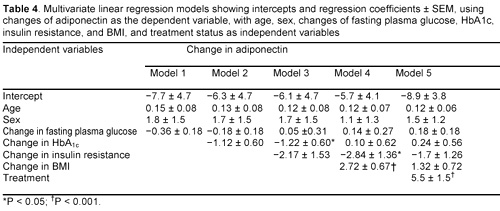
En el modelo sin ajuste, el estado terapéutico en forma exclusiva contribuyó con aproximadamente el 38% de la variabilidad en la modificación de la adiponectina en plasma (r2= 0.38). En el modelo corregido según otras variables (modelo 5), el estado del tratamiento contribuyó con alrededor del 24% de variabilidad (r2= 0.24) mientras que el r2 del modelo fue 0.44.Los resultados indican que el aumento en la concentración plasmática de adiponectina es consecuencia fundamentalmente del tratamiento con rosiglitazona. Mejoría de la sensibilidad a la insulina por adiponectina
Las funciones de la adiponectina se han ido descifrando en los últimos años. Aunque los estudios in vitro mostraron el efecto antiaterogénico, antiinflamatorio y apoptótico de la adiponectina (6-9), la evidencia firme que relaciona a la adiponectina con estas funciones biológicas in vivo es escasa. Muchas investigaciones in vivo, inclusive las llevadas a cabo por nuestro grupo, han mostrado asociación entre el bajo nivel de adiponectina en plasma, la resistencia a la insulina y todas las manifestaciones clínicas principales del síndrome metabólico (6,11-15). Sin embargo, la posible contribución directa de la concentración baja de adiponectina en la progresión de la diabetes o en la aceleración de la arteriosclerosis ha sido motivo de amplio debate. De hecho, en un estudio de observación longitudinal en monos, la disminución de la adiponectina plasmática se asoció con la aparición de resistencia a la insulina y diabetes (25). El nivel plasmático de la adiponectina también se relacionó con la medición directa de la sensibilidad a la insulina en los estudios de clampeo en el hombre (15). Más aún, la inyección de adiponectina recombinante en animales de experimentación aumentó la oxidación de ácidos grasos en músculo, mejoró la sensibilidad a la insulina y descendió la producción de glucosa hepática (16-18). Estos datos indican que la baja concentración de adiponectina puede contribuir con la fisiopatología de la resistencia a la insulina en pacientes con diabetes tipo 2 y también sugieren que la disponibilidad de adiponectina o su mayor expresión podrían representar nuevas modalidades de tratamiento de la resistencia a la insulina y de la diabetes tipo 2. Nuestro estudio aleatorizado y controlado con placebo en sujetos con diabetela medición directa de la sensibilidad a la insulina en los estudios de clampeo en el hombre (15). Más aún, la inyección de adiponectina recombinante en animales de experimentación aumentó la oxidación de ácidos grasos en músculo, mejoró la sensibilidad a la insulina y descendió la producción de glucosa hepática (16-18). Estos datos indican que la baja concentración de adiponectina puede contribuir con la fisiopatols tipo 2 demostró que el tratamiento con el agonista de los PPAR-&gamma -rosiglitazona- durante 3 meses duplica el nivel de adiponectina plasmática en estos pacientes. Los hallazgos brindan fuerte evidencia de que la producción endógena de adiponectina puede aumentarse con drogas como los agonistas del PPAR-γ, que podrían contribuir, de este modo, con un mejor control de la glucemia y con la reducción la resistencia a la insulina que se observa en estos enfermos. Además del tratamiento farmacológico, también encontramos que la pérdida de peso se asocia con elevación de los niveles de adiponectina en enfermos obesos. En un grupo de 22 pacientes con obesidad tratados con división gástrica, la reducción del 21% del IMC se acompañó de un incremento del 46% en el nivel promedio de adiponectina en plasma. La concentración de adiponectina también se correlacionó significativamente con el nivel de glucosa en plasma en estado de equilibrio (26). Estos estudios sugieren que la expresión de adiponectina endógena puede incrementarse, fenómeno que aumentaría la sensibilidad a la insulina. Unos pocos estudios animales brindan algo de comprensión en relación con los mecanismos por los cuales la adiponectina mejora la sensibilidad a la insulina. La inyección de adiponectina recombinante en modelos animales disminuye los niveles plasmáticos de ácidos grasos libres (16,17). Estos animales también mostraron mayor β oxidación de ácidos grasos en músculo esquelético, probablemente en forma secundaria a la mayor expresión de genes involucrados en la β oxidación y en la dispersión de energía, como la oxidasa acil-CoA y la proteína 2 de desacoplamiento (17). Como consecuencia, la adiponectina también redujo el contenido de triglicéridos en músculo. Debido a que los mayores niveles de ácidos grasos en plasma y el aumento del contenido de triglicéridos en músculo contribuyen con la resistencia a la insulina (27), es probable que la adiponectina mejore la sensibilidad a la insulina al descender los ácidos grasos y los triglicéridos. Además, la adiponectina también incrementó la fosforilación de tirosina de moléculas de señalización estimuladas por insulina, inclusive del receptor de insulina y el sustrato 1 del receptor de insulina en músculo esquelético (17). Sin embargo, aún debe investigarse si la mejoría en la sensibilidad a la insulina obedece al tratamiento con agonistas PPAR-γ o la reducción del peso mediada, al menos parcialmente, por la adiponectina.Si bien no investigamos la expresión de adiponectina en tejido adiposo en estos sujetos, especulamos que el incremento en la adiponectina en plasma asociada con rosiglitazona es secundario a la mayor transcripción del gen de adiponectina al activarse el factor de transcripción, PPAR-γ. Este hecho está avalado por los resultados de nuestro estudio previo en adipocitos murinos en cultivo en los cuales la rosiglitazona aumentó el nivel de ARNm de adiponectina en estado de equilibrio (21). El promotor proximal (1 kb) del gen de adiponectina humana sólo contiene la mitad del sitio del elemento de respuesta al PPAR-&gamma (AGGTCA entre -610 y -605 en relación al codón de iniciación ATG) (28,29). Su promotor proximal también contiene varios elementos regulatorios comúnmente observados en los promotores de genes expresados en tejido adiposo. Estos elementos cis- incluyen C/EBPs, SREBP, Ebox y GATA-1 (28,29). No obstante, existe la posibilidad de que la rosiglitazona incremente la estabilidad del ARNm de adiponectina o la síntesis, estabilidad y secreción de la proteína. En este trabajo observamos una correlación entre la concentración de adiponectina en plasma y la ganancia de peso luego del tratamiento con rosiglitazona. Estoe hallazgo parecería contradictorio a la correlación negativa previamente documentada entre la concentración plasmática de adiponectina y el peso corporal. La activación del PPAR-γ por rosiglitazona puede también, al incrementar la transcripción del gen de adiponectina, promover aumento del peso por una mayor diferenciación de los adipocitos y por el mayor número de adipocitos pequeños (30). Mientras este estudio sugiere algún tipo de interacción entre el PPAR-γ y el gen de adiponectina en los beneficios metabólicos, nuestros estudios genéticos brindaron información adicional de dicha conexión al mostrar que 1) la expresión del gen de adiponectina se relaciona con los fenotipos metabólicos y 2) que existe interacción genética entre los genes de adiponectina y de PPAR-&gamma que puede contribuir con la sensibilidad a la insulina. Expresión del gen de adiponectina y fenotipos metabólicos
Las variaciones genéticas en el gen humano de adiponectina han sido recientemente asociadas con el riesgo de obesidad, de diabetes tipo 2 y con elevación del colesterol asociado con lipoproteínas de baja densidad (31-33). En forma opuesta al amplio estudio a nivel de ADN y de proteínas plasmáticas, en el hombre sólo unas pocas investigaciones prestaron atención a la relevancia fisiológica del ARNm de adiponectina en tejido adiposo. Evaluamos la relación entre la expresión de ARNm de adiponectina de depósito específica de tejido adiposo y varios factores metabólicos en 66 mujeres que fueron sometidas a cirugía abdominal programada (34). La expresión de ARNm en tejido adiposo subcutáneo se correlacionó en forma negativa con la glucemia en ayunas mientras que la expresión de ARNm en tejido adiposo de epiplón se asoció en forma inversa con los niveles séricos de triglicéridos. Estos hallazgos mostraron que los niveles de ARNm de adiponectina en tejido adiposo se relacionan al menos con ciertos fenotipos del síndrome metabólico. Con la finalidad de establecer una asociación entre los genes de adiponectina con algunos fenotipos del síndrome metabólico, evaluamos el polimorfismo T94G del gen de adiponectina en 245 individuos no diabéticos y correlacionamos la frecuencia de alelos con varios parámetros del síndrome metabólico (35). Encontramos que la frecuencia del alelo G se relacionó con el IMC y que influyó directamente en la expresión de ARNm y de proteína en tejido adiposo. Más aún, el nivel de expresión de ARNm de adiponectina afectó la sensibilidad a insulina en adipocitos diferenciados 3T3-L1. Los hallazgos sugieren que el gen humano de adiponectina es un importante factor genético de conexión entre el síndrome de resistencia a la insulina y la obesidad. Interacción genética entre adiponectina y PPAR-γ
Nuestro grupo participó en el Stanford Asian-Pacific Program in Hypertension and Insulin Resistance (SAPPHIRe). En un estudio de asociación en hermanos y controles analizamos el genotipo de 1 793 descendientes chinos y japoneses de 601 familias hipertensas por el polimorfimso T94G del exón 2 del gen de adiponectina y el polimorfismo Pro12Ala del gen de PPAR-γ; correlacionamos los genotipos con la concentración sérica de insulina y el índice de resistencia a la insulina (HOMA-IR) como marcadores de sensibilidad a la insulina. El estudio genético del gen de PPAR-&gamma mostró que el polimorfismo Pro12Ala contribuye significativamente con la variación de la glucemia en ayunas, la glucemia a la hora y el HOMA-IR (36). El estudio del genotipo del gen de adiponectina mostró que el alelo T se asocia con mayor insulina a la hora y con mayor área bajo la curva de insulina (ABCi) in OGTT (37). Se encontraron interacciones importantes entre el gen de adiponectina y el genotipo PPAR-γ en la insulina en ayunas, insulina a las 2 horas y HOMA-IR. Nuestro estudio muestra que el gen de adiponectina se asocia con la sensibilidad a la insulina. Además, el efecto de la adiponectina está modificado por el genotipo PPAR-γ Pro12Ala lo cual refleja una interacción genética en asociación con la sensibilidad a la insulina. Estas observaciones avalan aún más el hecho de que la mayor expresión de adiponectina puede contribuir con el beneficio antihiperglucémico y posiblemente antiaterogénico de los agonistas PPAR-γ.
 Bibliografía del artículo
Bibliografía del artículo
- Funahashi T, Nakamura T, Shimomura I, et al. Role of adipocytokines on the pathogenesis of atherosclerosis in visceral obesity. Intern Med 1999;3:202.206.
- Hu E, Liang P, Spiegelman BM. AdipoQ is a novel adipocyte-specific gene dysregulated in obesity. J Biol Chem 1996; 271:10697-10703.
- Scherer PE, Williams S, Fogliano M, et al. A novel serum protein similar to C1q, produced exclusively in adipocytes. J Biol Chem 1995; 270:26746-26749.
- Maeda K, Okubo K, Shimomura I, et al. cDNA cloning and expression of a novel adipose specific collagen-like factor, apM1. Biochem Biophys Res Commun 1996; 221:286-289.
- Nakano Y, Tobe T, Choi-Miura NH, et al. Isolation and characterization of GBP28, a novel gelatin-binding protein purified from human plasma. J Biochem 1996; 120:803-812.
- Ouchi N, Kihara S, Arita Y, et al. Novel modulator for endothelial adhesion molecules: adipocyte-derived plasma protein adiponectin. Circulation 1999; 100:2473–2476.
- Ouchi N, Kihara S, Arita Y, et al. Adiponectin, an adipocyte-derived plasma protein, inhibits endothelial NF-kappa B signaling through a cAMP-dependent pathway. Circulation 2000;102:1296-1301.
- Yokota T, Oritani K, Takahashi I, et al. Adiponectin, a new member of the family of soluble defense collagens, negatively regulates the growth of myelomonocytic progenitors and the functions of macrophages. Blood 96:1723-1732, 2000
- Ouchi N, Kihara S, Arita Y, et al. Adipocyte-derived plasma protein, adiponectin,suppresses lipid accumulation and class A scavenger receptor expression in human monocyte-derived macrophages. Circulation 2001;103:1057-1063.
- Okamoto Y, Arita Y, Nishida M, et al. An adipocyte-derived plasma protein, adiponectin, adheres to injured vascular walls. Horm Metab Res 2000;32:47-50.
- Arita Y, Kihara S, Ouchi N, et al. Paradoxical decrease of an adipose-specific protein, adiponectin, in obesity. Biochem Biophys Res Commun 1999;257:79-83.
- Hotta K, Funahashi T, Arita Y, et al. Plasma concentrations of a novel, adipose-specific protein, adiponectin, in type 2 diabetic patients. Arterioscler Thromb Vasc Biol 2000;20:1595-1599.
- Yang WS, Lee WJ, Funahashi T, et al. Plasma adiponectin levels in overweight and obese Asians. Obesity Research 2002;10:1104-1110
- Huang KC, Chen CL, Chuang LM, et al. Plasma adiponectin levels and blood pressures in nondiabetic adolescent females. J Clin Endocrinol Metab 2003;88:4130-4134.
- Weyer C, Funahashi T, Tanaka S, et al. Hypoadiponectinemia in obesity and type 2 diabetes: close association with insulin resistance and hyperinsulinemia. J Clin Endocrinol Metab 2001; 86:1930-1935.
- Fruebis J, Tsao T-S, Javorschi S, et al. Proteolytic cleavage product of 30-kDa adipocyte complement-related protein increases fatty acid oxidation in muscle and causes weight loss in mice. Proc Natl Acad Sci U S A 2001;98:2005-2010.
- Yamaichi T, Kamon J, Waki H, et al. The fat-derived hormone adiponectin reverses insulin resistance associated with both lipoatrophy and obesity. Nat Med 2001;7:941-946.
- Berg AH, Combs TP, Du X, et al. The adipocyte-secreted protein Acrp30 enhances hepatic insulin action. Nat Med 2001;7:947-953
- Rocchi S, Auwerx J. Peroxisome proliferators-activated receptor-gamma: a versatile metabolic regulator. Annals of Medicine 1999; 31:342-351
- Whitcomb RW, Saltiel AR. Thiazolidinediones. Expert Opin Invest Drug 1995;4:1299-1309.
- Lin WS, Chang HM, Tai TY, et al. Effect of thiazolidinedione on gene expression in NIH3T3–L1 adipocytes (Abstract). Diabetes 1999;48 (Suppl. 1):A217.
- Yang WS, Jeng CY, Wu TJ, et al. Synthetic peroxisome proliferators-activated receptor-γ agonist, rosiglitazone, increases plasma levels of adiponectin in type 2 diabetic patients. Diabetes Care 2002;25:376-380.
- Balfour JA, Plosker GL. Rosiglitzaone. Drugs 1999;57:921-930.
- Mattews DR, Hosker JP, Rudenski AS, et al. Homeostasis model assessment: insulin resistance and beta-cell function from fasting plasma glucose and insulin concentrations in man. Diabetologia 1985; 28:412-419.
- Hotta K, Funahashi T, Bodkin NL, et al. Circulating concentrations of the adipocyte protein adiponectin are decreased in parallel with reduced insulin sensitivity during the progression to type 2 diabetes in Rhesus monkeys. Diabetes 2001;50:1126-1133.
- Yang WS, Lee WJ, Funahashi T, et al. Weight reduction increases plasma levels of an adipose-derived anti-inflammatory protein adiponectin. J Clin Endocrinol Metab 2001;86:3815-3819.
- Shulman GI. Cellular mechanism of insulin resistance. J Clin Invest 2000; 106:171-176.
- Saito K, Tobe T, Minoshima S, et al. Organization of the gene for gelatin-binding protein (GBP28). Gene 1999;229:67-73.
- Schäffler A, Langmann T, Palitzsch KD, et al. Identification and characterization of the human adipocyte apM-1 promoter. Biochim Biophys Acta 1998;1399:187-197.
- Okuno A, Tamemoto H, Tobe K, et al. Troglitazone increases the number of small adipocytes without the change of white adipose tissue mass in obese Zucker rats. J Clin Invest 1998;101:1354-1361.
- Stumvoll M, Tschritter O, Fritsche A, et al. Association of the T-G polymorphism in adiponectin (exon 2) with obesity and insulin sensitivity: interaction with family history of type 2 diabetes. Diabetes2002;51:37-41.
- Kondo H, Shimomura I, Matsukawa Y, et al. Association of adiponectin mutation with type 2 diabetes: a candidate gene for the insulin resistance syndrome. Diabetes 2002;51:2325-2328.
- Zietz B, Barth N, Scholmerich J, et al. Gly15Gly polymorphism within the human adipocyte-specific apM-1gene but not Tyr111His polymorphism is associated with higher levels of cholesterol and LDL-cholesterol in Caucasian patients with type 2 diabetes. Exp Clin Endocrinol Diabetes 2001;109:320-325.
- Yang WS, Chen MH, Lee WJ, et al. Adiponectin mRNA levels in the abdominal adipose depots of nondiabetic women. International Journal of Obesity 2003;27,896-900.
- Yang WS, Tsou PL, Lee WL, et al. Allele-specific differential expression of a common adiponectin gene polymorphism related to obesity. J Mol Med 2003;81:428-434.
- Chuang LM, Hsiung CA, Chen YD, et al. Sibling-based association study of the PPARgamma2 Pro12Ala polymorphism and metabolic variables in Chinese and Japanese hypertension families: a SAPPHIRe study. Stanford Asian-Pacific Program in Hypertension and Insulin Resistance. J Mol Med 2001;79:656-664
- Yang WS, Hsiung CA, Ho LT, et al. Genetic epistasis of adiponectin and PPARγ2 genotypes in modulation of insulin sensitivity: a family-based association study. Diabetologia 2003;46:977-983.
©
Está
expresamente prohibida la redistribución y la redifusión de todo o parte de los
contenidos de la Sociedad Iberoamericana de Información Científica (SIIC) S.A. sin
previo y expreso consentimiento de SIIC





 Artículos originales> Expertos del Mundo>
Artículos originales> Expertos del Mundo> Enviar correspondencia a:
Enviar correspondencia a:



