




 Artículos originales> Expertos del Mundo>
Artículos originales> Expertos del Mundo> Enviar correspondencia a:
Enviar correspondencia a: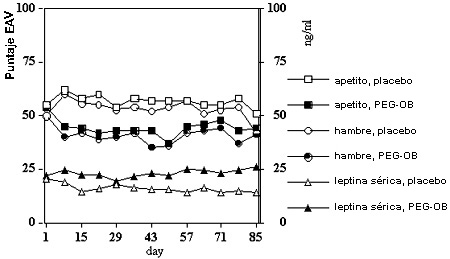
Figura 1. EAV (escala analógica visual). Eje izquierdo: puntuaciones de apetito y hambre. Eje derecho: valores séricos de leptina en el grupo de tratamiento con 20 mg/semana (n = 15) y en el placebo (n =15), todos antes del desayuno.Diferencias significativas en los cambios en el apetito y hambre durante el tratamiento en ambos grupos (ANOVA de dos factores, mediciones repetidas con interacción; p < 0.01). En los tratados con PEG-OB, el apetito y el hambre disminuyeron del día 1 al 8 y permanecieron en el nivel más bajo; con el placebo se incrementaron del día 1 al 8 y permanecieron al nivel más alto. Diferencias significativas en los cambios en las concentraciones séricas de leptina durante el tratamiento en ambos grupos dos factores de medidas repetidas con interacción; p < 0.05). Las concentraciones séricas de leptina en las muestras tomadas justo antes de la dosis siguiente semanal de PEG-OB aumentaron hasta un nuevo estadio de meseta durante las semanas 9-12 del estudio en los sujetos tratados. Las concentraciones totales cayeron con la pérdida de peso en el grupo placebo, alcanzando un nuevo estado de meseta también a las semanas 9-12.Reproducido con autorización de la American Journal of Clinical Nutrition . © Am J Clin Nutr. American Society for Clinical Nutrition.También la puntuación semanal del perfil de apetito antes del desayuno evidenció un cambio respecto de los valores basales: el apetito y el hambre disminuyeron en el grupo de leptina y aumentaron en el placebo (figura 1). 33,34 Durante el tratamiento, continuaron con valores significativamente más bajos comparados con el placebo. 33,34El gasto energético fue de 16.5 ± 2 MJ/d y 17.0 ± 2.8 MJ/d (basal), y 15.4 ± 2 MJ/d y 14.7 ± 2.2 MJ/d (después de 12 semanas de terapéutica) en los grupos de leptina y placebo, respectivamente. 33,34 Esto indica reducción en el consumo de energía de 1.1 ± 1 MJ/d en el primero y de 2.3 MJ/d en el segundo. Estas diferencias no fueron estadísticamente significativas entre los grupos (p = 0.07). 33,34Con respecto al metabolismo energético de 24 horas y las mediciones de oxidación de los sustratos en la cámara de respiración, después de 12 semanas de tratamiento con leptina o placebo, no se encontraron diferencias en el gasto de energía, la tasa metabólica durante el sueño o la oxidación de sustratos entre los grupos. 33,34 El gasto energético fue en promedio el 93% del basal. El CR no cambió significativamente en el período de tratamiento.En cuanto a la seguridad, la leptina parece ser en general bien tolerada y segura.Durante el período de tratamiento con 80 mg/semana de leptina, el peso corporal, el IMC, el porcentaje de grasa corporal, la masa grasa y la libre de ésta disminuyeron en forma significativa en ambos grupos. 35,36 Al final de este lapso, la pérdida de peso fue de 14.6 ± 0.8 kg en los que recibieron leptina versus 11.8 ± 0.9 kg con el placebo (p < 0.05). 35,36 El gasto energético y el CR disminuyeron significativamente en ambos grupos luego de 6 semanas de tratamiento. 35,36 Ninguno de estos cambios fue significativamente diferente entre los grupos. 35,36La puntuación de restricción dietética voluntaria (factor 1 TFEQ) aumentó significativamente en ambos grupos durante el período terapéutico. 36 La de hambre (factor 3 TFEQ) disminuyó en ambos. 36 En el grupo de leptina, la reducción en esta última durante las 6 semanas de tratamiento se relacionó positivamente con la pérdida de peso (r2 = 0.56; p < 0.01). 36Los tratados con leptina evidenciaron incrementos significativos en el peso y el IMC después de 4 y 8 semanas de seguimiento. 36 El aumento en el peso fue más lento en el grupo placebo respecto del de leptina (figura 2). 36
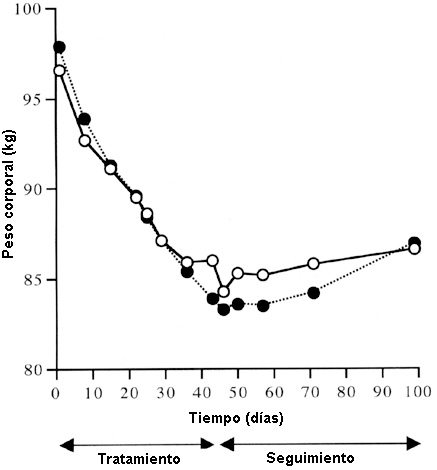
Figura 2. Recuperación de peso corporal a lo largo del tiempo para el placebo (O) (n = 10) y 80 mg/semana de leptina (•>) (n = 12).El peso corporal disminuyó significativamente en ambos grupos. 35,36 La pérdida media de peso fue 14.6 ± 0.8 kg en el grupo de leptina y 11.8 ± 0.9 kg en el placebo (p < 0.05). 35,36 El grupo de leptina mostró incrementos significativos en el peso corporal y el IMC después de 4 y 8 semanas de seguimiento. 36 El aumento en el peso fue más lento en el grupo placebo (p < 0.05). 36Durante el seguimiento, en el grupo placebo, la recuperación del peso se correlacionó en forma inversa con los cambios en la restricción alimentaria voluntaria (r2 = 0.60; p = 0.01) 36 y con la disminución en la puntuación (r2 = 0.47; p = 0.04). 36 Después de 8 semanas de seguimiento, la recuperación de peso en el grupo de leptina se correlacionó inversamente con el incremento en la restricción dietética voluntaria durante el período de tratamiento (r2 = 0.49; p < 0.02). 36 La recuperación en el seguimiento no se relacionó con el peso inicial o la pérdida del mismo durante la dieta con muy bajo aporte energético. 36DiscusiónEl tratamiento de hombres obesos con inyecciones subcutáneas semanales de 20 mg de leptina bajo condiciones de déficit energético de 1-2 MJ/d, produjo disminución en el apetito y en los niveles de hambre antes del desayuno en comparación con el placebo.33,34 Estas reducciones ocurrieron en el estado de abstinencia durante un período de equilibrio energético negativo. 34 Por el contrario, tanto el apetito como el hambre aumentaron en el grupo placebo. 34 Estas observaciones fueron paralelas al incremento en los niveles séricos de leptina en los tratados con esta sustancia y su reducción en los que recibieron placebo. 33,34 Además, se observó una disminución general del hambre, indicada por la valoración del TFEQ, en el grupo de leptina durante un período de equilibrio energético negativo comparado con el placebo, 34 pero que no provocó cambios en la limitación en la ingesta diaria de alimentos, la masa o los cambios en la composición corporales. 34 El tratamiento no evidenció un efecto independiente sobre el gasto calórico como los cambios en la tasa metabólica durante el sueño o en función de la masa libre de grasa. 34 Cuando los sujetos fueron sometidos a un equilibrio energético al corto plazo (a 93% del nivel original), no se encontraron variaciones en el perfil de apetito al final de las 12 semanas de terapia comparado con los valores basales ni diferencias entre los tratamientos. 34 La leptina a 20 mg/semana, modificó el apetito pero no cambió la composición corporal, el gasto energético o la pérdida de masa corporal comparado con el placebo. 34 Esto sugiere que la leptina tiene una actividad biológica predominantemente central en los hombres obesos. 34Durante las 6 semanas de tratamiento con leptina a 80 mg/semana, la pérdida de peso en ambos grupos (leptina y placebo) estuvo basada fundamentalmente en el incremento en la restricción dietética y en la reducción general en el hambre. 36 Sin embargo, la pérdida adicional en el grupo de leptina se debió a la administración de la dosis antes mencionada. 35,36 De este modo, los resultados referentes a la pérdida de peso son comparables a los estudios con modelos animales17,18 y a los trabajos de intervención iniciales en seres humanos. 22,23 La pérdida adicional de peso en el grupo de leptina durante el tratamiento probablemente no se debió a un efecto metabólico, ya que la reducción en la tasa metabólica en reposo fue similar en ambos grupos. 35,36 Esto es compatible con los resultados obtenidos durante el estudio con dosis menores. Por ende, las pérdidas extras de peso sólo pueden explicarse por la mayor restricción en la ingesta alimentaria en los tratados con leptina versus el placebo. 36 Se dieron instrucciones sobre la aceptación dietética independientemente de la terapéutica debido al incremento en los puntajes de restricción alimentaria voluntaria durante el programa de limitación energética. 36 La tasa de recuperación de peso corporal (expresada como porcentaje de pérdida de peso) después de 8 semanas de seguimiento fue mayor en el grupo de leptina respecto del placebo. 36 Debido a que no hubo una relación entre la recuperación de peso y la pérdida del mismo, puede decirse que no se debió a la mayor pérdida de peso. 36 Probablemente, el grupo placebo experimentó mayor apoyo en los cambios en los hábitos alimentarios y el hambre general para el mantenimiento del peso que el grupo de leptina. 36En conclusión, aunque el tratamiento con leptina llevó a mayor pérdida de peso corporal comparado con el placebo, el mantenimiento no fue sostenido por esta terapéutica. 36 Por el contrario, la restricción alimentaria fue más efectiva en el primer período de mantenimiento en el grupo placebo, lo que produjo una recuperación más lenta del peso. 36 Es probable que el tratamiento con leptina limite los cambios en el estilo de vida necesarios para la estabilización del peso después de haber adelgazado. 36 Quizá, para lograr mantener el peso luego del tratamiento con leptina se requiera su continuación con dosis más bajas.