HEPATOMETRIA ULTRA-SONOGRÁFICA EM CRIANÇAS: PROPOSTA DE NOVO MÉTODO - SÍNTESE COMENTADA E ESTUDO DE REPRODUTIBILIDADE INTER-OBSERVADORES
(especial para SIIC © Derechos reservados)
Coautores
Bety Spilberg Karpovas Chisman* Priscila Rodrigues Barbosa** Ilka Regina Souza de Oliveira*** Azzo Widman**** Luis Antonio Nunes Oliveira***** Giovanni Guido Cerri******
Médica Radiologista Assistente do Setor de Diagnóstico por Imagem do ICR/HC-FMUSP.*
Médica Colaboradora do Setor de Diagnóstico por Imagem do ICR/HC-FMUSP.**
Doutora em Medicina pela Universidade de São Paulo. Professora do Departamento de Radiologia da Faculdade de Medicina da Universidade de São Paulo.***
Doutor em Medicina pela Universidade de São Paulo. Médico Assistente Supervisor da Divisão de Cirurgia do Aparelho Digestivo II do HC-FMUSP.****
Médico Radiologista Diretor do Setor de Diagnóstico por Imagem do ICR/HC-FMUSP.*****
Professor Titular da Diciplina de Radiologia da Faculdade de Medicina da Universidade de São Paulo. Diretor da Divisão de Radiologia do INRAD/HC-FMUSP.******
Recepción del artículo: 4 de enero, 2005
Aprobación: 17 de enero, 2005
 Conclusión breve
O novo parâmetro de hepatometria em crianças é reprodutível por observadores diferentes e apresenta vantagens em relação ao parâmetro majoritariamente utilizado em outros métodos
Conclusión breve
O novo parâmetro de hepatometria em crianças é reprodutível por observadores diferentes e apresenta vantagens em relação ao parâmetro majoritariamente utilizado em outros métodos
 Resumen
Neste trabalho é exposto de forma sintética método ultra-sonográfico de biometria hepática em crianças, baseado em planos seccionais estabelecidos pela inter-relação de linhas de orientação externas a reparos anatômicos intra-abdominais, intra e extra-hepáticos. Em seguida é apresentado estudo da reprodutibilidade inter-observador de novo parâmetro por nós introduzido (diâmetro hepático crânio-caudal posterior na linha hemi-clavicular - CCPLHC) e do parâmetro classicamente utilizado na maioria dos estudos de hepatometria (diâmetro hepático crânio-caudal anterior na linha hemi-clavicular - CCALHC). Este trabalho contou com três observadores, que realizaram separadamente a hepatometria ultra-sonográfica em 31 crianças (entre 0 e 6 anos de idade). Foram excluídas da amostra crianças com doenças crônicas hepáticas ou das vias biliares. Para testar a reprodutibilidade foram utilizados o coeficiente de correlação de Pearson e o modelo de regressão linear. Os resultados mostraram haver correlação positiva e significante entre valores aferidos pelos três observadores para ambos os parâmetros. Aplicando-se o modelo de regressão linear observou-se que CCPLHC foi reproduzida por todos os observadores, enquanto que CCALHC não se mostrou reprodutível por qualquer dos observadores. Concluímos que o novo parâmetro de hepatometria em crianças é reprodutível por observadores diferentes e apresenta vantagens em relação ao parâmetro majoritariamente utilizado em outros métodos.
Resumen
Neste trabalho é exposto de forma sintética método ultra-sonográfico de biometria hepática em crianças, baseado em planos seccionais estabelecidos pela inter-relação de linhas de orientação externas a reparos anatômicos intra-abdominais, intra e extra-hepáticos. Em seguida é apresentado estudo da reprodutibilidade inter-observador de novo parâmetro por nós introduzido (diâmetro hepático crânio-caudal posterior na linha hemi-clavicular - CCPLHC) e do parâmetro classicamente utilizado na maioria dos estudos de hepatometria (diâmetro hepático crânio-caudal anterior na linha hemi-clavicular - CCALHC). Este trabalho contou com três observadores, que realizaram separadamente a hepatometria ultra-sonográfica em 31 crianças (entre 0 e 6 anos de idade). Foram excluídas da amostra crianças com doenças crônicas hepáticas ou das vias biliares. Para testar a reprodutibilidade foram utilizados o coeficiente de correlação de Pearson e o modelo de regressão linear. Os resultados mostraram haver correlação positiva e significante entre valores aferidos pelos três observadores para ambos os parâmetros. Aplicando-se o modelo de regressão linear observou-se que CCPLHC foi reproduzida por todos os observadores, enquanto que CCALHC não se mostrou reprodutível por qualquer dos observadores. Concluímos que o novo parâmetro de hepatometria em crianças é reprodutível por observadores diferentes e apresenta vantagens em relação ao parâmetro majoritariamente utilizado em outros métodos.
 Palabras clave
Fígado, dimensões, biometria, crianças, ultra-som, método
Clasificación en siicsalud
Palabras clave
Fígado, dimensões, biometria, crianças, ultra-som, método
Clasificación en siicsalud
 Artículos originales> Expertos del Mundo>
Artículos originales> Expertos del Mundo>
página www.siicsalud.com/des/expertos.php/71874
Especialidades
 Principal: Diagnóstico por Laboratorio, Pediatría,
Principal: Diagnóstico por Laboratorio, Pediatría,
 Relacionadas: Diagnóstico por Imágenes, Endocrinología y Metabolismo, Gastroenterología, Medicina Interna,
Relacionadas: Diagnóstico por Imágenes, Endocrinología y Metabolismo, Gastroenterología, Medicina Interna,
 Enviar correspondencia a:
Enviar correspondencia a:
Silvia Maria Sucena da Rocha. Instituto da Criança “Prof. Pedro de Alcântara” - Setor de Diagnóstico por Imagem. Av. Dr. Enéas de Carvalho Aguiar 647 2º Andar, CEP 05403-001 São Paulo, SP, Brasil.
SONOGRAPHIC BIOMETRY OF THE LIVER IN CHILDREN: PROPOSAL OF A NEW METHOD (SUMMARY AND COMMENTS) - STUDY OF INTER-OBSERVER REPRODUCIBILITY
 Abstract
Abstract
In this study we describe a sonographic biometric method to determine liver size in neonates, infants, and children up to 6 years old. Longitudinal section planes were based on external orientation lines related to intra-abdominal anatomic references, both extra and intra-hepatic, aiming to minimize observer related error. In order to study inter-observer reproducibility of a new parameter introduced (posterior cranio-caudal diameter at midclavicular line) and the parameter used in other methods (anterior cranio-caudal diameter at midclavicular line), three independent examiners performed sonographic liver biometry in 31 children (aged 0 to 6 years). Pearson’s coeficient and linear regression model were employed to determine inter-observer variability. Statistical analisis revealed positive and significant correlation between measurements performed by the three observers for both parameters. Linear regression model revealed that values of posterior cranio-caudal diameter at midclavicular line were reproducible by all observers, while values of anterior cranio-caudal diameter at midclavicular line were not reproducible by any observer. We conclude that the new parameter proposed is reproducible by different observers, therefore suitable to determine sonographic liver size in children, and a better parameter than anterior cranio-caudal diameter at midclavicular line, since its anatomic references are precise.
 Key words
Key words
Liver size, biometry, children, ultrasound, method
HEPATOMETRIA ULTRA-SONOGRÁFICA EM CRIANÇAS: PROPOSTA DE NOVO MÉTODO - SÍNTESE COMENTADA E ESTUDO DE REPRODUTIBILIDADE INTER-OBSERVADORES
(especial para SIIC © Derechos reservados)
Artículo completo
Introdução
O aumento do fígado é um achado clínico comum na infância, podendo ser decorrente de doença hepática intrínseca ou de alterações sistêmicas.1 A determinação do tamanho do fígado é, portanto, procedimento de rotina no exame clínico de crianças.
O método clínico de biometria hepática, contudo, apresenta limitações, decorrentes de variações na forma, eixo e posição do fígado,2,3 de suas relações com estruturas vizinhas2,4 e da técnica empregada,5,6 sendo operador dependente.7
A hepatometria “in vivo” pode, ainda, ser realizada por métodos de diagnóstico por imagem, tais como: radiografia,9,10-14 cintilografia,3,15-20 ultra-sonografia15,20-38 e tomografia computadorizada,39 que, por sua vez, procuram oferecer subsídios mais concretos, com melhor reprodutibilidade, com o objetivo, tanto de complementar a avaliação clínica, como de minimizar o fator operador-dependência deste procedimento.
Dentre os métodos de imagem, a ultra-sonografia apresenta vantagens, sobretudo na avaliação do paciente pediátrico, por tratar-se de método totalmente não invasivo, não utilizar radiação ionizante e não exigir sedação, além de permitir o estudo minucioso do parênquima e estruturas hepáticas. Assim, a ultra-sonografia é, de modo geral, o primeiro exame de imagem solicitado para esclarecimento diagnóstico, quando há suspeita clínica de hepatomegalia e o exame de escolha no monitoramento de alterações do tamanho do fígado, que possam ocorrer na evolução natural de doenças ou em conseqüência a terapia.
O método ultra-sonográfico, no entanto, tem como limitações o fator operador-dependência e as barreiras à progressão do feixe sonoro, representadas pelo ar e estruturas ósseas. As barreiras ao som assumem especial relevância no que se refere ao estudo do fígado, devido a sua localização, uma vez que, o acesso ao órgão pode ser prejudicado pela interposição dos arcos costais e porção variável de parênquima pulmonar que se insinua entre o fígado e a parede abdominal.
A forma do fígado constitui outro fator de dificuldade para a padronização de medidas, pois, sendo bizarra, grosseiramente semelhante a uma cunha e com ampla superfície superior, arredondada, exige definição de pontos de referência precisos quando se pretende padronizar uma técnica com boa reprodutibilidade.
No que se refere à hepatometria ultra-sonográfica em crianças, há multiplicidade de métodos propostos,21,24-26,28,33,35 o que, a nosso ver, revela a falta de um, que atenda às necessidades do examinador, isto é, um método preciso, reprodutível e de fácil execução.
Com o intuito de determinarmos um método que atendesse a essas prerrogativas, realizamos estudo de mensuração do fígado de crianças, entre 0 e 6 anos de idade,40 em que avaliamos diversos parâmetros de hepatometria, quanto à reprodutibilidade inter-observador e quanto às dificuldades técnicas para sua obtenção. Nesse trabalho foi realizada, ainda, a análise de correlação dos diversos parâmetros entre si.
Método
Propomos método de biometria hepática baseado em dois planos seccionais longitudinais, estabelecidos pela inter-relação de reparos anatômicos intra-abdominais, intra e extra-hepáticos. Para a avaliação do tamanho do fígado são utilizados dois parâmetros: a) o diâmetro crânio-caudal do lobo hepático esquerdo, medido na linha médio esternal (LME), tendo como reparo anatômico intra-hepático a veia hepática esquerda e b) o diâmetro crânio-caudal posterior do lobo hepático direito, na linha hemi-clavicular (LHC), tendo como reparo anatômico intra-hepático o ramo portal direito (figuras 1, 2 e 3).
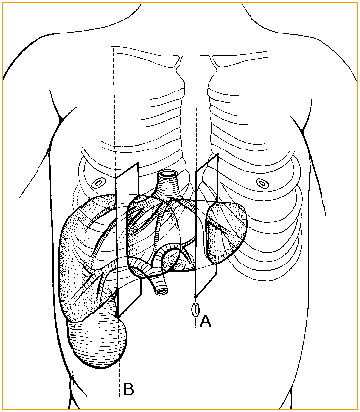
Figura1. Representação esquemática dos planos de corte para a hepatometria em crianças, estabelecidos pelas linhas de orientação externas: A (linha médio-esternal, para a medida do lobo hepático esquerdo) e B (linha hemi-clavicular, para a medida do lobo hepático direito).
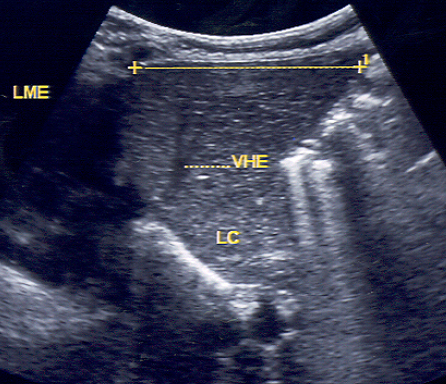
Figura 2. Medida do diâmetro crânio-caudal do lobo hepático esquerdo na linha médio-esternal (LME), tendo como reparo anatômico intra-hepático a veia hepática esquerda (VHE). Ressalta-se que a veia cava inferior não deve ser incluída na imagem. LC: lobo caudado.
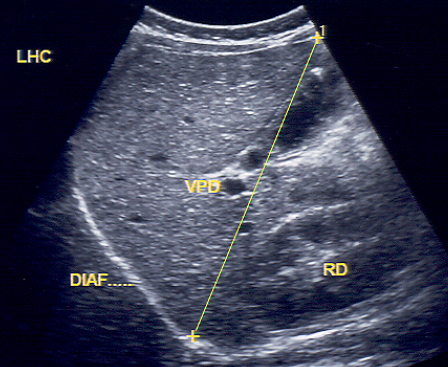
Figura 3. Medida do diâmetro crânio-caudal posterior do lobo hepático direito, medido na linha hemi-clavicular (LHC), tendo com reparo anatômico intra-hepático a veia porta direita (VPD), em corte transversal. Reparos anatômicos intra-abdominais extra-hepáticos: rim direito (RD) e ampla visualização do diafragma.
Comentários
O método proposto foi composto pelos parâmetros que apresentaram menores dificuldades técnicas e altos índices de correlação positiva com os demais parâmetros estudados, de forma a poderem representá-los. Ressalta-se que o diâmetro antero-posterior do lobo hepático esquerdo não apresentou correlação com qualquer dos parâmetros analisados.
O método se mostrou reprodutível por um mesmo observador e a introdução de reparos anatômicos intra-hepáticos resultou proveitosa, permitindo definição mais precisa dos planos de corte para aferição das medidas, minimizando o fator operador-dependência.
Estudo da variabilidade inter-observador
No período entre Agosto e Outubro de 2002 foi realizado estudo com o objetivo de testar a reprodutibilidade inter-observador do novo parâmetro introduzido (diâmetro crânio-caudal posterior na linha hemi-clavicular - CCPLHC) e do parâmetro classicamente utilizado para a medida do lobo hepático direito (diâmetro crânio-caudal anterior na linha hemi-clavicular - CCALHC).
População de estudo e metodo
Três examinadores independentes realizaram a biometria hepática em 31 crianças, com idades entre 0 e 6 anos, aplicando método ultra-sonográfico padronizado. Todas as crianças haviam sido encaminhadas para exame de ultra-sonografia abdominal no Setor de Diagnóstico por Imagem do ICR devido a suspeitas diagnósticas diversas. Foram excluídas da amostra crianças com doenças crônicas hepáticas ou das vias biliares.
Os exames de ultra-sonografia foram realizados em Modo-B, com equipamento ATL modelo APOGEE 800 PLUS e Aloka modelo SS-2000, utilizando-se transdutor convexo de 5.0 MHz.
A biometria hepática foi realizada separadamente por cada um dos examinadores (observador 1, 2 e 3), sem uma ordem pré-definida. Foram medidos os diâmetros CCPLHC e CCALHC.
A variabilidade inter-observadores foi testada utilizando-se o coeficiente de correlação de Pearson e o modelo de regressão linear.
Resultados
Os valores das medidas dos diâmetros CCPLHC e CCALHC obtidos pelos observadores 1, 2 e 3 são apresentados na tabela 1.
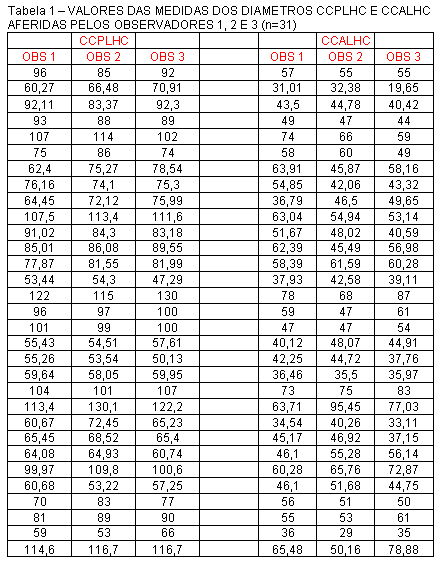
Os resultados do estudo de correlação mostraram que houve correlação positiva e significante entre os valores das medidas obtidas pelos três observadores para ambos os parâmetros analisados, ou seja, para um mesmo parâmetro, quanto maior o valor obtido por um observador, maior o valor obtido pelo outro.
Aplicando-se o modelo de regressão observou-se que os observadores 1, 2 e 3 reproduziram os valores de CCPLHC, enquanto que não houve reprodução dos valores de CCALHC por qualquer dos observadores.
Nos gráficos 1 a 6 são apresentados os coeficientes de correlação de Pearson (r), o nível de significância (p) e os modelos de regressão linear para os valores de CCPLHC (gráficos 1, 2 e 3) e CCALHC (gráficos 4, 5 e 6).
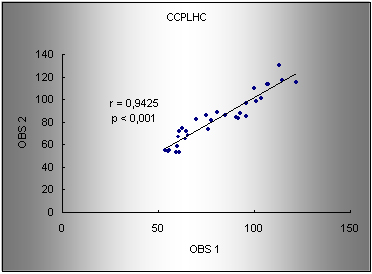
Gráfico 1. Regressão para os valores de CCPLHC entre os observadores 1 e 2. r: coeficiente de correlação de Pearson. Modelo de regressão: obs1 = 5.65 + 0.91 (obs2).
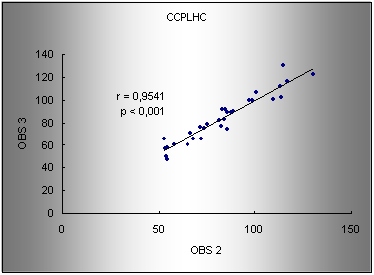
Gráfico 2. Regressão para os valores de CCPLHC entre os observadores 2 e 3. r: coeficiente de correlação de Pearson. Modelo de regressão: obs2 = 3.26 + 0.96 (obs3).
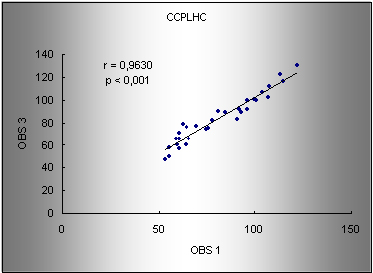
Gráfico 3. Regressão para os valores de CCPLHC entre os observadores 1 e 3. r: coeficiente de correlação de Pearson. Modelo de regressão: obs1 = 3.45 + 0.93 (obs3).

Gráfico 4. Regressão para os valores de CCALHC entre os observadores 1 e 2. r: coeficiente de correlação de Pearson. Modelo de regressão: obs1 = 17.52 + 0.68 (obs2).
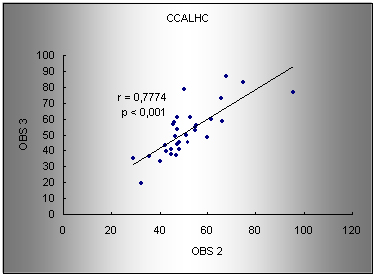
Gráfico 5. Regressão para os valores de CCALHC entre os observadores 2 e 3. r: coeficiente de correlação de Pearson. Modelo de regressão: obs2 = 17.82 + 0.64 (obs3).

Gráfico 6. Regressão para os valores de CCALHC entre os observadores 1 e 3. r: coeficiente de correlação de Pearson. Modelo de regressão: obs1 = 17.27+ 0.63 (obs3).
Discussão
A maioria dos estudos de biometria hepática em crianças21,24-26,33,34 propõe como parâmetro para avaliação do tamanho do lobo hepático direito a medida do comprimento da borda anterior do fígado na linha hemi-clavicular (“liver span”), que denominamos CCALHC. Esse parâmetro, no entanto, utiliza a interface hepato-diafragmática anterior como um dos reparos anatômicos. A falta de definição dessa interface, pela interposição de arcos costais e/ou parênquima pulmonar, pode comprometer a precisão da medida e resultar em discrepâncias ao se tentar reproduzi-la.15 Em estudo realizado anteriormente40 comprovamos a reprodutibilidade de CCALHC por um mesmo observador. No presente estudo, porém, os resultados não mostraram reprodutibilidade deste parâmetro por observadores diferentes.
O novo parâmetro que introduzimos para avaliação do comprimento hepático na linha hemi-clavicular (CCPLHC), tem como referência a interface hepato-diafragmática posterior. Esta interface, pela ausência de interposição de parênquima pulmonar, mostra-se nítida, permitindo definição precisa dos limites do órgão. CCPLHC mostrou-se reprodutível, tanto em estudo de variabilidade intra-observador,40 como neste de variabilidade inter-observadores, devido à definição precisa de seus pontos de referência.
Conclusão
Pelo apresentado, concluímos que o novo parâmetro de hepatometria em crianças é reprodutível por observadores diferentes, indicando que pode ser utilizado na determinação das dimensões do fígado em crianças e apresenta vantagens em relação ao parâmetro majoritariamente utilizado em outros métodos.
Presentemente estamos realizando estudo populacional para a determinação ultra-sonográfica dos valores normais do tamanho do fígado de crianças em idade pré-escolar na cidade de São Paulo (Brasil) aplicando o método testado.
Los autores no manifiestan conflictos.
 Bibliografía del artículo
Bibliografía del artículo
- Walker WA, Mathis RK. Hepatomegaly. Pediatric Clin North Am, v. 22, p. 929-42, 1975.
- Bricks LF, Kobinger ME, Rañna W. Hepatoesplenomegalia In: Marcondes E. Pediatria Básica 8a ed. São Paulo, Savier, 1991, p. 193-197.
- Sullivan S, Krasner N, Willians R. The clinical estimation of liver size: a comparison of thechniques and an analysis of the source of error. British Medical Journal, v. 2, p. 1042-3, 1976.
- Lawson EE, Grand RJ, Neff RK, Cohen LF. Clinical estimation of liver span in infants and children. Am J Dis Child, v. 132, p. 474-6, 1978.
- Castell DO, O'Brien KD, Munch H, Chalmers T. Estimation of liver size by percussion in normal individuals. Ann Intern Med, v. 70, p. 1183-1189.
- Younoszai MK, Mueller S. Clinical assesment of liver in normal children. Clin Pediatr, v. 14, p. 378-80, 1975.
- Weisman LE, Cagle N, Mathis R, Merenstein GB. Clinical estimation of liver size in the normal neonate. Clin Pediatr (Phila), v. 21, p. 596-598, 1982.
- Carpentieri U, Gustavson LP, Leach TM, Bruce H. Liver size in normal infants and children. South Med J, v. 70, p. 1096-1097, 1977.
- Deligeorgis D, Yannakos D, Panatotou P, Doxiadis S. The normal borders of the liver in infancy and childhood - clinical and x-ray study. Arch Dis Child, v. 45, p. 702-704, 1970.
- Walk L. Roengenologic determination of the liver volume. Acta Radiol, v. 55, p. 49-56, 1961.
- Walk L. Assessment of liver size. Digestion, v. 1, p. 289-295, 1968.
- Walk, L. Quantitative method to determine liver size. Radiologe, v. 18, p. 354-355, 1078.
- Walk L. Normal liver size as determined with quantitative methods. Radiologe, v. 22, p. 188-189, 1982.
- Walk L. Liver size in children determined with quantitative methods. Radiologe, v. 25,p. 221-223, 1985.
- Holder LE, Strife J, Padikal TN, Perkins PJ, Kereiakes JG. Liver size determination in pediatrics using sonographac and scintigraphic techniques. Radiology, v. 117, p. 349-53, 1975.
- Markisz JA, Treves ST, Davis RT. Normal hepatic and splenic size in children: scintigraphic determination. Pediatr Radiol, v.17, p. 273-276, 1987.
- Naftalis J, Leevy CM. Clinical estimation of liver size. Am J Diag Dis, v. 8, p. 236-243, 1963.
- Peternel WW, Schaefer JW, Shiff L. Clinical evaluation of liver size and hepatic scintiscan. Am J Dis Child, v. 11, p. 346-50, 1966.
- Rosenfield AT, Scheider PB. Rapid evaluation of hepatic size on radioisotope scan. J Nucl Med, v.15 , p. 237-240, 1974.
- Skrainka B, Stahlhut J, Fullbeck CL, Knight F, Holmes RA, Butt JH. Measuring liver span: bedside examination versus ultrasound and scintiscan. J Clin Gastroenterol, v. 8, p. 267-270, 1986.
- Assadamongkol K, Phuapradit P, Udompanich O, Varavithya W. Liver size and serum alkaline phosphatase in normal Thai school - aged children. J Med Assoc Thai, v. 72, suplplement 1, p. 88-93, 1989.
- Baddeley H, Benson M, Liefman G, Singcharoen T et al. Measurements of liver volume using water delay ultrasonography. Diagn Imag Clin Med, v. 55, p. 330-336, 1986.
- Carr D, Duncan JG, Railton R, Smith CB. Liver volume determination by ultrasound: a feasebility study. Br J Radiol, v. 49, p. 776-778, 1976.
- Chen CM, Wang JJ. Clinical and sonographic assessment of liver size in normal chinese neonates. Acta Paediatr, v. 82, p. 345-347, 1993.
- Dittrich M, Milde S, Dinkel E, Baumann W, Weitzel D. Sonografic biometry of liver and spleen in children. Pediatr Radiol, v. 13 , p. 349-353, 1983.
- Friis H, Ndhlovu P, Mduluza T et al. Ultrasonographic organometry: liver and spleen among children in Zimbabwe. Trop Med Int Health, v. 1, p. 183-190, 1996.
- Gosink BB, Leymaster CE. Ultrasonic determination of hepatomegaly. J Clin Ultrasound, v. 9, p. 37-41, 1981.
- Haddad-Zebouni S, Hindy R, Slaba S et al. Évaluation échographique de la taille des reins, du fois et de la rate chez l'enfant. Arch Pédiatr, v. 6, p. 1266-1270, 1999.
- Hessel G. Hepatometria na infância - comparação entre o método clínico e ultra - sonográfico. Campinas, 1991. Dissertação (Mestrado) - Faculdade de Ciências Médicas da Universidade Estadual de Campinas - SP.
- Holmes JH, Sundgren C, Ilke D, Finch J. A simple ultrasonic method for evaluating liver size. J Clin Ultrasound, v. 5, p. 89-91, 1977.
- Jungthirapanich J, Kaewtubtim J, Poovorawan Y. A new reference line for measuring the liver size in healthy newborns. J Assoc Thai, v. 81, p. 038-043, 1998.
- Kardel T, Holm HH, Rasmussen SN, Mortensen T. Ultrasonic determination of liver and spleen volumes. Scand. J Clin Lab Invest, v.27, p. 123-128, 1971.
- Konus Ö, Özdemir A, Akkaya A, Erbas G, Celik H, Isik S. Normal liver, spleen, and kidney dimensions in neonates, infants, and children: evaluation with sonography. A J R, v. 171, p. 1693-1698, 1998.
- Niederau C, Sonnenberg A, Müller JE, Erckenbrecht JF, Scholten T, Fritsch WP. Sonographic measurements of the normal liver, spleen, pancreas, and portal vein. Radiology, v. 149, p. 537-540, 1983.
- Phuapradit P, Assadamongkol K, Udompanich O, Varavithya W. Liver size and serum alkaline phosphatase in normal Thai school - aged children. J Med Assoc Thai, v. 69, suplplement 2, p. 69-76, 1986.
- Rasmussen, S N. Liver volume determination by ultrasonic scanning. Dan Med Bull, v. 25, p. 1-46, 1978.
- Rylance GW, Moreland TA, Cowan MD, Clark DC. Liver volume estimation using ultrasound scanning. Arch Dis Child, v. 57, p. 283-286, 1982.
- Wladimiroff JW, Sekeris A. Ultrasonic assessment of liver size in the newborn. J Clin Ultrasound, v. 5, p. 316-320, 1977.
- Jones JH, Robinson PJ. Organ volume determination by CT scanning: reduction of respiration induced erros by feed back monitoring. J Comput Assist Tomogr, v. 10, p. 167-171, 1986.
- Rocha SMS, Oliveira IRS, Widman A, Chisman BSK, Fukushima JT, Oliveira LAN, Cerri GG. Hepatometria ultra-sonográfica em crianças (proposta de novo método). Radiol Bras, v.36, p. 63-70, 2003.
©
Está
expresamente prohibida la redistribución y la redifusión de todo o parte de los
contenidos de la Sociedad Iberoamericana de Información Científica (SIIC) S.A. sin
previo y expreso consentimiento de SIIC





 Artículos originales> Expertos del Mundo>
Artículos originales> Expertos del Mundo> Enviar correspondencia a:
Enviar correspondencia a:








