




 Artículos originales> Expertos del Mundo>
Artículos originales> Expertos del Mundo> Enviar correspondencia a:
Enviar correspondencia a:
Figura 1. Señales inducidas por el TLR y estimulación de la inmunidad natural y adquirida. La unión de un ligando al TLR sobre una CPA inicia una cascada bioquímica que incluye los adaptadores MyD88 y símil MyD88, lo que induce la fosforilación de la IRAK, la activación del complejo de la quinasa IκB (complejo IKK) y la fosforilación de la IκB. La fosoforilación de la IκB produce la translocación nuclear del NF-κB, lo cual induce las citoquinas inflamatorias y moléculas coestimulantes (B7-1 y B7-2, también denominadas CD80 y CD86). La estimulación de las células T naive provocada por las interacciones entre los ligandos B7, el receptor CD28, los complejos del péptido CMH-II y el TCR resulta en la activación de las células T (inmunidad adquirida). Las células T se transformarán en células Th1 o Th2 en relación con la estimulación de las citoquinas IFN-γ o IL-4, respectivamente.Existen por lo menos 11 TLR identificados en los mamíferos, aunque en humanos el gen TLR11 es silente.3 Los TLR forman homodímeros que reconocen ligandos específicos o heterodímeros que distinguen varios ligandos y estimulan las vías de señalización que llevan a la expresión diferencial de genes o citoquinas inflamatorias o moléculas coestimulantes.12 Esta expresión genética dependería de la combinación particular de un TLR con una de las moléculas adaptadoras.13 En algunos casos, los TLR también pueden interactuar con receptores no relacionados para reconocer una amplia variedad de ligandos (tabla 1). Por lo tanto, la heterodimerización o la cooperación con receptores no relacionados permite que unos pocos TLR reconozcan un número importante de ligandos e induzcan diferencialmente la producción de citoquinas.14


Figura 2. Estructuras de segmentos repetitivos para: (A) pectina nativa o ácido poligalacturónico; (B) el análogo del antígeno de S. typhi Vi u O-acetilpectina en donde C-2 y C-3 están O-acetilados con Ac = CH3-C (0)-; y (C) el producto pectina-benzaldehído con el residuo benzaldehído unido a un grupo carboxilo a través de una etilén diamina.Por el contrario, la inmunización con pectina-benzaldehído (figura 2C) asociada al péptido antígeno resultó en la producción de un título elevado de anticuerpos (figura 3). Sin embargo, la formación de un polisacárido aldehído quizá no sea suficiente para conferir propiedades inmunopotenciadoras. El manano-benzaldehído indujo la inmunidad Th1, mientras que el periodato oxidado dextrano con contenido de grupos aldehídos no potenció la actividad inmune, lo que indica la existencia de estructuras aún no determinadas (Marciani y col., observaciones no publicadas).
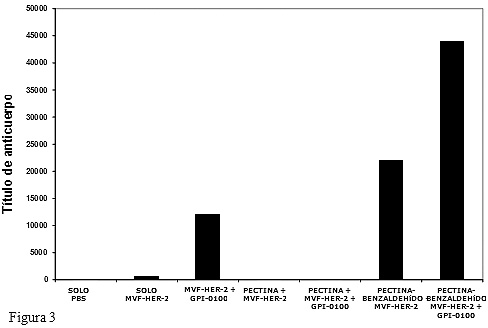
Figura 3. Efectos inhibitorio y sinérgico de la pectina y pectina-benzaldehído sobre la respuesta inmune contra un péptido quimérico de 42 aminoácidos del MVF-HER-2. Se inmunizaron por vía subcutánea ratones BALB/c de siete semanas de edad (5 por grupo) en los días 1 y 15 con 50 mcg de péptido solo o 100 mcg de GPI-0100, 120 mg de pectina, 100 mcg de GPI-0100 + 10 mg de pectina, 10 mg de pectina-benzaldehído y 100 mcg de GPI-0100 + 10 mg de pectina-benzaldehído. Los controles negativos fueron inmunizados con PBS estéril. Los animales fueron sacrificados 14 días después de la segunda inmunización y se determinó el IgG antígeno específico plasmático con ELISA en placas o platos de microtitulación recubiertas con el péptido MVF-HER-2.En relación con la creación de una vacuna, la pectina-benzaldehído asociada a GPI-0100 mostró un efecto sinérgico sobre la respuesta humoral. Así, el aumento del título de anticuerpos inducido por esta asociación fue significativamente mayor al producido por cada agonista o su suma (figura 3). El hecho de que este sinergismo no fuera causado por la combinación del GPI-0100 con la pectina se demostró a través de la inhibición de la respuesta humoral inducida por el análogo de las saponinas (figura 3). Si bien se desconocen los motivos de este efecto inhibidor, es improbable que la pectina aniónica hidrofílica “secuestre” el GPI-0100. A pesar de que se dispone de pocos datos relacionados con las propiedades inmunorreguladoras de la pectina, es posible que la inmunosupresión sea causada por el ácido poligalacturónico a través de mecanismos similares a los inducidos por el antígeno de S. typhi Vi.38 No obstante, el agregado de grupos formadores de imina a un polisacárido que no es ligando del TLR ni agente inmunopotenciador produjo un agonista Th1 efectivo. Este hallazgo muestra que los polisacáridos son plataformas adecuadas para construir agonistas inmunopotenciadores efectivos. A través de la modificación de polisacáridos ligandos del TLR se puede inducir tanto la inmunidad natural como la adquirida, requisito básico para desarticular la autotolerancia e inducir la autoinmunidad como en el caso de las vacunas oncológicas.