EFECTIVIDAD, TOXICIDAD Y PRONOSTICO POTENCIAL DE LA QUIMIOTERAPIA CON VBM EN EL ESTADIO TEMPRANO DEL LINFOMA DE HODGKIN. EXPERIENCIA DEL GRUPPO ITALIANO PER LO STUDIO DEI LINFOMI (GISL)
(especial para SIIC © Derechos reservados)
Coautores
Francesco Valentino, Chiara Broglia* Stefano Luminari, Caterina Mammi, Massimo Fed** Giuseppe Polimeno*** Francesco Merli**** Emilio Iannitto***** Caterina Stelitano****** Giovanni Quarta******* Enrico Capochiani********
Università di Pavia, IRCCS Policlinico S. Matteo*
Università di Modena, Policlinico di Mod**
Ospedale “Miulli”, Acquaviva delle Fonti***
Arcispedale “S. M. Nuova”, Reggio Emilia****
Cattedra-Divisione Ematologia con TMO, Università, Policlinico di Palermo*****
Ospedali Riuniti “Bianchi, Melacrino, Morelli”, Reggio Calabria******
Ospedale “A. Perrino”, Brindisi*******
Dipartimento Oncologico, Ospedale di Livorno********
Recepción del artículo: 19 de octubre, 2005
Aprobación: 25 de octubre, 2005
 Conclusión breve
Para el tratamiento del linfoma de Hodgkin, el régimen quimioterapéutico con vinblastina, bleomicina y metotrexato (VBM) asociado a la radioterapia constituye el estándar de referencia. Este esquema, modificado y sumado al tratamiento radiante de los sitios afectados casi no presenta toxicidad pulmonar o hematológica.
Conclusión breve
Para el tratamiento del linfoma de Hodgkin, el régimen quimioterapéutico con vinblastina, bleomicina y metotrexato (VBM) asociado a la radioterapia constituye el estándar de referencia. Este esquema, modificado y sumado al tratamiento radiante de los sitios afectados casi no presenta toxicidad pulmonar o hematológica.
 Resumen
Antecedentes: La quimioterapia con vinblastina, bleomicina y metrotexato (VBM) asociada a la irradiación constituye una combinación terapéutica efectiva en el estadio temprano del linfoma de Hodgkin, aunque se publicaron resultados contradictorios respecto de la toxicidad y la indicación adecuada de esta asociación. Pacientes y métodos: El GISL trató y evaluó –en dos ensayos clínicos– 169 pacientes en fases tempranas de la enfermedad de Hodgkin con presentación favorable. En el primer estudio (MH-1), realizado entre 1998 y 1995, 87 pacientes fueron medicados con el esquema VBM original asociado a radioterapia de campo extendido (EF-RT). En el ensayo siguiente (MH-1b), llevado a cabo entre 1996 y 2004, se incrementaron las dosis de vinblastina y metrotexato, se redujeron las de bleomicina y se administró una pequeña cantidad de prednisona junto con la infusión de cualquier droga antitumoral (VbMp); la irradiación se limitó solamente a los sitios afectados (IF-RT) y debía comenzar al menos 25 días después de la finalización de la quimioterapia. De los 82 pacientes tratados con el protocolo MH-1b, 67 tenían 65 años o menos (MH-1b < 65) y 15 eran mayores (MH-1b > 65). Resultados: La remisión completa fue obtenida por 96%, 91% y 80% de los pacientes de los estudios MH-1, MH-1b < 65 y MH-1b > 65, respectivamente; las tasas de recaída fueron del 12%, 9% y 0 y las medianas de los períodos de seguimiento de 111, 55 y 49 meses. Para la totalidad del grupo MH-1, la toxicidad pulmonar fue aceptable y más grave cuando la quimioterapia siguió a la radioterapia y no a la inversa. En el grupo M-1b < 65, estas toxicidades fueron mitigadas y en el MH-1b > 65, 3 de 15 pacientes fueron afectados por infecciones graves. Conclusiones: La VbMp seguida de radioterapia del campo afectado presenta una toxicidad hematológica y pulmonar casi nula. El protocolo modificado pareció tan efectivo como el original VBM + EF-RT y las diferencias fueron mínimas y estadísticamente no significativas. En fases de investigación se estudia el agregado de ciclofosfamida al régimen VbMp con el fin de mejorar su poder citodestructor. El objetivo está constituido por la curación, incluso de las formas tempranas y no favorables de la enfermedad, a través de la aplicación de radioterapia exclusivamente a los sitios afectados y evitar el riesgo de cardiotoxicidad tardía que se observa en las asociaciones con antraciclinas.
Resumen
Antecedentes: La quimioterapia con vinblastina, bleomicina y metrotexato (VBM) asociada a la irradiación constituye una combinación terapéutica efectiva en el estadio temprano del linfoma de Hodgkin, aunque se publicaron resultados contradictorios respecto de la toxicidad y la indicación adecuada de esta asociación. Pacientes y métodos: El GISL trató y evaluó –en dos ensayos clínicos– 169 pacientes en fases tempranas de la enfermedad de Hodgkin con presentación favorable. En el primer estudio (MH-1), realizado entre 1998 y 1995, 87 pacientes fueron medicados con el esquema VBM original asociado a radioterapia de campo extendido (EF-RT). En el ensayo siguiente (MH-1b), llevado a cabo entre 1996 y 2004, se incrementaron las dosis de vinblastina y metrotexato, se redujeron las de bleomicina y se administró una pequeña cantidad de prednisona junto con la infusión de cualquier droga antitumoral (VbMp); la irradiación se limitó solamente a los sitios afectados (IF-RT) y debía comenzar al menos 25 días después de la finalización de la quimioterapia. De los 82 pacientes tratados con el protocolo MH-1b, 67 tenían 65 años o menos (MH-1b < 65) y 15 eran mayores (MH-1b > 65). Resultados: La remisión completa fue obtenida por 96%, 91% y 80% de los pacientes de los estudios MH-1, MH-1b < 65 y MH-1b > 65, respectivamente; las tasas de recaída fueron del 12%, 9% y 0 y las medianas de los períodos de seguimiento de 111, 55 y 49 meses. Para la totalidad del grupo MH-1, la toxicidad pulmonar fue aceptable y más grave cuando la quimioterapia siguió a la radioterapia y no a la inversa. En el grupo M-1b < 65, estas toxicidades fueron mitigadas y en el MH-1b > 65, 3 de 15 pacientes fueron afectados por infecciones graves. Conclusiones: La VbMp seguida de radioterapia del campo afectado presenta una toxicidad hematológica y pulmonar casi nula. El protocolo modificado pareció tan efectivo como el original VBM + EF-RT y las diferencias fueron mínimas y estadísticamente no significativas. En fases de investigación se estudia el agregado de ciclofosfamida al régimen VbMp con el fin de mejorar su poder citodestructor. El objetivo está constituido por la curación, incluso de las formas tempranas y no favorables de la enfermedad, a través de la aplicación de radioterapia exclusivamente a los sitios afectados y evitar el riesgo de cardiotoxicidad tardía que se observa en las asociaciones con antraciclinas.
 Palabras clave
Enfermedad de Hodgkin, estadio temprano, quimioterapia, terapia radiante, toxicidad tardía
Clasificación en siicsalud
Palabras clave
Enfermedad de Hodgkin, estadio temprano, quimioterapia, terapia radiante, toxicidad tardía
Clasificación en siicsalud
 Artículos originales> Expertos del Mundo>
Artículos originales> Expertos del Mundo>
página www.siicsalud.com/des/expertos.php/76977
Especialidades
 Principal: Hematología,
Principal: Hematología,
 Relacionadas: Medicina Farmacéutica, Medicina Interna, Oncología,
Relacionadas: Medicina Farmacéutica, Medicina Interna, Oncología,
 Enviar correspondencia a:
Enviar correspondencia a:
Prof. Paolo G. Gobbi, Medicina Interna, Oncologia e Gastroenterologia, Università di Pavia, IRCCS Policlinico S. Matteo, P.le Golgi n° 2, 27100 Pavia, Italia
 Patrocinio y reconocimiento
Patrocinio y reconocimiento
Este trabajo fue parcialmente subvencionado por el Ministero dell’Università e della Ricerca Scientifica e Tecnologica, Roma; la Associazione “A. “Serra” y la Fondazione Cassa di Risparmio di Modena, Modena, el IRCCS Policlinico S. Matteo y la “Ferrata-Storti Foundation”, Pavia, ItaliaAgradacemos a la Srta. Deborah Converso por la recolección de datos y a la Dra. Rachel Stenner por la revisión cuidadosa del manuscrito en inglés
EFFECTIVENESS, TOXICITY AND POSSIBLE EVOLUTION OF VBM CHEMOTHERAPY IN EARLY-STAGE HODGKIN’S LYMPHOMA
 Abstract
Abstract
Background: VBM chemotherapy (vinblastine, bleomycin and methotrexate) plus irradiation is an effective therapeutic combination in early-stage Hodgkin’s lymphoma, but conflicting results have been collected on the toxicity of and correct indication for this combination. Patients and methods: The GISL treated 169 evaluable patients with early-stage, favorable presentation Hodgkin’s disease in two successive trials. In the first (MH-1), conducted between 1988-1995, 87 patients were administered the original VBM schedule coupled with extended-field radiotherapy (EF-RT). In the subsequent study (MH-1b), performed between 1996-2004, the doses of vinblastine and methotrexate were intensified, the dose of bleomycin was reduced, and small amounts of prednisone were given contemporaneously with any infusion of antitumoral drug (VbMp); irradiation was delivered to involved sites only and had to begin at least 25 days after the end of chemotherapy. Of the 82 patients treated with the MH-1b protocol, 67 were < 65 years old (MH-1b < 65) and 15 were > 65 years old (MH-1b > 65). Results: Complete remission was achieved by 96, 91 and 80% of the patients in the MH-1, MH-1b < 65 and MH-1b > 65 trials, respectively; relapse rates were 12, 9 and 0%, with median follow-ups of 111, 55 and 49 months. Hematological and pulmonary toxicity were acceptable on the whole in the MH-1 group, but more severe when chemotherapy followed radiotherapy than vice versa. In the MH-1b < 65 both these toxicities were abated, while in the MH-1b > 65 severe infections affected 3/15 patients. Conclusions: VbMp followed by involved-field radiotherapy shows negligible hematological and pulmonary toxicity. The modified protocol appeared as effective as the original VBM + EF-RT protocol, with minimal and not statistically significant differences. The addition of cyclophosphamide to VbMp is under investigation to improve the cell-killing potential of the regimen. The purpose is to cure even early unfavorable presentations of the disease maintaining radiotherapy to involved sites only and avoiding the risk of late cardiotoxicity given by combinations including anthracyclines.
 Key words
Key words
Hodgkin’s disease, early stage, chemotherapy, radiation therapy, late toxicity
EFECTIVIDAD, TOXICIDAD Y PRONOSTICO POTENCIAL DE LA QUIMIOTERAPIA CON VBM EN EL ESTADIO TEMPRANO DEL LINFOMA DE HODGKIN. EXPERIENCIA DEL GRUPPO ITALIANO PER LO STUDIO DEI LINFOMI (GISL)
(especial para SIIC © Derechos reservados)
Artículo completo
Introducción
El mejor tratamiento del estadio temprano del linfoma de Hodgkin (LH) todavía se encuentra en fases de investigación clínica aun cuando con las terapias disponibles se obtienen resultados satisfactorios. De hecho, en la actualidad, aproximadamente el 90% de los pacientes en estadios tempranos de la enfermedad pueden curarse con tratamientos que combinan la quimioterapia de bajo impacto con un régimen de radioterapia del campo afectado (34-40 Gy).1
Hasta hace 20 años, el consenso general era la utilización de la radioterapia de campo extendido con la condición de que la estadificación previa hubiera sido particularmente objetiva y posiblemente basada en la laparotomía exploratoria y esplenectomía. Posteriormente, los estudios que mostraron las desventajas de la estadificación mediante la laparotomía exploratoria, las tasas de recaídas relativamente elevadas luego de la radioterapia y la incidencia constante de tumores sólidos secundarios durante un lapso muy prolongado luego del tratamiento radiante indujeron a los médicos a disminuir el campo de irradiación y combinar la quimioterapia con el fin de contrarrestar, tanto las posibles infiltraciones microscópicas contiguas a las lesiones documentadas como lo inadecuado de una estadificación meramente clínica.
En este contexto, el régimen ABVD (doxorrubicina, bleomicina, vinblastina y metotrexato) se constituyó en el tratamiento de referencia, el cual se administra generalmente a través de un número variable de ciclos de acuerdo con la presentación clínica más o menos favorable, evaluada con la presencia o no de masas palpables, síntomas B, aumento de la tasa de eritrosedimentación, anemia e hipoalbuminemia.
Sin embargo, la utilización de una antracicilina combinada con la irradiación al mediastino –requerida frecuentemente en las presentaciones tempranas del LH– expone a los pacientes a un riesgo, documentado recientemente, de miocardiopatía isquémica tardía y muerte súbita cardíaca.3-5 Si fuera posible limitar o evitar las antraciclinas, reducir el volumen y la dosis de la irradiación –sin perder la efectividad– se prevendría un porcentaje significativo de toxicidades potencialmente letales.
Un enfoque práctico para este problema ha sido la utilización de regímenes quimioterapéuticos con antracicilinas menos cardiotóxicas que la doxurrubincina como la epidoxorrubicina (EBVD, EVE)6,7 o esquemas que no incluyeran ni las primeras ni antracenedionas (VBM, MVP).8,9
El Gruppo Italiano per lo Studio dei Linfoma (GISL) ha adquirido más de 15 años de experiencia con el régimen VBM combinado con radioterapia en los estadios tempranos del LH, desde que llevó exitosamente a cabo dos estudios multicéntricos no aleatorizados: el MH-1,10 desde enero de 1988 a diciembre de 1995, y el MH-1b,11 entre enero de 1996 y diciembre de 2001. Sin embargo, debido a una completa falta de acuerdo entre los miembros del GISL respecto de la política terapéutica a implementar luego de diciembre de 2001, muchos pacientes fueron tratados de acuerdo con el protocolo MH-1b y agrupados conjuntamente en esta actualización.
Pacientes y métodos
Todos los pacientes no tratados tenían diagnóstico de LH probado mediante biopsia, con tipos histológicos diferentes de la esclerosis nodular con depleción linfocitaria o depleción linfocitaria propiamente dicha. Todos habían sido estadificados clínicamente como IA o IIA según los criterios del Cotswolds Meeting,12 no tenían más de tres sitios afectados, una tasa de eritrosedimentación inferior a 40 mm en la primera hora y no presentaban masas palpables. En virtud de la intensificación determinada para dos de las tres drogas del régimen VBM, la inclusión en el ensayo MH-1b se restringió a individuos menores de 65 años y el límite inferior del estado general se fijó en 50 puntos de la escala de Karnofsky. Esta restricción fue anulada para los pacientes tratados luego de diciembre de 2001, debido a la baja toxicidad registrada en el estudio MH-1b. Los pacientes con compromiso infradiafragmático no fueron excluidos.
La estadificación fue clínica y constó –además de los estudios de rutina– de ecografías abdominales, tomografías computadas de tórax y abdomen y una punción biopsia unilateral de la médula ósea. No se realizaron linfoangiografías. Los datos clínicos principales de ambos estudios se presentan en la tabla 1. Todos los procedimientos de estadificación llevados a cabo durante la evaluación inicial se repitieron luego del tratamiento, con excepción de la biopsia de médula ósea. La respuesta clínica fue analizada y clasificada en remisión completa (RC), remisión parcial (RP), sin respuesta (SR) y enfermedad progresiva (EP), según lo recomendado por el Cotswolds Meeting.12
Tabla 1
Ciento dos pacientes fueron incluidos en el estudio MH-1.10 Se excluyeron, por violación de protocolo, tres pacientes mal diagnosticados en el estadio IIIA de la enfermedad; dos, con masas mediastinales; tres, con tipos histológicos diferentes de los requeridos, y uno que previamente había recibido tratamiento. De los 87 pacientes con < 65 años, 43 recibieron radioterapia previa al VBM, 41 se sometieron a la secuencia inversa y tres fueron tratados con 3 ciclos de quimioterapia antes de la irradiación y otros 3 ciclos posteriores a ésta. La mediana de seguimiento alcanza hasta el momento 11 meses (intervalo 15-189). Los resultados preliminares de los primeros 50 pacientes evaluables fueron comunicados en 1996,10 cuando la mediana del seguimiento fue de hasta 38 meses.
Para el final de 2001, 57 pacientes había ingresado al estudio MH-1b.11 Otros 10 individuos de < 65 años recibieron posteriormente este régimen, de manera tal que un total de 67 pacientes pueden ahora ser evaluados en relación con la respuesta clínica y la toxicidad y fueron incluidos en esta actualización, luego de una mediana de seguimiento de 55 meses (intervalo: 8-88). Además de estos 67 pacientes, otros 15 –mayores de 65 años– fueron sometidos al mismo tratamiento que el especificado en el protocolo MH-1b.
Quimioterapia
El régimen basado en VBM se combinó con la radioterapia en los dos protocolos. En el estudio MH-1 se empleó el esquema VBM original asociado con EF-IR, pero los médicos podían escoger la secuencia de quimioterapia y radioterapia para cada paciente. En el MH-1b se utilizó una variante del VBM al incrementar las dosis de vinblastina y metotrexato y reducir la de bleomicina y –en todos los casos– seguida de radioterapia limitada a los campos afectados.
Tanto el esquema VBM original como el modificado (VbMp) se presentan en la tabla 2.
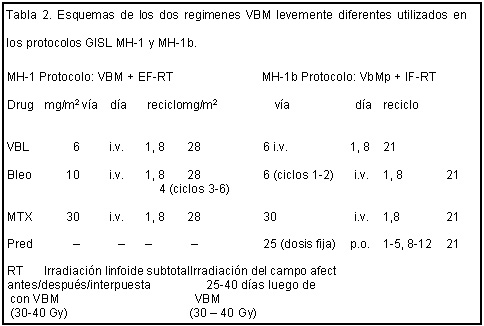
Se calculó la intensidad de dosis para cada droga y para el régimen completo de acuerdo con los criterios comunicados por Hryniuk13 y los ejemplos publicados por DeVita y col.14 De acuerdo con estos cálculos, la intensificación de dosis determinada en el esquema VbMp, en relación con el VBM, fue de 1.22 para la vinblastina, 1.25 para el metotrexato y 0.74 para la bleomicina, con una intensidad de dosis promedio para el régimen completo de 1.07 (pacientes < 65 años).
Radioterapia
La terapia radiante se administró mediante equipos de megavoltaje en diferentes divisiones radioterapéuticas, pero con enfoques distintos en los dos estudios. En el MH-1, el tratamiento consistió en la irradiación linfoide subtotal (STLI) incluidos los campos del manto y pedículo paraaórtico-esplénico en el caso de presentación supradiafragmática e irradiación de campo Y-invertida completa (incluido el bazo) en la enfermedad infradiafragmática. En el estudio MH-1b, solamente se irradiaron los campos afectados. En los dos casos de presentación infradiafragmática observados en el MH-1b, el bazo no estuvo afectado, por lo que no se lo irradió. Los límites de los campos de irradiación fueron prefijados a 5 cm de las áreas que clínicamente se consideraron afectadas. La irradiación mediastinal también incluyó los hilios con márgenes externos de 1-2 cm sobre el tejido pulmonar sano. En ambos estudios, las dosis recomendadas fueron de 36-40 Gy, aunque hubo diferencias inevitables respecto de la fuente, energía, fracción de dosis, dosis total y áreas de los campos entre las distintas instituciones.
Evaluación de la toxicidad
La toxicidad fue medida de acuerdo con los criterios del Eastern Cooperative Oncology Group (ECOG).15 La prueba básica para evaluar y controlar la toxicidad pulmonar potencial de la bleomicina y la radioterapia fue la radiografía simple de tórax. En este sentido, se tomaron como grados progresivos de toxicidad, cuando se asociaron a los síntomas correspondientes: 1) un fino infiltrado reticular en la base de los pulmones; 2) infiltrado intersticial alveolar bibasal; 3) compromiso progresivo del lóbulo inferior y 4) consolidación lobular. Las pruebas de función pulmonar y la determinación de la difusión del monóxido de carbono se llevaron a cabo solamente a demanda, cuando los síntomas respiratorios (principalmente tos o disnea) no se correlacionaron con lesiones irrefutables en las radiografías simples de tórax.
Estadística
Los grados de toxicidad fueron determinados estadísticamente como categorías de observaciones ordenadas según magnitudes crecientes y analizadas mediante la prueba de la U de Mann-Whitney.16 La supervivencia global (SG) se calculó a partir de la fecha del diagnóstico hasta la de la última observación o el óbito. La supervivencia libre de enfermedad (SLE) se midió desde el comienzo del tratamiento hasta la presentación de uno de los siguientes sucesos: progresión de la enfermedad durante el curso del tratamiento, la remisión incompleta al final de éste, recaída o muerte debida a la enfermedad.17 Las respuestas parcial (RP) y nula (SR) fueron consideradas como sucesos ya que a menudo ocultan un componente tumoral resistente o refractario18 y en realidad comparten la mayoría de los requerimientos terapéuticos19 de las recaídas tempranas, las que actualmente se consideran eventos incuestionables para los propósitos estadísticos. Las curvas se calcularon de acuerdo con el método de Kaplan y Meier20 y no fueron excluidas las muertes debidas a causas distintas del linfoma de Hodgkin.
Resultados
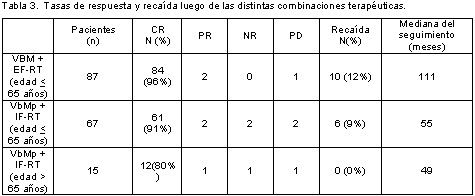
La tabla 3 muestra que la eficacia de la combinación VbMp + IF-RT fue levemente inferior, aunque las diferencias no fueron estadísticamente significativas, que el esquema original VBM + EF-RT. Esto es verdadero en relación con el porcentaje de remisiones completas y recaídas, especialmente si estas últimas se asocian con los seguimientos diferentes de las dos series. VbMp + IF-RT pareció inducir una tasa de remisión más baja en los pacientes ancianos comparados a los más jóvenes, aunque las remisiones obtenidas parecen ser sorprendentemente estables a lo largo del tiempo.
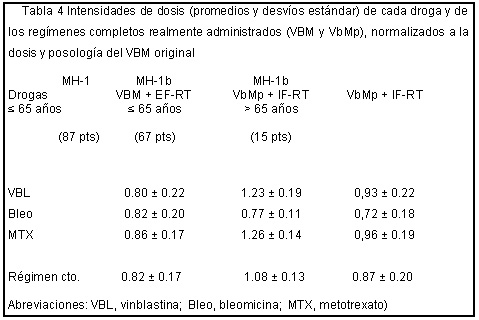
La figura 1 muestra que la supervivencia global de los pacientes tratados con VBM + EF-RT y VbMp + IF-RT no fue estadísticamente diferente, aun cuando la curva de supervivencia del último grupo de pacientes fue bastante menor. Ambas curvas resultaron, según lo esperado, superiores a la de los pacientes mayores, entre los que se incluyeron varias presentaciones con estadios avanzados y síntomas B. Las curvas de la supervivencia libre de enfermedad (figura 2) se disponen más cercanas que las de la supervivencia global, excepto la curva de los pacientes ancianos. La tabla 4 muestra los datos referidos al promedio de la intensidad de dosis real de cada droga administrada y de todo el régimen. Se obtuvieron la intensificación planeada para vinblastina y metotrexato y la disminución de la intensidad de bleomicina, las cuales fueron significativas. Esto también se demostró por la intensidad de dosis elevada de vinblastina, metrotexato y de todo el régimen VbMp que recibieron los pacientes ancianos, en comparación al esquema VBM original en los más jóvenes. Esta diferencia en la intensidad de dosis de los fármacos pueden ser considerado un buen control cruzado de la toxicidad aguda registrada. La tabla 5 muestra la toxicidad hematológica, la cual es el principal determinante del tamaño de dosis e intervalos de administración de la droga.
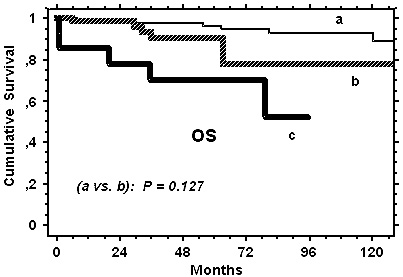
Figura 1. Supervivencia global (OS) de los 87 pacientes < 65 años tratados con VBM + EF-RT (curva a) y de los 82 pacientes tratados con VbMp + IF-RT: 67 de estos pacientes (curva b) tenían edades comparables al grupo de la curva a, mientras que 15 (curva c) tenían más de 65 años y también presentaron estadios avanzados.
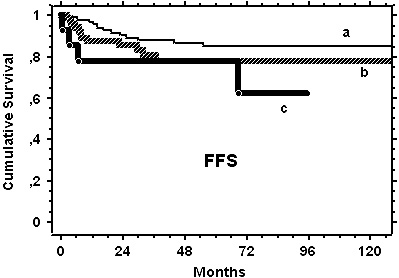
Figura 2. Supervivencia libre de enfermedad (FFS) de los 87 pacientes < 65 años tratados con VBM + EF-RT (curva a) y de los 82 tratados con VbMp + IF-RT: 67 de estos pacientes (curva b) tenían edades comparables con el grupo de la curva a, mientras que los 15 restantes (curva c) eran mayores de 65 años.
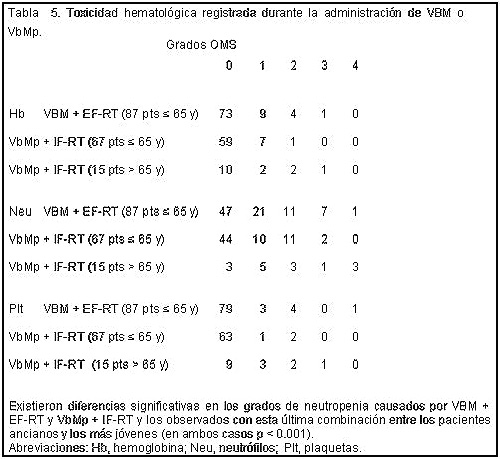
En los pacientes < 65 años no hubo diferencias significativas respecto del grado de anemia, neutropenia y trombocitopenia, mientras que la toxicidad fue manifiesta en los pacientes ancianos. De hecho, se registraron 3 muertes por sepsis en el grupo de 15 ancianos.
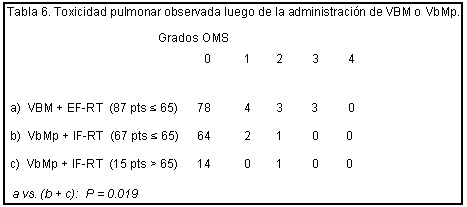
Como se muestra en la tabla 6, hubo menos toxicidad pulmonar en el grupo tratado con VbMp + IF-RT, tanto en jóvenes como ancianos, quizá como consecuencia de un intervalo mayor entre la quimioterapia y la radioterapia y el empleo de dosis acumulativas menores de bleomicina.
Discusión
La quimioterapia VBM fue diseñada por investigadores de la Universidad de Stanford8 como un régimen con toxicidad a largo plazo para evaluar la posibilidad de disminuir la extensión de la radioterapia combinada en los pacientes laparotomizados. Los resultados preliminares fueron prometedores y el British National Lymphoma Investigation evaluó el régimen VBM asociado a la IF-RT en dos estudios con pacientes estadificados clínicamente.9,21 Las conclusiones de estos estudios fueron que la VBM es un régimen efectivo en las fases tempranas del linfoma de Hodgkin, aunque, si bien la toxicidad registrada en el primer estudio había sido aceptable (principalmente pulmonar), la observada posteriormente (pulmonar y hematológica) fue considerada grave e intolerable.
El GISL evaluó la efectividad y toxicidad de la asociación entre la VBM y la irradiación en dos pasos consecutivos. En un principio,10 el esquema original –no modificado– de VBM fue combinado con la EF-RT en pacientes estadificados clínicamente para contrarrestar la inexactitud forzosa de la estadificación del estadio clínico no quirúrgica. Este tratamiento demostró ser efectivo a pesar de un leve aumento de las toxicidades hematológica y pulmonar, especialmente cuando la irradiación precedió a la quimioterapia y no a la inversa. En el estudio posterior,11 el GISL mantuvo la secuencia terapéutica que probó ser menos tóxica –radioterapia luego de quimioterapia– e instrumentó las siguientes modificaciones: reducción de la dosis de bleomicina luego del segundo ciclo, disminución de los campos irradiados (IF-RT) y leve aumento del intervalo entre la quimioterapia y la radioterapia con el fin de minimizar la toxicidad pulmonar e incrementar la intensidad de dosis de la vinblastina y metotrexato para contrarrestar la disminución de la bleomicina y la radioterapia.
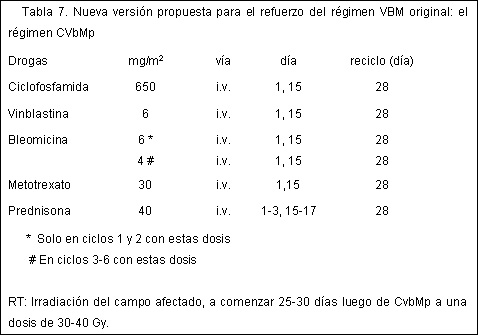
Disminuyeron las toxicidades hematológica y pulmonar y los resultados clínicos no fueron estadísticamente diferentes de los obtenidos en el estudio precedente. Esto, en el contexto general, fue un resultado de suma importancia, ya que en los estudios simultáneos realizados en Stanford22 y Gran Bretaña,9 los cuales interpusieron la radioterapia entre dos cursos de VBM (“sandwich”), mostraron la persistencia de una marcada toxicidad pulmonar, lo cual impidió a los médicos la utilización rutinaria de este tratamiento en la práctica clínica. Sin embargo, paralelamente al control adecuado de la toxicidad pulmonar, en el segundo estudio del GISL se observó una tasa de remisión levemente inferior y una tasa de recaídas ligeramente elevada (aunque las diferencias fueron estadísticamente no significativas), las cuales fueron adjudicadas a un aumento insuficiente de la intensidad de dosis promedio del régimen completo y a la inexactitud de la estadificación clínica. Estos resultados son manifiestos incluso en la actualidad, luego de 2 años más de seguimiento y tras haber incluido otros 17 pacientes respecto del último análisis, con lo que el GISL ha comenzado a mejorar la efectividad del VBM al mismo tiempo que se mantiene el control adecuado de la toxicidad pulmonar y se restringe la irradiación a los sitios afectados, solamente sobre la base de una estadificación inicial exclusivamente clínica. Se decidió mejorar el potencial citodestructor e implementar un estudio piloto que evaluará los resultados y efectos colaterales de una versión ulterior modificada del régimen VBM. Las modificaciones consistieron en el agregado de ciclofosfamida y el refuerzo de la actividad antitumoral del régimen completo, además de poder escoger un esquema de administración bisemanal de las cuatro drogas con el fin de distribuir mejor los intervalos entre las infusiones, en virtud del agregado de ciclofosfamida. Las dosis de los fármacos y los tiempos de administración del nuevo esquema se muestran en la tabla 7. Los primeros seis pacientes tratados con este régimen obtuvieron la remisión completa sin presentar toxicidad hematológica o pulmonar, aunque se pretende que el estudio piloto se complete luego de tratar 20 pacientes sucesivos. Se espera que el nuevo régimen se pueda asociar de manera segura a la irradiación del mediastino, al no haber antraciclinas y medidas que permitan disminuir los efectos colaterales pulmonares, que sea tan efectivo y posiblemente menos cardiotóxico que el régimen ABVB y reemplazar a éste cuando se lo utilice asociado a la radioterapia en pacientes en etapas tempranas (o “intermedias”) desfavorables de la enfermedad de Hodgkin.
En relación con los ancianos, la asociación terapéutica entre el VBM y la irradiación ya había mostrado ser efectiva en el estudio de Zinzani y col.33 Estos investigadores trataron 19 pacientes con una edad promedio de 68 años (intervalo: 60-75), muchos de los cuales estaban en fases avanzadas de la enfermedad, y se registraron 15 respuestas completas y 3 parciales. Solamente en un paciente no se observó respuesta. La toxicidad fue insignificante. Cinco pacientes murieron por la enfermedad, pero en el contexto general los resultados fueron considerados como aceptables en el subgrupo de pacientes ancianos. Nuestros resultados con VbMp + IF-RT en 15 individuos mayores (media: 74 años; intervalo: 68-77) en todos los estadios de la enfermedad son congruentes con los de Zinzani y col. Básicamente, no se observó toxicidad y solamente preocuparon 3 muertes debidas a infecciones graves. Por este motivo, el GISL decidió que los pacientes ancianos deben ser excluidos de aquí en más de los estudios de intensificación de esta combinación terapéutica.
Los autores no manifiestan “conflictos de interés”.
 Bibliografía del artículo
Bibliografía del artículo
- Dihel V, Stein H, Hammel M, Zollinger R, Connors JM. Hodgkin’s lymphoma: biology, and treatment strategies for primary, refractory and relapsed disease. Hematology 2003 (Am Soc Hematol Educ Program): 225-47.
- Aisenberg AC. Problems in Hodgkin’s disease management. Blood. 1999; 93:761-779.
- Glanzman C, Kaufmann P, Jenni R, Hess OM, Huguenin P. Cardiac risk after mediastinal irradiation for Hodgkin’s disease. Radiother Oncol 1998; 46:51-62.
- Enrici RM, Anselmo AP, Donato V et al. Relapse and late complications in early-stage Hodgkin’s disease patients with mediastinal involvement treated with radiotherapy alone or plus one cycle of ABVD. Haematologica 1999; 84:917-23.
- Brusamolino E, Lunghi F, Orlandi E et al. Treatment of early-stage Hodgkin’s disease with four cycles of ABVD followed by adjuvant radiotherapy: analysis of efficacy and long-term toxicity. Haematologica 2000; 85:1032-9.
- Nordijk E, Carde P , Mandard AM et al. Preliminary results of the EORTC-GPMC controlled clinical trial H7 in early stage Hodgkin's disease. EORTC Lymphoma Cooperative Group. Group Pierre-et-Marie-Curie. Ann Oncol. 1994; 5 (Suppl. 2):523-9.
- Pavone V, Gobbi PG, Adamo F et al. Preliminary results of the Italian Lymphoma Intergroup randomized study ABVD versus EVE in unfavorable stage I A and II A Hodgkin's disease. Haematologica 2001; 86 (Suppl. to n 10):107.
- Horning SJ, Hoppe RT, Hancock SL et al. Vinblastine, bleomycin, and methotrexate: an effective adjuvant chemotherapy in favorable Hodgkin’s disease. J Clin Oncol. 1988; 6:1822-31.
- Moody AM, Pratt J, Vaughan Hudson G et al. British National Lymphoma Investigation: pilot studies of neoadjuvant chemotherapy in clinical stage IA and IIA Hodgkin’s disease. Clin Oncol. 2001; 13:262-8.
- Gobbi PG, Pieresca C, Frassoldati A et al. Vinblastine, bleomycin, and methotrexate chemotherapy plus extended-field radiotherapy in early, favorably presenting, clinically staged Hodgkin’s patients: the Gruppo Italiano per lo Studio dei Linfomi experience. J Clin Oncol. 1996; 14:527-533.
- Gobbi PG, Broglia C, Merli F et al. Vinblastine, bleomycin and methotrexate chemotherapy plus irradiation for early-stage, favorable Hodgkin’s lymphoma. The experience of the Gruppo Italiano Studio Linfomi (GISL). Cancer 2003: 98:2393-401.
- Lister TA, Crowther D, Sutcliff SB et al. Report of a committee convened to discuss the evaluation and staging of patients with Hodgkin's disease. J Clin Oncol. 1989; 7:1630-6.
- Hryniuk WM. Average relative dose intensity and the impact on design of clinical trials. Semin Oncol. 1987; 14:65-74.
- DeVita VT Jr, Hubbard SM, Longo DL. The chemotherapy of lymphoma: looking back, moving forward – The Richard and Hinda Rosenthal Foundation Award Lecture. Cancer Res. 1987; 47:5810-24.
- Oken MM, Creech RH, Tormey DC et al. Toxicity and response criteria of the Eastern Cooperative Oncology Group. Am J Clin Oncol. 1982; 5:129-37.
- Armitage P, Berry G. Statistical methods in medical research (ed 2). Oxford, United Kingdom: Blackwell Scientific, 1987:296-357.
- Dixon DO, McLauglin P, Hagemeister FB et al. Reporting outcomes in Hodgkin's disease and lymphoma. J Clin Oncol. 1987; 5:1670-2.
- Carde P. Should poor risk patients with Hodgkin's disease be sorted out for intensive treatments Leuk Lymphoma. 1995; 15:31-40.
- Longo DL, Duffey PL, Young RC et al. Conventional-dose salvage combination chemotherapy in patients relapsing with Hodgkin's disease after combination chemotherapy: the low probability for cure. J Clin Oncol. 1992; 10:210-8.
- Kaplan EL, Meier P. Nonparametric estimation from incomplete observation. J Am Stat Assoc. 1958; 53:457-81.
- Bates NP, Williams MV, Bessell EM et al. Efficacy and toxicity of vinblastine, bleomycin, and methotrexate with involved-field radiotherapy in clinical stage IA and IIA Hodgkin’s disease: a British National Lymphoma Investigation pilot study. J Clin Oncol. 1994; 12:288-96.
- Horning SJ, Hoppe RT, Mason J et al. Stanford - Kaiser Permanente G1 study for clinical stage I to IIA Hodgkin’s disease: subtotal lymphoid irradiation versus vinblastine, methotrexate and bleomycin chemotherapy and regional irradiation. J Clin Oncol. 1997; 15:1736-44.
- Zinzani PL, Magagnoli M, Bendandi M et al. Efficacy of the VBM regimen in the treatment of elderly patients with Hodgkin’s disease. Haematologica. 2000; 85:729-32.
©
Está
expresamente prohibida la redistribución y la redifusión de todo o parte de los
contenidos de la Sociedad Iberoamericana de Información Científica (SIIC) S.A. sin
previo y expreso consentimiento de SIIC





 Artículos originales> Expertos del Mundo>
Artículos originales> Expertos del Mundo> Enviar correspondencia a:
Enviar correspondencia a: Patrocinio y reconocimiento
Patrocinio y reconocimiento







