|
Antecedentes
Pese a los avances registrados en la terapia médica y al desarrollo de técnicas de acceso mínimo para la ablación endometrial, el papel de la histerectomía no ha disminuido significativamente en el Reino Unido. En efecto, durante 1998 se llevaron a cabo 62 775 histerectomías en Inglaterra y Gales,1 y la cifra es aun mayor en EE.UU.: 645 000.2 El número de histerectomías abdominales sobrepasa actualmente al de las vaginales, en el Reino Unido, en una proporción de 4:1 para el tratamiento de las enfermedades benignas; esta relación es similar en EE.UU. y otros países europeos.3,4 La vía vaginal queda relegada principalmente al tratamiento del prolapso.4
Las pacientes sometidas a histerectomía por vía vaginal muestran menos dolor posoperatorio, menos complicaciones perioperatorias, recuperación más rápida y reinserción laboral más temprana que las intervenidas por vía abdominal.5,6 El costo de la histerectomía vaginal es también menor que el de la abdominal o la realizada con asistencia laparoscópica; así, su utilización se traduce en significativos ahorros.5 Pese a las recomendaciones para el empleo de este abordaje6,7 y las sugerencias del Real Colegio de Obstetras y Ginecólogos de auditar las indicaciones de histerectomía para establecer la tasa óptima de histerectomías vaginales,8 no han ocurrido hasta ahora cambios en la práctica cotidiana. De hecho, las guías publicadas con el fin de determinar la vía de la histerectomía más adecuada sólo han tenido efectos limitados.7,10
Las posibles explicaciones de la falta de progreso en este tema abarcan las preferencias del cirujano, la falta de descenso uterino y la necesidad de más entrenamiento en cirugía vaginal.6,10 La histerectomía vaginal (para el prolapso) forma parte del repertorio de cualquier ginecólogo entrenado en el mundo.
Este estudio investiga una estrategia para cambiar la práctica diaria, y detalla los resultados logrados cuando un ginecólogo promedio, sin entrenamiento extra, toma la decisión deliberada de realizar todas las histerectomías por vía vaginal, siempre que ello sea posible.
Métodos
El estudio incluyó todas las histerectomías por patologías benignas (excepto prolapso) llevadas a cabo o asistidas por el autor desde enero de 1994 hasta diciembre de 1998. Fueron excluidas del protocolo las pacientes con neoplasias ginecológicas, enfermedades anexiales o tuboováricas, evidencia de endometriosis extensa con morbilidad uterina asociada, enfermedad fuera de la pelvis que requiriese exploración abdominal o un tamaño uterino mayor que el de un embarazo de 16 semanas.
Se llevó registro de la edad, paridad, peso, antecedentes quirúrgicos de cada paciente, así como de las indicaciones de histerectomía, necesidad de ooforectomía y disminución de los niveles de hemoglobina. Las operaciones fueron calificadas como de complejidad alta (cuando obligó intraoperatoriamente a cambiar la vía) o de complejidad normal. Las complicaciones fueron clasificadas de la siguiente manera: (1) intraoperatorias, (2) inmediatas posoperatorias (ocurridas dentro de las seis semanas), y (3) posoperatorias tardías (acaecidas luego de seis semanas). Se definió como hipertermia posoperatoria a la temperatura superior a 38 °C en dos o más ocasiones, excluyendo las primeras 24 horas posteriores a la operación.
Resultados
En total fueron evaluadas 272 histerectomías de entre las 553 llevadas a cabo en el período de cinco años. Se excluyeron 187 histerectomías vaginales por prolapso uterovaginal y 31 histerectomías abdominales por endometriosis extensa y/o miomatosis uterina (tamaño uterino mayor que el de una gestación de 16 semanas).
Las restantes 63 histerectomías fueron efectuadas por
patologías malignas. Las indicaciones para efectuar la
operación en los dos grupos están detalladas en la tabla 1.
En estas series, 201 de 273 histerectomías (74%) fueron
indicadas por la misma forma de disfunción menstrual en
ausencia de patología pélvica mayor

En
total, 97 histerectomías fueron abdominales y 175 vaginales.
No hubo diferencias significativas entre los dos grupos en
cuanto a las características de las pacientes (tabla 2),
incluyendo específicamente la incidencia de nuliparidad y cesáreas
anteriores. La incidencia de complicaciones fue baja, con
valores similares en ambos grupos (tabla 2).

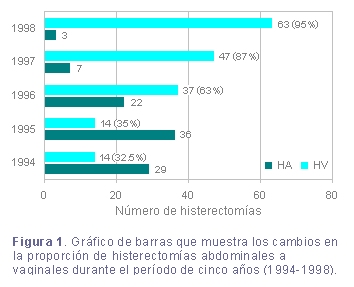
La
figura 1 muestra la distribución de las histerectomías
abdominales y vaginales realizadas por año desde 1994 hasta
1998. La proporción de histerectomías vaginales aumentó
gradualmente desde 32% en 1994 hasta 95% en 1998.
También
se observó incremento gradual de remociones vaginales ováricas,
desde ninguna en el primer año del estudio hasta 83% de las
ooforectomías realizadas en el último año (tabla 3).

Con
el abordaje vaginal ocurrieron sólo dos casos de fracaso
durante el período evaluado; en ellos fue necesario, durante
la operación, cambiar la vía vaginal planeada por la
abdominal. El primer caso ocurrió en el tercer año del
estudio; existía dificultad para el acceso por la presencia
de un arco subpubiano estrecho y una significativa
endometriosis útero-sacra y en el saco de Douglas. Esta fue
mucho mejor evaluada bajo visión directa por vía abdominal,
que aseguró la correcta identificación ureteral y permitió
obtener una hemostasia completa. El segundo fracaso ocurrió
en el cuarto año; se observó incidentalmente en la paciente
en cuestión un carcinoma ovárico avanzado con ovarios de
tamaño normal y compromiso del saco de Douglas. Esta situación
no fue detectada clínicamente antes de la operación, y
constituye un evento clínico raro.
Discusión
Viabilidad. El estudio demuestra que la vía vaginal para la histerectomía es posible en la mayoría de los casos. Todas las mujeres que requieren histerectomía por problemas menstruales con útero normal o de tamaño moderadamente aumentado podrían acceder a cirugía por vía vaginal mediante un adecuado asesoramiento. Estas pacientes son mayoritarias en nuestra práctica, y creemos que también en todo el mundo. Tal cambio de práctica no requiere que el cirujano lidie con casos dificultosos, representados por grandes úteros o necesidad de ooforectomías vaginales. Y con el incremento de la experiencia, los demás beneficios de la estrategia se harán evidentes.
Hasta el momento, la vía de la histerectomía es generalmente asumida como abdominal o determinada mediante examen pelviano bimanual en la consulta ambulatoria. Tal examen conlleva gran variación interobservador e intraobservador, y parece un elemento débil para definir la viabilidad de la histerectomía vaginal. Sin embargo, cuando esta evaluación es efectuada en la sala de operaciones, el panorama es más favorable de lo que la mayoría de los ginecólogos podrían anticipar. Este cambio en la práctica y en las actitudes promovido por Seth7 condujo a la experiencia aquí señalada.
Motivos comúnmente invocados para desestimar la realización de histerectomía vaginal
Falta de prolapso. Existen muchos datos disponibles acerca de la viabilidad de la remoción de úteros no prolapsados por vía vaginal.7,11 Nuestra propia experiencia indica que la distancia promedio del cérvix hasta el introito luego de la tracción es de 2.5 cm en la mayoría de las pacientes que no presentan síntomas de prolapso. Aún en el caso de cérvix más grande en vagina, la división del complejo de ligamentos cardinales uterosacros logra significativo descenso cervical en la mayoría de las pacientes, con la consiguiente fácil remoción vaginal del útero. En verdad, siempre pudimos ligar dicho complejo, incluso en el pequeño número de fracasos en cuanto a la realización de una histerectomía vaginal tal como había sido planeada.
Utero grande. La intención de este estudio no fue aspirar a la remoción de grandes úteros, aunque ello ocurrió a medida que aumentaba nuestra experiencia y confianza. Recomendamos el empleo de análogos LHRH para reducir preoperatoriamente el tamaño uterino y el de los miomas. Con este recurso fue posible remover por vía vaginal, después de la reducción, úteros más voluminosos que un embarazo de 18 semanas.3 Con respecto a la extracción de grandes úteros, preferimos la técnica de enucleación y miomectomía a la de bisección uterina. Cuando se encuentran dificultades, ello no obedece usualmente al tamaño uterino sino a la posición de los miomas. Los miomas bajos posteriores y los bajos anteriores subserosos de más de 6-7 cm son los más problemáticos en comparación con los intramurales, superiores o fúndicos, los cuales son habitualmente muy fáciles de remover.
Cesáreas o cirugías pelvianas anteriores. Las cesáreas y las cirugías pelvianas anteriores no constituyeron problema alguno, excepto en un caso que presentaba densas adherencias entre el fondo uterino y la pared abdominal anterior. No consideramos esta situación como contraindicación, y efectuamos histerectomías vaginales en forma rutinaria a pacientes con 2-4 cesáreas previas. En nuestra experiencia, la disección de la vejiga es mucho más fácil por vía vaginal luego de una cesárea previa que por histerectomía abdominal. Otras cirugías pelvianas raramente influyeron en la remoción vaginal del útero.
Necesidad de ooforectomía. En EE.UU., al 50% de todas las mujeres sometidas a histerectomía se les efectúa conjuntamente ooforectomía bilateral.20 El aumento del número de ooforectomías vaginales fue un hecho tardío en el estudio; a medida que nuestra experiencia y confianza aumentaban, este cambio ocurrió en forma automática. Ello no constituye un prerrequisito para el cambio en la práctica médica descripto aquí. La frecuencia de ooforectomía vaginal aumentó rápidamente desde cero hasta un 82% hacia el final del período de cinco años. En mujeres premenopáusicas, la remoción ovárica por vía vaginal es usualmente simple de efectuar y no requiere instrumento especial alguno. Pero en aquellas que hayan transitado algunos años de la posmenopausia, el ligamento infundíbulo-pélvico se halla muchas veces significativamente acortado, y por ello es difícil de alcanzar. En estas pacientes, la utilización de un laparoscopio para seccionar los ligamentos infundíbulo-pélvicos puede ser de utilidad. El estudio demuestra claramente que la práctica adicional de ooforectomías no necesita la vía abdominal o de asistencia laparoscópica en la mayoría de los casos.
Nuliparidad. En nuestra experiencia, ha sido sorprendentemente fácil remover los úteros nulíparos; esto podría obedecer al menor tamaño de úteros y cérvices. En estas pacientes se observa a menudo descenso cervical, con cérvices que llegan a 1-3 cm del introito al aplicárseles tracción.
Papel de la laparoscopia
Los defensores de las posiciones más extremas promueven la histerectomía vaginal con asistencia laparoscópica como técnica para convertir la histerectomía abdominal en vaginal.19 Ello requiere alto grado de habilidad laparoscópica, equipos costosos y mayor tiempo quirúrgico. El enfoque aquí recomendado no posee ninguna de esas desventajas. Nuestro estudio demuestra claramente que el laparoscopio no es esencial para facilitar la histerectomía vaginal y que sólo debería ser usado en un pequeño número de pacientes adecuadamente seleccionadas, con sospecha diagnóstica de patologías coexistentes. Nosotros lo utilizamos sólo en un puñado de pacientes durante el período del estudio. El motivo más frecuente para realizar una laparoscopia fue la verificación de la hemostasia luego de un procedimiento dificultoso. En dos de esas ocasiones utilizamos diatermia bipolar para efectuar la hemostasia. Una de estas laparoscopias tuvo lugar 4 horas después de concluida la operación, ya que se observaba mucho fluido en el drenaje, y logró suprimir completamente el sangrado.
Cuándo esperar dificultades
La obesidad hace muy difícil remover el útero por vía vaginal. Aún cuando es lógico evitar la realización de procedimientos abdominales en pacientes muy obesas que presentan riesgo de complicaciones posoperatorias, estas mismas mujeres constituyen el grupo en las cuales la histerectomía vaginal podría ser extremadamente dificultosa. La obesidad, en nuestra opinión, reduce la accesibilidad al útero; además, recomendaríamos la ayuda de asistentes experimentados cuando se intenta efectuar histerectomía vaginal en este grupo de pacientes, ya que la necesidad de retracción es mucho mayor que en caso de índice de masa corporal normal.
Nuestro enfoque
Nuestro enfoque fue extremadamente cauto pero con la mente abierta, y se orientó principalmente a adoptar la decisión sobre la vía de remoción en el quirófano, bajo anestesia; la paciente había sido apropiadamente aconsejada. La decisión de realizar la histerectomía por vía vaginal, en nuestra opinión, puede sólo ser tomada luego de iniciado el procedimiento e inmediatamente después de pinzar el complejo de los ligamentos cardinales uterosacros.
Hemos hallado con frecuencia que, luego de comenzar el procedimiento, percibimos que éste iba a ser muy dificultoso, sólo para darnos cuenta posteriormente que era muy simple tras pinzar el complejo de ligamentos cardinales uterosacros. La ausencia de complicaciones demuestra que este enfoque es razonablemente seguro. Más importante aún fue la falta de complicaciones durante la fase inicial del estudio (la curva de aprendizaje, que explica las altas tasas de complicaciones cuando se introducen nuevas técnicas).
¿Cómo podría cambiarse de una vía vaginal planeada a un abordaje abdominal, de un modo seguro y expeditivo? La seguridad de la paciente demanda que, cuando la situación que favorece el cambio está presente durante la operación, debería ser prontamente reconocida sin experimentar sensación de fracaso. Nuestra recomendación es que, ante una dificultad aparente para el abordaje vaginal que obstaculiza el progreso (esto es usualmente evidente para todos en el quirófano), el cirujano solicite a la enfermera circulante que tome nota del tiempo. Así, se podría dejar transcurrir un máximo de 10-15 minutos más antes de abrir el abdomen. Nosotros hemos utilizado a menudo esta técnica en la práctica diaria, y aun luego de finalizar el estudio; sin embargo, la necesidad de cambiar a una vía abdominal surgió sólo en una ocasión en los últimos cinco años.
Cómo lograr este cambio en la práctica
Recomendamos los siguientes pasos simples a aquellos que consideren cambiar la vía de la histerectomía. El cambio, desde la óptica de nuestra experiencia, es
más bien rápido y sorprendente.
- tomar la decisión de realizar todas las histerectomías potomar la decisión de realizar todas las histerectomías por vía vaginal.
- auditar las propias tasas de histerectomía vaginal previas a la decisión en los últimos seis meses.
- elegir inicialmente mujeres que han tenido hijos, con índice de masa corporal y tamaño uterino normales.
- aconsejar a las pacientes teniendo en cuenta el pequeño riesgo de los procedimientos abdominales.
- llevar a cabo las primeras diez histerectomías en pacientes cuidadosamente seleccionadas antes de intentarlo con mujeres con úteros grandes, con cesáreas previas o en primíparas.
Conclusiones
Hay muchos datos acerca de la superioridad de la vía vaginal para la histerectomía.5-7,9,11,12-20 Los costos son menores al hacerse más breve la estadía hospitalaria;6,10,16,18 y como la histerectomía es la operación ginecológica más común, cualquier ahorro en su práctica ejercerá efectos importantes sobre el costo de las cirugías ginecológicas a nivel mundial. La internación más breve es también un resultado deseable desde la perspectiva de la paciente. No se realizó un análisis de costo-beneficio para medir la influencia de la duración de la internación y del retorno laboral; sin embargo, las pacientes en quienes se practicó histerectomía vaginal refieren que retoman sus actividades normales mucho más rápidamente, y presentan superior calidad de vida que las sometidas a histerectomía abdominal o asistida laparoscópicamente.17
No hay un estudio de la literatura que haya indagado acerca del cambio de la práctica de la histerectomía en un período de tiempo. La estrategia propuesta es simple, y puede ser aplicada muy fácilmente por cualquier ginecólogo en ejercicio en cualquier parte del mundo; el cambio puede ser muy rápido, tal como lo observamos nosotros, para nuestra sorpresa. El récord de seguridad que hemos demostrado y el éxito práctico de este enfoque debe alentar a todos los departamentos de ginecología a prepararse para investigar este cambio de política. Además, los que no optan por el cambio deberían dar sus razones a pacientes y profesionales de la salud. Más importante aún, deberían analizar sus prácticas para determinar los resultados y el impacto, tanto sobre la calidad de vida de la paciente como sobre los costos hospitalarios, de las histerectomías en sus propias instituciones.
Técnica
El tiempo promedio necesario para realizar la histerectomía vaginal en estas pacientes es de 15-20 minutos, y todos nuestros residentes deberían lograrlo al finalizar sus doce meses de rotación en el equipo. Las pacientes reciben antibióticos profilácticos durante la inducción anestésica y se les permite comer y beber cuando regresan a la sala de recuperación. El tiempo para el alta es decidido según la necesidad de analgesia; la duración promedio de la internación es de 2.5 días (rango 1-5 días).
La mayoría de los procedimientos son efectuados bajo anestesia general; la analgesia espinal es utilizada cuando se considera inadecuada la anestesia general. Se coloca a la paciente en posición de litotomía y luego se la examina para evaluar la movilidad y tamaño uterinos, así como la presencia de masas tuboováricas. No se efectúa cateterización de rutina para vaciar la vejiga.
Se infiltra utilizando 10 ml de marcaína con adrenalina (1 en 200 000). Se realiza una incisión alrededor del cérvix que involucra el espesor total del epitelio vaginal, excepto lateralmente, donde es superficial. Posteriormente, la incisión es efectuada 1-2 cm más alta. Esto contribuye a ingresar más fácilmente al fondo de saco de Douglas; el epitelio vaginal es luego empujado utilizando una gasa montada sobre el dedo. El peritoneo del fondo de saco de Douglas es generalmente visible en este punto, y es incidido utilizando tijeras de McIndoe. La entrada exitosa en el fondo de saco de Douglas se acompaña habitualmente de la salida de una pequeña cantidad de líquido peritoneal. El epitelio vaginal anterior es sostenido con una pinza de disección con dientecillos, y se efectúa la separación de la vejiga utilizando tijeras inicialmente, y luego en forma roma. La vejiga debe ser rebatida mediante un retractor de pared vaginal anterior de Wertheim; en este punto, el peritoneo es visible, pero no incidido.
Se coloca una pinza angulada durante todo el procedimiento; la primera pinza es colocada generalmente en el complejo de ligamentos cardinales uterosacros izquierdo, y se intenta incluir la totalidad. Este es posteriormente ligado utilizando una sutura de Vicryl® 20 montada en una aguja curva de 5/8 (este tipo de sutura se emplea a lo largo de todo el procedimiento). Se cortan todas las suturas con un cabo de 2-3 cm de longitud, y se dejan libres; los pedículos son pinzados y cortados uno a continuación del otro, para evitar el uso simultáneo excesivo de pinzas.
Luego de atar el complejo de ligamentos cardinales uterosacros, los vasos uterinos son pinzados y ligados (se intenta incluir la totalidad del pedículo vascular en una pinza). Las suturas son cortadas a longitudes similares a las del primer pedículo; en este punto, la punta de la pinza ingresa usualmente en el peritoneo anterior. Si el peritoneo no es fácilmente visible en este punto, se procede a su apertura.
Los pedículos de los ligamentos anchos son pinzados, cortados y ligados. Como estos pedículos son a veces largos, acostumbramos a efectuarles diatermia luego de atados. Se tiene cuidado a lo largo de todo procedimiento de evitar dejar vasos entre los pedículos.
En este punto, si se observa algún sangrado, habitualmente es debido a los vasos de las paredes vaginales; todos los pedículos son inspeccionados cuidadosamente antes de cerrar la cúpula vaginal. Esta última es cerrada utilizando sutura continua, comenzando desde atrás y progresando hacia adelante. No se efectúa cierre peritoneal, y las suturas de la cúpula son colocadas cuidadosamente, incluyendo el peritoneo posterior, con el fin de cerrar cualquier espacio existente entre la pared vaginal y el peritoneo. Se incluye el espesor total del epitelio vaginal en las suturas, y se deja un drenaje redivac en la pelvis a través de la cúpula (los puntos de sutura son colocadas cuidadosamente a su alrededor para procurar no incluirlo en un punto).
Se coloca de rutina una sonda de Foley en la vejiga durante 24 horas, y tanto el catéter como el drenaje son removidos a la mañana siguiente. La cantidad promedio de líquido drenado es de alrededor de 70 ml (rango,10-300 ml). El seguimiento se efectúa mediante un control posoperatorio, generalmente cuatro semanas después del alta. Nosotros dictamos cursos para enseñar nuestra técnica a otros cirujanos, y hemos editado un vídeo que la ejemplifica.
Copyright © SIIC 2003.
Dr. Rajiv Varma
Bibliografía
- Royal
College of Obstetrics & Gynaecology Data 1999
- Inpatient
discharges from non-Federal hospitals, United States,
1998. National Centre for Health Statistics, US Department
of Health and Human Services; 2001
- Davies
A, Vizza E, Bournas N, OConnor H, Magos A. How to
increase the proportion of hysterectomies performed
vaginally. Am J Obstet Gynecol 1998; 179(4): 1008-12.
- Mulholland
C, Harding N, Bradley S, Stevenson M. Regional variation
in the utilisation rate of vaginal and abdominal
hysterectomies in the United Kingdom. Journal of Public
Health Medicine 1996; 18:400-5..
- Dorsey
JH, Holtz PM, Griffiths RI, McGrath MM and Steinberg EP.
Cost and changes associated with three alternative
techniques of hysterectomy. N Engl J Med 1996;335: 476-82
- Kovac
SR, Christie SJ, Bindbeutel GA. Abdominal versus vaginal
hysterectomy, a statistical model for determining
physicians decision making and patient outcome. Med
Decis Making 1991; 11: 19-28
- Sheth
SS. Vaginal hysterectomy. In: Studd J, ed. Progress in
Obstetrics & Gynecology 1993; 10: 317-339. Edinburgh,
Churchill Livingstone
- RCOG
Effective procedures in gynaecology suitable for audit
Royal College of Obstetricians and Gynaecologists London
1998.
- Van
den Eeden SK, Glasser M, Mathias SD, Colwell HH, Pasta DJ,
Kunz K. Quality of life, healthcare utilisation and costs
among women undergoing hysterectomy in a managed care
setting. Am J Obstet Gynecol 1998; 178: 91-100.
- Kovac
SR. Guidelines to determine the route of hysterectomy.
Obstet Gynecol 1995; 85:18-23
- Unger
J B, Vaginal removal of the Benign Non prolapsed uterus:
Experience with 300 consecutive operations. Am J Obstet
Gynecol 1999; 180(6): 1337-44.
- Pratt
JH, Daikoku NH. Obesity and vaginal hysterectomy. J Reprod
Med 1990; 35: 945-944.
- Gitch
G, Berger E, Tatra G. Trends in thirty years of vaginal
hysterectomy. Surg Gynecol obstet 1991; 172:207-210.
- Carlson
KJ. Outcomes of Hysterectomy. Clinical Obstet Gynecol
1997; 40: 939- 49
- Nezhat
C, Bess O, Admon D, Nezhat CH, Nezhat F. Hospital cost
comparison between abdominal, vaginal and laparoscopy
assisted vaginal hysterectomies. Obstet Gynecol 1994;
83(5): 713-716.
- Ransom
SB, Mc Neeley SG, Whight C, Diamond MP. A cost analysis of
endometrial ablation, abdominal hysterectomy, vaginal
hysterectomy and LAVH in the treatment of primary
menorrhhagia. Journal of the American Association of
Gynecologic Laparoscopists.1996; 4: 29-32.
- Summitt
RL, Stovall TG, Lipscomb GH, Ling FW. Randomised
comparison of laparoscopy-assisted vaginal hysterectomy
with standard vaginal hysterectomy in an outpatient
setting. Obstet Gynecol 1992; 80(6): 895-901.
- Kalogirou
D, Antoniou G; Karakitsos P; Zioris C, Salampasis C.
Comparison of abdominal and vaginal hysterectomy. Study of
complications. Clin Exp Obstet Gynecol 1996; 23(3):
161-167.
- Langebrekke
A; Eraker R; Britt-Ingjerd N et al . Abdominal
hysterectomy should not be considered as a primary method
of uterine removal. A prostpective study of 100 patients
referred to hysterectomy. Acta Obstet Gynecol Scand 1996;
75: 404- 407.
- Gross
CP, Nicholson W, Powe NR. Factors affecting prophylactic
oophorectomy in postmenopausal women. Obstet Gynaecol
1999;94:962-8.
- Ottosen
C. Lingman G, Ottosen L. Three methods for hysterectomy: a
randomised , prospective study of short term outcome. Br J
Obstet Gynaecol 2000;107:1380-5.
|






