Autismo
El autismo es un trastorno grave del desarrollo neurológico que dura toda la vida y se caracteriza por dificultades en diversos dominios.1 Esta enfermedad limita la capacidad del paciente para funcionar con normalidad. Entre los aspectos principales de este trastrono multifacético se incluyen las anormalidades conductuales, las limitaciones sociales, las anormalidades en el procesamiento sensorial y las alteraciones en la capacidad de comunicación.
Según la Autism Society of America (ASA), actualmente el autismo es considerado una epidemia. Hoy por hoy se cree que un millón y medio de estadounidenses –incluidos nińos y adultos– padecen autismo. Desgraciadamente, dicho número se incrementa.
El autismo es un trastorno de etiología diversa y no existe un marcador biológico para su diagnóstico o un examen para distinguir a los sujetos autistas con precisión y seguridad.2 Actualmente se estima que en la susceptibilidad al autismo están involucrados más de 15 genes.3 La relación entre el autismo y las alteraciones en la respuesta inmune fue seńalada en un estudio efectuado recientemente, en el cual se informó un aumento en los niveles de citoquinas en nińos con trastornos incluidos en el espectro del autismo.4 En un estudio efectuado en adolescentes con autismo se informó la presencia de un grupo de anormalidades cerebrales estructurales junto con un agrandamiento significativo del volumen de la sustancia gris.5 No obstante, también se sugirió la asociación con otros factores ambientales como el mercurio6 y con la exposición materna durante la gestación.7
Se desconoce el modo de inicio del autismo y de las anormalidades del crecimiento y desarrollo cerebral en esta enfermedad. Actualmente ciertos expertos como Bauman y col.8 proponen que el inicio de los trastornos neurológicos es prenatal y tiene lugar antes de las 30 semanas de gestación. No obstante, los padres de los pacientes refieren tanto la presencia de irregularidades desde el nacimiento como un desarrollo normal hasta un determinado momento en el cual comienza la regresión o el deterioro. Esto se debería a la heterogeneidad de la población autista.
Aunque no existe cura para el autismo, a lo largo de los ańos se evaluaron diferentes estrategias terapéuticas. Los tratamientos convencionales se centran en las intervenciones educativas o del desarrollo. En cambio, mediante las terapias complementarias y alternativas se pretende erradicar la causa.9 La secretina es una opción para el tratamiento del autismo que se popularizó luego de la atención generalizada proporcionada por los medios de comunicación. El interés en la administración de secretina para el tratamiento del autismo fue generado mediante un estudio efectuado por Horvath y col.10 en 1998. En este estudio, tres nińos con autismo fueron sometidos a endoscopia debido a problemas de índole gastrointestinal y diarrea crónica. Antes de la infusión de secretina, se había evaluado el estado psicológico y el nivel de desarrollo de cada nińo. Luego de la administración de secretina se efectuó una evaluación basada en las observaciones de los maestros y terapeutas, quienes no tenían conocimiento sobre el tratamiento con secretina, en un video en el cual se podía observar la conducta de los nińos y en entrevistas a los padres. De acuerdo con los resultados, se observó una mejoría significativa en el lenguaje, la conducta y la capacidad de comunicación e interacción social.
El propósito del presente artículo es actualizar la primera revisión efectuada mediante la inclusión de estudios nuevos. En un principio, se discutirán brevemente los estudios en los cuales se examinaron los aspectos neurógenos de la secretina. Luego se analizarán los estudios en los cuales se evaluó la utilidad de la administración de secretina a los pacientes autistas.
Secretina
La secretina es una hormona gastrointestinal compuesta por 27 aminoácidos secretada en respuesta al pasaje de alimento por el intestino. La función principal de esta hormona es incrementar el volumen y el contenido de bicarbonato de los jugos pancreáticos. La secretina es una hormona puramente peptídica. Las formas sintéticas tienen secuencias de aminoácidos idénticas a la secretina humana o porcina. Las inyecciones de secretina están aprobadas por la Food and Drug Administration (FDA) para ser utilizadas in vivo para el diagnóstico de los trastornos gastrointestinales. Existen indicios crecientes acerca de la función adicional de la secretina en el sistema nervioso central. El interés en la secretina se intensificó debido a que en muchos estudios se demostró que puede atravesar la barrera hematoencefálica,11 que tiene función de neuropéptido12 y que es capaz de activar regiones cerebrales que incluyen las áreas que presentan anormalidades en el autismo.13
Koves y col.12 estudiaron la distribución de la inmunorreactividad de la secretina en el sistema nervioso de humanos, gatos y ratas mediante un enfoque inmunohistoquímico conocido como técnica ABC o método de inmunofluorescencia. Así, efectuaron el mapeo de los elementos de inmunorreactividad a la secretina en las ratas. La distribución hallada se comparó con aquella presente en los gatos y en los seres humanos. Se concluyó que, más allá del tracto gastrointestinal, existe síntesis de secretina en estructuras del sistema nervioso central como las células cerebelares de Purkinje, los núcleos cerebelares centrales, las células piramidales de la corteza motora, las células sensitivas primarias y algunas células de las estructuras límbicas. Koves y col. observaron que la secretina estaba presente en el sistema nervioso y en los ganglios sensitivos de ratas, gatos y seres humanos. Este hallazgo sustenta el punto de vista que indica que la secretina no es solamente un péptido gastrointestinal, sino también un neuropéptido.
En un estudio realizado por Kuntz y col.14 se investigó el efecto de la administración periférica de secretina en concentraciones similares a las de los aminoácidos extracelulares en el hipocampo de ratas. Con dicho objetivo, se aplicó la técnica de microdiálisis en el hipocampo de ratas con libertad de movimiento. Dicha técnica permite la determinación fehaciente de la concentración extracelular de los neurotransmisores cerebrales. Debido al supuesto papel del glutamato y el ácido gamma aminobutírico (GABA) en el autismo, se estudió el efecto producido por la secretina sobre dichos neurotransmisores. Se inyectó una dosis de 30 unidades clínicas (UC)/kg de peso corporal, correspondiente a 8.7 μg/kg de pentahidrocloruro de secretina. Luego de la inyección se observó, mediante la técnica de microdiálisis mencionada, un aumento de los niveles de glutamato y GABA. No obstante, ningún otro aminoácido se modificó. Los resultados de este estudio concuerdan con los hallazgos de Yung y col.,15 quienes informaron que la secretina facilita la neurotransmisión gabaérgica en el cerebelo de la rata.
Estudios sobre la efectividad de la administración de secretina para tratar el autismo
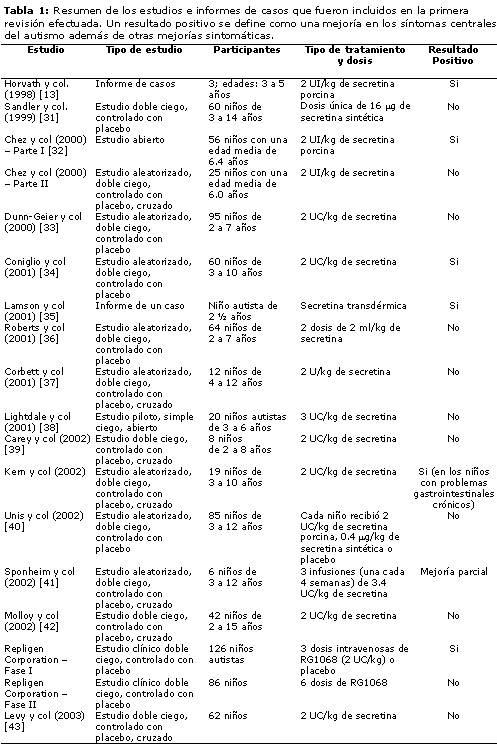
Desde 1998, luego de que en el estudio realizado por Horvath y col.10 se informó una mejoría en los nińos con autismo que habían sido tratados con secretina, fueron llevados a cabo varios estudios. En la tabla 1 se resumen los resultados de los trabajos incluidos en la primera revisión efectuada.
Actualización sobre estudios de casos y ensayos clínicos
La utilidad de la secretina para el tratamiento del autismo continúa en evaluación mediante el estudio de casos y los ensayos clínicos. La búsqueda para la realización de esta revisión fue efectuada mediante la utilización de las bases de datos PubMed y Medline (desde 1998 hasta marzo de 2006). Los términos utilizados para efectuar la búsqueda fueron los siguientes: “secretina”, “autismo” y “secretina y autismo”. En el resto de esta sección se discuten estudios más recientes no mencionados en la revisión previa.
Richman y col.16 informaron el estudio de un caso sobre el efecto de la administración de secretina a un nińo de 4 ańos con diagnóstico de autismo que recibió una dosis de 2 UC/kg. Los datos fueron recolectados antes y después de la administración de acuerdo con las siguientes categorías principales: deficiencias en la comunicación, intereses y conductas repetitivas y trastornos en las interacciones sociales. Los resultados se obtuvieron mediante la utilización de las escalas Childhood Autism Rating Scale, Autism Diagnostic Observation Schedule-Generic, Motor Imitation Scale e Interactive Imitation Scale. De acuerdo con los resultados, la secretina no tuvo efectos sustanciales sobre la interacción social o la estereotipia. El único cambio positivo informado que persistió hasta los 3 meses luego de la administración de secretina fue una mejoría leve en el contacto visual. No obstante, la madre del nińo estudiado refirió que la duración del contacto visual sostenido fue muy breve y no presentó cambios. Además, de acuerdo con lo referido por la madre del paciente a los 3 meses de seguimiento, la administración de secretina no produjo cambios conductuales significativos.
Owley y col.17 llevaron a cabo un estudio sobre la efectividad de la secretina en 2001. Efectuaron un estudio cruzado, controlado con placebo, a doble ciego para evaluar la eficacia de la administración endovenosa de secretina porcina para el tratamiento del autismo en 56 nińos de 3 a 12 ańos. Los nińos recibieron 2 UC/kg de secretina al inicio (grupo secretina-placebo) o al final de la semana 4 (grupo placebo-secretina). Los resultados fueron determinados principalmente mediante la Autism Diagnostic Observation Schedule (ADOS). No se hallaron diferencias significativas entre el grupo tratado con secretina y el que recibió placebo en el puntaje de la ADOS correspondiente al desempeńo social y la comunicación. Los hallazgos del estudio contrastaron con los hallazgos del estudio de Horvath y col.10 en el cual se utilizó secretina porcina.
Recientemente, Pallanti y col.18 informaron los casos de dos nińos autistas de 9 y 7 ańos en los cuales se confirmaron los resultados de Horvath y col.19 Se sugiere entonces que los nińos autistas con reflujo gastroesofágico y un cociente intelectual elevado pueden constituir un subtipo de pacientes con buena respuesta a la secretina. En primer lugar se evaluó la inteligencia de los nińos mediante la Stanford-Binet Intelligence Scale. Luego se administró una dosis intravenosa de secretina de 2 CU/kg de peso corporal. El propósito fue administrar 6 inyecciones consecutivas de secretina, una cada 4 semanas. Se utilizaron la Behavioral Summarized Evaluation, la Clinical Global Impression Scale y la Childhood Autism Rating Scale. Uno de los nińos tenía esofagitis por reflujo, mientras que el otro padecía diarrea crónica. Fueron evaluados antes y luego del tratamiento y durante el seguimiento con intervalos de un día, una semana, cuatro semanas y seis meses a partir del tratamiento inicial. La administración de secretina provocó una mejoría significativa y duradera de los síntomas principales solamente en el nińo que tenía esofagitis por reflujo. Con respecto al segundo nińo, que tenía diarrea crónica, el tratamiento fue suspendido luego de la segunda inyección ya que no se informaron efectos ni mejorías. Se observaron mejorías significativas en el uso del bańo, el sueńo, la risa, el llanto o la risa nerviosa en momentos inapropiados, la respuesta al tacto, luces, sonidos, gustos o aromas y en la conciencia del dolor, calor o frío. Además se advirtió una mejoría conductual global y, en particular, relacionada con la ingesta. El estudio confirmó aun más lo sugerido por Horvath y col.19 y también corroboró el efecto inhibidor sobre las secreciones gástricas que posee la secretina.20 Además, los autores sugirieron que es posible que los nińos autistas con reflujo gastroesofágico y un cociente intelectual elevado representen un subtipo de paciente que probablemente responde mejor a la administración de secretina. Llamativamente, Kern y col.21 hallaron que los nińos con diarrea crónica activa presentaron una disminución de las conductas aberrantes al ser tratados con secretina.
En un estudio llevado a cabo en 2006 por Toda y col.,22 se investigó la influencia de la administración endovenosa de secretina sobre el sistema dopaminérgico y serotoninérgico del sistema nervioso central en nińos autistas. Al igual que lo informado en un estudio previo23 se sugirió la participación de dichos sistemas en la patogénesis del autismo. Toda y col. investigaron la efectividad de la administración de secretina a 12 nińos con autismo de 4 a 6 ańos en un estudio a simple ciego y cruzado. Antes del inicio del estudio se efectuaron análisis de sangre, de los metabolitos urinarios de la secretina, resonancia magnética nuclear (RMN) cerebral, tomografía computarizada por emisión de fotón único (SPECT) cerebral y electroencefalograma para excluir a los pacientes con alguna lesión. Se administró secretina o solución salina fisiológica en goteo endovenoso durante 1 hora de manera alternada con intervalos de 4 semanas. La dosis de secretina osciló entre las 8 y 12 unidades/kg. Se utilizó la Autism Diagnostic Interview - Revised (ADI-R) para evaluar la conducta previa a la administración y luego de 2, 4, 6 y 8 semanas para estimar la mejoría sintomática. Los autores investigaron la relación entre la mejoría sintomática y los cambios en los niveles del metabolito de la dopamina ácido homovanílico (AHV), del metabolito de la serotonina ácido 5-hidroxindol-3-acético (5-HIAA), y de la coenzima 6R-5,6,7,8-tetrahidro-L-biopterina en el líquido cefalorraquídeo (LCR) antes y después de la administración de secretina. Como resultado del estudio se halló un aumento de los niveles de AHV en el LCR de todos los nińos que presentaron mejorías en el puntaje de la ADI-R luego de la administración de secretina. No obstante, el nivel de AHV también se incrementó en 2 de los 5 nińos que no presentaron mejorías en el puntaje de la ADI-R. El nivel de 5-HIAA en el LCR aumentó en 7 nińos, 5 de los cuales presentaron puntajes de la ADI-R coincidentes con una mejoría sintomática. Además, el nivel de 6R-5,6,7,8-tetrahidro-L-biopterina aumentó significativamente en 5 nińos y disminuyó o no se modificó positivamente en otros 5 nińos. El puntaje de la ADI-R mejoró en todos los nińos con un nivel elevado de 6R-5,6,7,8-tetrahidro-L-biopterina. Ningún nińo sin un aumento en el nivel de 6R-5,6,7,8-tetrahidro-L-biopterina presentó una mejoría en el puntaje de la ADI-R. De acuerdo con los resultados del estudio, la secretina activaría el recambio metabólico de la dopamina en el sistema nervioso central mediante un aumento de los niveles de 6R-5,6,7,8-tetrahidro-L-biopterina, lo cual resultaría en una mejoría sintomática. Luego de la administración de secretina, el puntaje de la ADI-R mejoró en 7 de los 12 nińos y la conducta destructiva como el mal carácter, la agresividad y la automutilación mejoró en 4 de los 12 nińos. Adicionalmente, en 3 de los 12 nińos, la hiperactividad y la concentración mejoraron. No obstante, en 2 de los 12 nińos se percibió un deterioro sintomático.
En 2005, Ratliff-Schaub y col. llevaron a cabo un estudio a doble ciego, aleatorizado, controlado y cruzado para evaluar la efectividad de la administración de secretina por vía transdérmica.24 Participaron 15 nińos con diagnóstico de autismo o trastorno generalizado del desarrollo de 4.5 a 9.8 ańos. La distribución se llevó a cabo mediante la aplicación de una tabla de números aleatorios para asignar el orden del tratamiento a administrar. Este consistía en períodos sucesivos de 4 semanas interrumpidos por un período de lavado farmacológico. Todos los nińos recibieron diariamente 2 UC/kg de secretina formulada como ungüento durante 4 semanas. Los resultados se determinaron mediante la Autism Treatment Evaluation Checklist (ATEC), la cual fue aplicada por los padres y maestros al inicio del estudio y cada una de las 4 semanas durante las cuales los nińos recibían placebo o tratamiento activo. De acuerdo con los resultados del estudio, no se observaron diferencias significativas en la disminución del puntaje de la ATEC entre la administración de secretina y placebo. Tampoco fue significativa la diferencia en el lenguaje, la sociabilidad, la esfera sensorial y el estado de salud entre los grupos tratados con secretina o placebo. El estudio reveló que los efectos de la secretina no fueron significativamente diferentes en comparación con el placebo. De los 15 nińos, 7 no recibieron medicación adicional alguna durante el estudio y los 8 restantes tomaban alguna medicación concomitante. También se sugirió una mejoría moderada en el lenguaje de los nińos que no recibían medicación adicional. Los autores informaron, además, la ausencia de diferencias en el lenguaje, la sociabilidad o la esfera sensorial al comparar los resultados de la administración de secretina con la de placebo en los nińos con diarrea. Se concluyó que la pequeńa magnitud de la muestra pudo haber afectado los resultados. En consecuencia, los autores recomendaron la realización de estudios adicionales con un número mayor de participantes antes de recomendar el tratamiento con secretina.
En 2005, Handen y Hofkosh25 llevaron a cabo un estudio piloto, cruzado, a doble ciego y controlado con placebo para evaluar la efectividad de la administración de secretina porcina para tratar los síntomas de los pacientes autistas. Se evaluó la seguridad y la eficacia de dicho tratamiento en ocho nińos autistas sin trastornos gastrointestinales. La edad de los nińos osciló entre 6 y 9 ańos. El cociente intelectual varió entre el retraso mental moderado y un nivel mayor de capacidad. El estudio tuvo una duración de 4 meses. Luego de las evaluaciones iniciales, los participantes fueron asignados para integrar el grupo secretina/placebo o el grupo placebo/secretina; la dosis de secretina administrada fue de 2 UC/kg. El seguimiento incluyó evaluaciones al finalizar las semanas 1 y 2 y el primer y segundo mes luego de la infusión. Los resultados se determinaron mediante la aplicación de la Aberrant Behavior Checklist, Clinical Global Impressions Scale, The Dosage Record and Treatment Emergent Symptom Scale y la Gilliam Autism Rating Scale. No se observaron diferencias significativas entre los grupos tratados con secretina o placebo en cuanto a la reducción de los síntomas. Los resultados coincidieron con investigaciones previas sobre la efectividad de la secretina. Mediante la evaluación más profunda de las respuestas individuales se demostró una amplia gama de resultados terapéuticos. Un nińo presentó una disminución significativa del puntaje de la subescala de irritabilidad. Sin embargo, otros dos presentaron un empeoramiento de los síntomas tras la administración de secretina. Un nińo experimentó una mejoría significativa de las características centrales del trastorno y del comportamiento 3 a 4 semanas luego de la administración de secretina. Como conclusión se informó la necesidad de efectuar investigaciones más profundas sobre la utilización de la secretina para el tratamiento del autismo.
La Repligen Corporation,26 que posee los derechos para SecreFloTM, llevó a cabo varios ensayos clínicos. Entre ellos se incluyó un estudio clínico de fase III a doble ciego y controlado con placebo. En él se evaluó a 132 nińos de 2 ańos y 8 meses a 4 ańos y 11 meses con síntomas de autismo moderados a graves. Los nińos fueron evaluados al inicio del estudio. Luego se les administró RG1068 o placebo durante 18 semanas. A continuación fueron reevaluados para detectar la aparición de mejorías sintomáticas. El estudio se realizó con el propósito de demostrar mejoras en la interacción social evaluada mediante la Autism Diagnostic Observation Schedule (ADOS) y la Clinical Global Impression of Change (CGI). En 2004 Repligen informó públicamente que el estudio había fracasado debido a que no se alcanzó el objetivo principal, es decir, no se hallaron mejorías en la interacción social de acuerdo con los resultados de la aplicación de la ADOS y la CGI. No se descubrieron diferencias significativas en los efectos adversos entre el grupo que recibió la droga activa y el que recibió placebo y no se informaron efectos adversos graves. La compańía interrumpió sus investigaciones sobre el uso de secretina en el tratamiento del autismo y se involucró en estudios clínicos de evaluación del uso de dicho agente para tratar a los pacientes esquizofrénicos (comunicación verbal, Repligen Corporation, febrero de 2006).
Conclusión
El uso de secretina para el tratamiento del autismo es un tema que recibió mucha atención debido a los informes de casos en los cuales se obtuvieron mejorías significativas de los síntomas centrales. Si bien el mecanismo de acción de la secretina es relativamente desconocido, en algunos estudios se sugirió la posibilidad de que la secretina no cumpliera solamente la función de neuropéptido gastrointestinal, sino también la de un neuropéptido12 capaz de atravesar la barrera hematoencefálica.11 Este gran interés resultó en la realización de varios estudios para evaluar la administración de secretina para tratar el autismo. Los resultados fueron heterogéneos. No obstante, principalmente se sugiere la ausencia de un alivio sintomático o de un beneficio significativo en comparación con la administración de placebo.
De acuerdo con los resultados de los estudios efectuados por Pillanti y col.18 y por Kern y col.21 existiría un “subtipo gastrointestinal” de nińos autistas que responden de manera positiva a la administración de secretina. No obstante, no se sabe en qué medida dicho subgrupo contribuyó en la obtención de resultados positivos, ya que este aspecto no se estudió de manera adecuada. Para obtener conclusiones sólidas es necesario efectuar investigaciones adicionales acerca de la efectividad de la administración de secretina a un determinado subgrupo de pacientes.
Finalmente, en los estudios clínicos sobre el tratamiento con secretina efectuados en nińos se verificó un efecto significativo mediante la administración de placebo. Sandler27 informó que la expectativa positiva de los padres esperanzados o aquella transmitida por los medios de comunicación provocaría la magnificación del efecto placebo hallada en los estudios. Los padres esperanzados pueden malinterpretar las variaciones en la conducta como una prueba de efectividad.
En conclusión, los resultados de los estudios de investigación sobre la administración de secretina para tratar el autismo fueron desfavorables y heterogéneos. La complejidad y disparidad de los síntomas en combinación con la falta de entendimiento claro de la etiopatogenia del autismo pueden contribuir con la heterogeneidad de los resultados obtenidos en los estudios.
BIBLIOGRAFÍA
1. Esch BE, Carr JE. Secretin as a treatment for autism: a review of the evidence. Journal of Autism and Developmental Disorders 2004; 34(5):543-556.
2. Gomut M, Bernard FA, Davis MH et al. Change detection in children with autism:an auditory event-related fMRI study. NeuroImage 2006; 29:475-484.
3. Ozonoff S, Rogers SJ. From Kanner to the Millennium. Scientific advances that have shaped clinical practice. In Ozonoff S, Rogers SJ, Hendren RL. Autism spectrum disorders: a research review for practitioners, 2003; pp. 3-33. American Psychiatric Publishing Inc.: Arlington, VA.
4. Fombonne E. Epidemiology of autistic disorder and other pervasive developmental disorders. Journal of Clinical Psychiatry 2005; 66(10):3-8.
5. Steingard RJ, Connor DF, Au T. Approaches to psychopharmaology. In Bauman ML, Kemper TL. The neurobiology of autism (2nd edition) 2005; pp. 79-102. The John Hopkins University Press: Baltimore, Maryland.
6. Veenstra-VanderWeele J, Christian SL, Cook EH Jr. Autism as a paradigmatic complex genetic disorder. Annual Review of Genomics and Human Genetics 2004; 5:379-405.
7. Molloy CA, Morrow AL, Meinzen-Derr J et al. Elevated cytokine levels in children with autism spectrum disorder. Journal of Neuroimmunology 2006; 172(1-2):198-205.
8. Hazlett HC, Poe MD, Gerig G, Smith RG, Piven J. Cortical gray and white brain tissue volume in adolescents and adults with autism. Biological Psychiatry 2006; 59:1-6.
9. Geier MR, Geier DA. The potential importance of steroids in the treatment of autistic spectrum disorders and other disorders involving mercury toxicity. Medical Hypotheses 2005; 64(5):946-954.
10. Arn TL, Stodgell CJ, Rodier PM. The teratology of autism. International Journal of Developmental Neuroscience 2005; 23:189-199.
11. Bauman M, Filipek PA, Kemper TL. Early infantile autism. In Cerebellum and Cognition. Eds. J. D. Schmahmann, pp 367-386. San Diego: Academic Press.
12. Levy SE, Hyman SL. Novel treatments for autistic spectrum disorders. Mental Retardation and Developmental Disabilities 2005; 11:131-142.
13. Horvath K, Stefanatos G, Sokolski KN, Wachtel R, Nabors L, Tildon J. Improved social and language skills after secretin administration in patients with autistic spectrum disorders. Journal of Association Academy of Minority Physicians 1998; 9:9-15.
14. Dogrukol-Ak D, Tore F, Tuncel N. Passage of VIP/PACAP/ secretin family across the blood-brain barrier: therapeutic effects. Current Pharmacological Design 2004; 10:1325-1340.
15. Koves K, Kausz M, Reser D et al. Secretin and autism: a basic morphological study about the distribution of secretin in the nervous system. Regulatory Peptides 2004; 123:209-216.
16. Kuntz A, Clement HW, Lehnert W et al. Effects of secretin on extracellular amino acid concentrations in rat hippocampus. Journal of Neural Transmission 2004; 111:931-939.
17. Yung WH, Leung PS, Ng SSM et al. Secretin facilitates GABA transmission in the cerebellum. Journal of Neuroscience 2001; 21(18):7063-7068.
18. Pallanti S, Lassi S, La Malfa G et al. Short report: autistic gastrointestinal and eating symptoms treated with secretin: a subtype of autism. Clinical Practice and Epidemiology in Mental Health 2005; 1(24).
19. Horvath K, Papadimitriou JC, Rabsztyn A et al. Gastrointestinal abnormalities in children with autistic disorder. Journal of Pediatrics 1999; 135:559-563.
20. Chung I, Li P, Lee K, Chang T, Chey WY. Dual inhibitory mechanism of secretin action on acid secretion in totally isolated, vascularly perfused rat stomach. Gastroenterology 1994; 107:1751-1758.
21. Kern JK, Miller VS, Evans PA, Trivedi MH. Efficacy of porcine secretin in children with autism and pervasive developmental disorder, Journal of Autism and Developmental Disorders 2002; 32(3):153-160.
22. Toda Y, Mori K, Hashimoto T et al. Administration of secretin for autism alters dopamine metabolism in the central nervous system. Brain and Development 2005; (in press).
23. Segawa M. A neurological model of infantile autism (in Japanese). No No Kagaku 1998; 20:169-75.
24. Ratliff-Schaub K, Carey T, Reeves GH, Rogers MM. Randomized controlled trial of transdermal secretin on behavior of children with autism. Autism 2005; 9(3):256-265.
25. Repligen Corporation. Phase 3 study of secretin for autism fails to meet dual primary endpoints development of secretin for schizophrenia to continue. Press Release, 2004.
26. Welch MG, Keune JD, Welch-Horan TB, Anwar N, Anwar M, Ruggiero DA. Secretin activates visceral brain regions in the rat including areas abnormal in autism. Cellular and Molecular Neurobiology 2003; 23:817-837.
27. Owley T, McMahon W, Cook EH et al. Multisite, double-blind, placebo-controlled trial of porcine secretin in autism. Journal of the American Academy of Child and Adolescent Psychiatry 2001; 40(11):1293-1299.
28. Sandler A. Placebo effects in developmental disabilities: Implication for research and practice. Mental Retardation and Developmental Disabilities Research Reviews 2005; 11:164-170.
29. Handen B, Hofkosh D. Secretin in children with autistic disorder: a double-blind, placebo controlled trial. Journal of Developmental and Physical Disabilities 2005; 17(2):95-106.
30. Richman DM, Reese RM, Daniels D. Use of evidence-based practice as a method for evaluating the effects of secretin on a child with autism. Focus on Autism and Other Developmental Disabilities 1999; 14(4):204-211.
31. Sandler AD, Sutton KA, Deweese J, Girardi MA, Shepard V, Bodfish JW. Lack of benefit of a single dose of synthetic human secretin in the treatment of autism and pervasive developmental disorder. New England Journal of Medicine 1999; 341(24):1801-1806.
32. Chez MG, Buchanan CP, Bagan BT et al. Secretin and autism: a two part clinical investigation. Journal of Autism and Developmental Disorders 2000; 30:87-94.
33. Dunn-Geier J, Ho HH, Auesperg E et al. Effect of secretin on children with autism: a randomized controlled trial. Developmental Medicine and Child Neurology 2000; 42:796-802.
34. Coniglio SJ, Lewis JD, Lang C et al. A randomized, double-blind, placebo-controlled trial of single-dose intravenous secretin treatment for children with autism. Journal of Pediatrics 2001; 138:649-655.
35. Lamson DW, Plaza SM. Transdermal secretin for autism-a case report. Alternative Medicine Review 2001; 6:311-313.
36. Roberts W, Weaver L, Brian J et al. Repeated doses of porcine secretin in the treatment of autism: a randomized, placebo-controlled trial. Pediatrics 2001; 107(5):E71.
37. Corbett B, Khan K, Czapansky-Beilmand D et al. A double-blind, placebo-controlled crossover study investigating the effect of porcine secretin in children with autism. Clinical Pediatrics 2001; 40:327-331.
38. Lightdale JR, Hayer C, Duer A et al. Effects of intravenous secretin on language and behavior of children with autism and gastrointestinal symptoms: a single-blinded, open-label pilot study. Pediatrics 2001; 108(5):E90.
39. Carey T, Ratliff-Schaub K, Funk J, Weinle C, Myers M, Jenks J. Double-blind placebo-controlled trial of secretin: effects on aberrant behavior in children with autism. Journal of Autism and Developmental Disorders 2002; 32(3):161-167.
40. Unis AS, Munson JA, Rogers SJ et al. A randomized, double-blind, placebo-controlled trial of porcine versus synthetic secretin for reducing symptoms of autism. Journal of the American Academy of Child and Adolescent Psychiatry 2002, 44(11):1315-1231.
41. Sponheim E, Oftedal G, Helveschou SB. Multiple doses of secretin in the treatment of autism: a controlled study. Acta Paediatrica 2002; 91:540-545.
42. Molloy CA, Manning-Courtney P, Swayne S et al. Lack of benefit of intravenous synthetic human secretin in the treatment of autism. Journal of Autism and Developmental Disorders 2002; 32(6):545-551.
43. Levy SE, Souders MC, Wray J et al. Children with autistic spectrum disorders. Comparison of placebo and single dose of human synthetic secretin. Archives of Disease in Childhood 2003; 88:731-736.
|


![]()
![]()
