Introducciůn
Hace ya mŠs de un siglo Escherich describiů una bacteria aislada de heces de
individuos sanos y la denominů Bacterium coli comune.
Este microorganismo anaerobio facultativo, conocido actualmente como
Escherichia coli es un habitante normal del intestino grueso de los
mamŪferos, donde juega un papel importante en su fisiologŪa; la mayorŪa de las
cepas de E. coli son inofensivas y ademŠs pueden ejercer un efecto
protectivo por impedir la proliferaciůn de otras mŠs virulentas. Pero la minorŪa de
E. coli que causan enfermedad son un excelente ejemplo del modo por el
cual mŪnimas variaciones en la estructura genťtica pueden permitir a las bacterias
causar diferentes enfermedades como meningitis, septicemia, pielonefritis y
diarrea. Reciťn en 1945 Bray pudo comprobar que E. coli puede ser
diarreigťnico en humanos, especialmente en niŮos. Las cepas de E. coli
diarreigťnicas constituyen un grupo heterogťneo de microorganismos con
diferentes propiedades de virulencia y epidemiologŪa.
CategorŪas diarreigťnicas1
Escherichia coli enterotoxigťnica (ETEC) se adhiere al intestino
delgado mediante fimbrias y elabora dos tipos de enterotoxinas: termolŠbil (LT) y
termoestable (ST). Escherichia coli enteroinvasiva (EIEC) invade el
enterocito y produce una diarrea similar a la producida por Shigella. Escherichia
coli enteropatogťnica (EPEC) produce la lesiůn A/E (attaching and
effacing) con destrucciůn de las microvellosidades. Escherichia coli
enterohemorrŠgica (EHEC) posee fimbrias de adherencia y elabora potentes
citotoxinas SLT (shiga-like-toxins) que se relacionan con el sŪndrome
urťmico-hemolŪtico (SUH). Escherichia coli enteroagregativa (EAEC)
tambiťn posee fimbrias de adherencia y elabora dos enterotoxinas. Escherichia
coli con adherencia difusa (DAEC) posee una fimbria mediadora de este tipo de
adherencia, pero aķn no existen estudios epidemiolůgicos concluyentes con
respecto a su capacidad diarreigťnica.2
Factores de patogenicidad1
Como la mayorŪa de los patůgenos, E. coli sigue una estrategia de
infecciůn: 1) colonizaciůn de un sitio en la mucosa, 2) evasiůn de las defensas del
huťsped, 3) multiplicaciůn, 4) daŮo al huťsped.
El hecho mŠs destacable de las cepas de E. coli diarreigťnicas es su
habilidad para colonizar la superficie de la mucosa intestinal, a pesar de los
movimientos peristŠlticos y de la competencia de los integrantes de la microbiota
normal, incluyendo cepas de E. coli no patůgenas.
La presencia de fimbrias de adherencia es una propiedad de todas las cepas de
E. coli, incluidas las no patůgenas. Sin embargo, las cepas diarreigťnicas
poseen antŪgenos fimbriales especŪficos que incrementan su habilidad colonizadora
y permiten su adherencia al intestino delgado, sitio que normalmente no es
colonizado.
Una vez que ha colonizado el intestino, sigue diferentes estrategias de patogťnesis,
segķn su tipo o categorŪa, a saber:
- producciůn de enterotoxinas (ETEC y EAEC),
- invasiůn (EIEC) y/o
- adherencia Ūntima con seŮales o eventos de membrana (EPEC y EHEC).
Cabe aclarar que el modo de interacciůn es especŪfico para cada categorŪa.
La versatilidad en el genoma de E. coli, que le confiere las diferentes
propiedades de virulencia, se fundamenta principalmente en dos configuraciones
genťticas: plŠsmidos de virulencia e islas cromosomales de patogenicidad. Las seis
categorŪas de E. coli diarreigťnicas descritas son portadoras de al menos
un plŠsmido de virulencia. Por una parte, EIEC, EHEC, EPEC y EAEC son portadoras
de familias de plŠsmidos, cada uno de los cuales codifica para mķltiples factores de
virulencia. Asimismo, EPEC, EHEC y EAEC poseen ademŠs genes cromosomales
organizados como un grupo denominado "isla de patogenicidad".
Los rasgos de patogenicidad individuales, como la producciůn de toxinas, pueden
ser codificados por transposones (toxina ST de ETEC) o por fagos (toxina
Shiga).3,4,5
Escherichia coli enteroagregativa (EAEC)
La observaciůn de la adherencia de EPEC a cťlulas HEp-2, realizada por
Cravioto y col. en 1979, fue crucial no sůlo en el campo de la investigaciůn de
EPEC, sino que permitiů, ademŠs, establecer dos categorŪas mŠs de E. coli
patogťnicas. El patrůn de adherencia de EPEC fue descrito como "adherencia
localizada", denotando la presencia de microcolonias en la superficie de las cťlulas
en cultivo. Las bacterias no EPEC adherŪan de una manera diferente que fue
definida inicialmente como "difusa". Sin embargo, en un estudio realizado por
Nataro, en Chile en 1987, se subdividiů el fenotipo difuso en dos categorŪas:
agregativas y difusas "verdaderas". Las agregativas se distinguen por la
autoaglutinaciůn de las bacterias y por su adhesiůn, ademŠs, a la superficie de
vidrio del cubreobjetos. El patrůn se define como stacked-brick (pilas de
ladrillos). Mientras que en la adherencia difusa las bacterias se observan dispersas
sobre la superficie de las cťlulas HEp-2 con poca agregaciůn y poca adherencia al
vidrio entre las cťlulas.
A fines de la dťcada del '80 y comienzos de los '90, la relaciůn inconsistente entre
EAEC y diarrea condujo a dudar acerca de su papel como patůgeno humano, de
manera similar a lo ocurrido con EPEC en los '70.6
Si bien la patogenicidad de ETEC y EIEC pudo atribuirse a marcadores especŪficos y
demostrarse en modelos animales, la evidencia de la patogenicidad de EPEC fue
sůlo epidemiolůgica hasta 1978, cuando dos cepas de EPEC demostraron su
patogenicidad en adultos voluntarios. Y asŪ como con EPEC, en los primeros
aislamientos de EAEC no se pudo demostrar la presencia de ningķn factor de
virulencia conocido como diarreigťnico. La observaciůn de que estas cepas a
menudo eran recuperadas de individuos aparentemente sanos condujo a un
escepticismo sobre la patogenicidad de EAEC, hasta que dos estudios con
voluntarios y un nķmero de brotes de diarrea probaron que al menos algunas cepas
de EAEC causaban diarrea en humanos. AdemŠs, estudios de casos y controles y de
vigilancia en los ķltimos quince aŮos sugieren fuertemente que EAEC constituye una
causa importante de diarrea en personas de todas las edades en paŪses
industrializados y en vŪas de desarrollo.7,8
Patogťnesis
Las cepas EAEC producen aumento en la secreciůn de mucus con
atrapamiento de las bacterias formando una biopelŪcula de mucus y bacterias. Se
demostrů a travťs de diversos experimentos que esta pelŪcula se produce in
vivo, y tambiťn se observů que la diarrea por EAEC es predominantemente
mucosa, aunque no se ha dilucidado completamente el significado de esta
caracterŪstica. AdemŠs de esta propiedad, se ha observado que la infecciůn por
EAEC estŠ acompaŮada por efectos citotůxicos en la mucosa intestinal. Vial y col.,
en 1988, observaron la lesiůn producida por EAEC a travťs de microscopia ůptica.
La lesiůn se caracteriza por acortamiento de las microvellosidades, necrosis
hemorrŠgica de los extremos de la vellosidad y respuesta inflamatoria leve con
edema e infiltraciůn mononuclear de la submucosa. En biopsias de pacientes
fallecidos por diarrea persistente causada por EAEC se evidenciů la destrucciůn de
la mucosa ileal. Los efectos citotůxicos se demostraron por cultivo en cťlulas T84,
en las cuales la citotoxicidad causada por EAEC se manifiesta por vesiculizaciůn de
la membrana, seguida de muerte celular y exfoliaciůn de las cťlulas de la
monocapa. AdemŠs, este efecto se acompaŮa de incremento en la formaciůn de
vacuolas y separaciůn del nķcleo del citoplasma circundante. Estos efectos
citotůxicos requieren la presencia de genes codificados en un plŠsmido de 65 mDa,
que contiene ademŠs los genes que codifican la adherencia. Sin embargo, no todas
las EAEC producen efectos citotůxicos sobre la mucosa, lo cual indica la elevada
heterogeneidad que presentan estas cepas, y conduce a resultados inconsistentes
entre su presencia y diarrea, como demuestran algunos estudios
epidemiolůgicos.9,10,11
Adherencia
Nataro y col. identificaron en 1992 una estructura fimbrial flexible de 2 a 3 nm
de diŠmetro, denominada fimbria de adherencia agregativa I (AAF/I). La adherencia
a cťlulas HEp-2 producida por la cepa 17-2 estŠ mediada por esta fimbria. Los
genes que codifican para la fimbria estŠn organizados en dos grupos, separados por
9 Kb, dentro del plŠsmido pAA. La regiůn 1 contiene un grupo de genes requeridos
para la sŪntesis y el ensamblaje de la proteŪna, incluida la subunidad estructural de
la fimbria misma. La regiůn 2 contiene un gen activador de la transcripciůn,
denominado aggR.
MŠs recientemente se identificů una fimbria que presenta una homologŪa del 25%
con la primera y fue denominada AAF/II, cuya cepa prototipo es la 042, aislada en
Perķ.
No existen datos concluyentes sobre la frecuencia de apariciůn de una u otra. Las
fimbrias AAF son necesarias para la adherencia a cťlulas epiteliales y para la
formaciůn de la biopelŪcula. Una proporciůn considerable de EAEC presenta este
fenotipo pero no expresa ninguna de las fimbrias citadas, lo que indica que podrŪan
existir otras adhesinas de naturaleza no fimbrial, lo que aķn no se
demostrů.12,13
EAST1
Es una proteŪna de 38 residuos de aminoŠcidos, homůloga a ST (toxina
termoestable de ETEC), sůlo que en lugar de 6 residuos de cisteŪna, EAST1 presenta
4.14,15 Tambiťn presenta homologŪa con un pťptido de la
membrana de las cťlulas eucariotas, denominado guanilina, y se observů que
produce aumento en la diferencia de potencial y corriente de cortocircuito a travťs
de tejido ileal de conejo montado en using chambers. Se ha visto que el
gen astA que codifica para esta proteŪna, estŠ presente en el 40% de las
cepas EAEC, pero tambiťn se lo ha encontrado, aun con mayor frecuencia, en cepas
EHEC y tambiťn asociado a E. coli no patůgenas. En un estudio reciente
realizado en Japůn, cepas de E. coli que presentaron EAST1 como ķnica
caracterŪstica diarreigťnica, fueron incluidas como posibles
patůgenos.16
Otras citotoxinas
Los efectos tůxicos observados en modelos animales, en explantos de cťlulas
intestinales y en cťlulas T84 no son acompaŮados por internalizaciůn de la bacteria
o por adherencia Ūntima.1 Diversos grupos informaron la
identificaciůn de citotoxinas secretadas por EAEC. Es el caso de Pet, una
serinproteasa originalmente identificada como una proteŪna secretada capaz de
reducir la resistencia e incrementar la corriente de cortocircuito a travťs de tejido
yeyunal de rata montado en using chambers. AdemŠs de su actividad
enterotůxica, Pet tiene efectos citotůxicos en cťlulas epiteliales en cultivo y sobre
eritrocitos por un mecanismo que probablemente involucra la degradaciůn de la
proteŪna de membrana espectrina.17,18
Modelo propuesto para el mecanismo patogťnico de EAEC
Hasta el presente, con los datos disponibles, se puede formular sůlo una
hipůtesis del mecanismo: Nataro propone un modelo en tres etapas basado en
ensayos in vitro y con animales.
La primera etapa involucra la adherencia inicial a la mucosa intestinal o a la capa de
mucus o a ambas. Tanto AAF/I como AAF/II parecen ser las mediadoras de esta
primera etapa. En la segunda etapa se producirŪa un incremento en la producciůn
de mucus, que conducirŪa a la formaciůn de una biopelŪcula espesa conteniendo
bacterias. Esta biopelŪcula podrŪa facilitar la colonizaciůn persistente y contribuir a la
mala absorciůn de nutrientes. La tercera etapa, sugerida por evidencias
histopatolůgicas y moleculares, incluirŪa la elaboraciůn de citotoxinas que podrŪa
resultar en daŮo de las cťlulas intestinales. Con respecto al sitio de colonizaciůn, los
datos no son concluyentes, pero las evidencias seŮalan como mŠs probable la
colonizaciůn del intestino delgado.19,20
EpidemiologŪa
Un nķmero creciente de publicaciones sostienen la asociaciůn entre diarrea y
EAEC en los paŪses en vŪas de desarrollo, con mayor prominencia en diarreas
persistentes (14 dŪas o mŠs).
Parece haber una asociaciůn geogrŠfica entre EAEC y diarrea. En la India, por
ejemplo, se publicaron diferentes trabajos en los cuales EAEC fue hallado en
diarreas persistentes, pacientes ambulatorios e internados y casos esporŠdicos
detectados durante estudios de vigilancia. Tambiťn existen estudios realizados en
Brasil, en los cuales EAEC se asociů con diarreas persistentes en un elevado
porcentaje de casos. EAEC tambiťn ha sido implicada como agente causal en casos
esporŠdicos en Mťxico, Chile, Bangladesh e IrŠn.
Si bien la mayorŪa de los trabajos implican a EAEC en casos esporŠdicos endťmicos
de diarrea, cada vez se informa un mayor nķmero de brotes en los cuales este
patůgeno estŠ involucrado.21 Un ejemplo es el trabajo de
Eslava22 que describe dos brotes de diarrea ocurridos en el servicio
de nutriciůn de un hospital de la ciudad de Mťxico. Smith y col. informaron cuatro
brotes en Gran BretaŮa en 1994, que involucraron 19, 10, 51 y 53 pacientes. Los
sŪntomas en estos pacientes fueron vůmitos y diarrea, habitualmente sin fiebre. Si
bien cada uno de estos brotes estuvo relacionado con el consumo de comida en un
restaurante, no se pudo identificar un origen ķnico.
Detecciůn y diagnůstico
La infecciůn por EAEC se diagnostica mediante el aislamiento de E. coli
de las heces del paciente y la demostraciůn del patrůn agregativo en cťlulas
HEp-2. Esta prueba es el gold standard. Si bien se describieron diferentes
variantes de esta tťcnica, varios estudios comparativos sugieren que la forma
original de incubaciůn de las bacterias con las cťlulas durante 3 horas, sin cambio
de medio, es la que mejor permite discriminar entre los tres patrones, difuso,
agregativo y localizado.
Se demostrů que el plŠsmido de 60 mDa presente en la mayorŪa de EAEC tiene un
alto grado de homologŪa entre las diferentes cepas. A partir de ťl se desarrollů una
sonda de 1 Kb que, en general, presenta elevada especificidad.23,24
Se diseŮaron primers para detectar diferentes regiones del plŠsmido de 60
mDa. Estos primers pueden estar dirigidos a las regiones estructurales o
de regulaciůn de la expresiůn de las fimbrias o a la identificaciůn de los genes
codificadores de toxinas.
Los laboratorios de bacteriologŪa clŪnica no disponen, habitualmente, de un
laboratorio de cultivo de cťlulas para poder arribar al diagnůstico preciso de EAEC.
En nuestro medio, el esquema de diagnůstico no permite discriminar entre EPEC y
EAEC, ya que la clasificaciůn se realiza sobre la base de pruebas serolůgicas. En las
figuras 1 y 2 se observa la distribuciůn de frecuencias de patůgenos aislados en el
Hospital Materno Infantil Dr. Humberto Notti durante 1995 y 1996. Se observa que,
en general, EPEC se aŪsla en segundo lugar entre los patůgenos bacterianos, con
una frecuencia de alrededor de 20%.
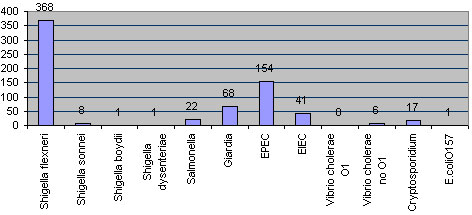
Figura 1. Distribuciůn de frecuencias de patůgenos aislados durante 1995 en el laboratorio de
BacteriologŪa del Hospital Materno Infantil Dr. Humberto Notti de la provincia de Mendoza, Argentina.
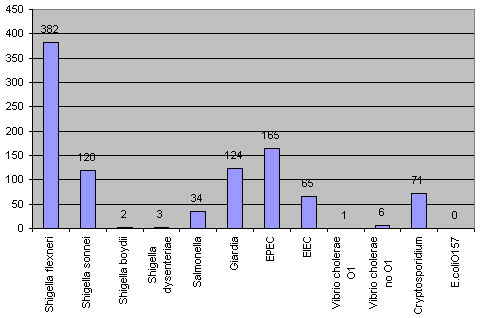
Figura 2. Distribuciůn de frecuencias de patůgenos aislados durante 1996 en el laboratorio de
BacteriologŪa del Hospital Materno Infantil Dr. Humberto Notti de la provincia de Mendoza, Argentina.
El interťs por arribar a un diagnůstico certero que permitiera evaluar la importancia
de EPEC no sůlo en cuanto a su frecuencia, sino a las caracterŪsticas de las cepas
circulantes en nuestro medio condujo a la realizaciůn de un primer
trabajo,25 en el que se utilizaron ensayos de adherencia en cťlulas
para distinguir entre los patrones localizado, difuso y agregativo, relacionados con
diferentes categorŪas diarreigťnicas, como se aclarů anteriormente. El fenotipo de
adherencia localizada fue encontrado en 15% de las cepas y el agregativo en 21%.
Estos resultados seŮalaron que entre las cepas clasificadas como EPEC sobre la
base de la serologŪa existŪa otra clase de cepas, con factores de patogenicidad
especŪficos, diferentes de EPEC.
A partir de estos resultados se propuso un segundo trabajo, orientado a proponer
una metodologŪa alternativa, que se utilice como prueba de tamizaje y que permita
restringir el cultivo de cťlulas para la confirmaciůn del resultado.
Este estudio estuvo orientado a evaluar la utilidad de PCR como herramienta para
el diagnůstico de EAEC, comparando los resultados con los obtenidos a travťs de la
prueba de referencia.
Materiales y mťtodo
Se estudiaron 87 cepas de Escherichia coli aisladas durante 1995 y
1996, identificadas por pruebas bioquŪmicas y serologŪa, correspondiendo cada cepa
a un caso de diarrea. La poblaciůn estudiada corrrespondiů a niŮos menores de 2
aŮos con diarrea aguda, atendidos en el Hospital Materno Infantil Dr. Humberto
Notti de la provincia de Mendoza.
Las muestras fueron obtenidas por evacuaciůn espontŠnea, recogidas en recipientes
estťriles y procesadas dentro de las 2 horas. Se realizaron extendidos para examen
microscůpico directo de materia fecal con tinciůn de Gram, tinciůn de azul de
metileno (observaciůn de leucocitos) y examen en fresco para la detecciůn de
Entamoeba histolytica y Giardia lamblia; para la investigaciůn de
Cryptosporidium se realizů tinciůn de Ziehl-Neelsen modificada.
Una diluciůn adecuada de materia fecal se destinů a la siembra en placas de Petri
con agar Mac Conkey. De cada placa se tomaron 3 colonias fermentadoras de
lactosa y se les realizaron las pruebas bioquŪmicas de rutina.
En cada colonia tipificada bioquŪmicamente como Escherichia coli se
investigaron los antŪgenos somŠticos "O", por la tťcnica de aglutinaciůn en
portaobjetos, utilizando sueros monovalentes provistos por el Instituto MalbrŠn. Los
serogrupos investigados fueron los siguientes: O26, O44, O55, O86, O111, O114,
O119, O125, O126, O127, O128, O136, O142. La investigaciůn de factores de
patogenicidad por PCR y ensayo de adherencia en cťlulas se realizů en las cepas
que fueron positivas para alguno de los serogrupos mencionados.
Ensayo de adherencia en cťlulas HEp-2
Se utilizaron cťlulas HEp-2 (ATCC: American Type Culture Collection),
adquiridas en la Asociaciůn Banco Argentino de Cťlulas (ABAC). Las cťlulas se
cultivaron en Minimum Essential Medium (MEM) con sales de Earle (Sigma Co.),
suplementado con 10% de suero fetal bovino (Gen) sin antibiůticos, en estufa a
37ļC y 5% de CO2. Se adaptů el mťtodo descrito por Cravioto y col.
en 1979. Los frascos de cultivo con monocapas de cťlulas fueron tripsinizados para
desprender las cťlulas, que se resuspendieron en MEM con suero fetal bovino 2%.
Se realizů recuento celular en cŠmara de Neubauer y luego 2.5x104
cťlulas se sembraron sobre cubreobjetos de vidrio dentro de placas de Petri de
vidrio de 50 mm y se incubaron hasta que alcanzaron el 70% de confluencia (24
hs.). Se retirů el MEM y se remplazů por medio fresco con 0.5% de D-manosa. Se
inocularon las placas con 20 μl de caldos de cultivos bacterianos, durante 3
horas a 37įC, se retirů el caldo, se lavů tres veces con PBS, se fijů con metanol y
se coloreů con Giemsa al 7.5%. Las cepas de referencia utilizadas en cada ensayo
fueron: 2348/69: patrůn de adherencia localizada; AA17-2: patrůn agregativo;
RS51-1: patrůn difuso, HS (O9:H4): patrůn negativo. Los ensayos se realizaron por
duplicado. Los cubreobjetos se montaron sobre portaobjetos y se observaron con
aumento 1 000x.
Amplificaciůn de un fragmento de la fimbria AAF/I
Esta regiůn forma parte del plŠsmido pCVD432 que estŠ relacionado con el
patrůn de adherencia agregativa en el ensayo en cťlulas HEp-2. Se utilizů el
siguiente set de primers:
pCVD432/start (5' CTG GCG AAA GAC TGT ATC AT 3') y pCVD432/stop (5' CAA
TGT ATA GAA ATC CGC TGT T 3'). El tamaŮo del fragmento amplificado es de 630
bp.26
A continuaciůn se transcribe la regiůn amplificada y la ubicaciůn de los primers
en su interior:

Condiciones de la reacciůn
Mezcla de nucleůtidos trifosfato (dNTP): 0.2 mM; MgCl2: 1.5
mM; cebadores: 0.5 μM de cada uno; Taq polimerasa: 2 unidades; buffer 10x
(usar 1X). Volumen final: 50 μl.
Esquema de ciclado
1 paso de 5 min a 94ļC
30 ciclos de 40 s a 94ļC
30 ciclos de 1 min a 53ļC
30 ciclos de 1 min a 72ļC
1 paso de 3 min a 72ļC
Control positivo: cepa AA 17-3
Control negativo: cepa HS
Amplificaciůn de un fragmento del gen de la enterotoxina EAST1
(Enteroaggregative Heat Stable Enterotoxin I)
Los cebadores fueron diseŮados para amplificar una regiůn de 108 pares de
bases (bp) del gen astA-1, que codifica para la enterotoxina EAST1 de
EAEC.
Estos fueron diseŮados en el Institut fŁr Hygiene und Mikrobiologie de la
Universidad de WŁrzburg, Alemania (datos no publicados).
START 5ī GCC ATC ACA GTA TAT CCG 3ī
STOP 5ī GCG AGT GAC GGC TTT GTA GT 3ī
A continuaciůn se reproduce parte de la secuencia del gen obtenida del Genbank Nį
de acceso L11241

Condiciones de la reacciůn
Mezcla de nucleůtidos trifosfato (dNTP): 0.2 mM; MgCl2:
1.5mM; cebadores: 0.6 μM de cada uno; Taq polimerasa: 2 unidades; buffer
10x (usar 1X).
Esquema de ciclado
1 paso de 5 min a 94ļC
30 ciclos de 40 s a 94ļC
30 ciclos de 1 min a 65ļC
30 ciclos de 1 min a 72ļC
1 paso de 3 min a 72ļC
Control positivo: cepa AA 17-3
Control negativo: cepa HS
Preparaciůn del templado
Se incubů 1 ml de un caldo de cultivo bacteriano en TSB (tripticasa soya
broth) durante 18 horas. Se centrifugů y el sedimento fue tratado con 150
μl de Tritůn 1% y hervido durante 10 minutos a 100ļC y centrifugado 5
minutos a 10 000 rpm. Para la reacciůn de PCR se emplearon 10 μl de
templado.
AnŠlisis con enzimas de restricciůn
El anŠlisis con enzimas de restricciůn constituye una metodologŪa para
comprobar que el fragmento amplificado presenta la secuencia especŪfica. Despuťs
de la reacciůn de PCR se llevů a cabo la digestiůn con AluI que corta el
producto de PCR de los primers de AAF/I en dos fragmentos de 391 y 239
bp26 y con HhaI que corta el producto de PCR de astA-
1 en dos fragmentos de 71 y 37 bp.27 En la figura 3
se observa la fotografža que muestra los productos de PCR.

Figura 3. Productos de PCR de los primers pCVD 432 y astA y anŠlisis con enzimas de
restricciůn. M: Marcador de peso molecular 100 bp. 1: Producto de amplificaciůn de 630 bp
de pCVD432. 2,3: Producto de digestiůn del amplificado de pCVD432, de 391 bp y 239 bp
obtenido con la enzima de restricciůn Alu I. 4: Control negativo. 5: Producto de
amplificaciůn de 108 bp de astA. 6,7: Producto de digestiůn del amplificado de astA,
de 71 bp y 37 bp obtenido con la enzima de restricciůn Hha I.
Resultados
Como se observa en la figura 4, segķn el ensayo de adherencia en cťlulas
HEp-2, 22 cepas (25%) mostraron el patrůn de adherencia localizada; 18 cepas
(21%) presentaron adherencia agregativa; 10 (11%) evidenciaron el patrůn difuso.
Estos resultados fueron similares a los hallados en un trabajo
anterior.25 En las figuras 5, 6 y 7 se observan las fotografžas
correspondientes a los patrones de adherencia.

Figura 4. Distribuciůn de los patrones de adherencia en cťlulas HEp-2. La figura muestra el porcentaje
observado para cada patrůn, sobre un total de 87 cepas.

Figura 5. Patrůn de adherencia localizada (1 000x) Las flechas seŮalan los acķmulos de bacterias
tŪpicos.
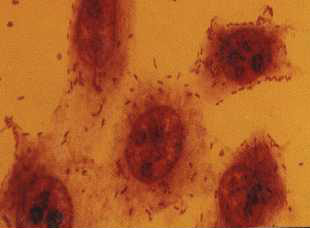
Figura 6. Patrůn de adherencia difusa (1 000x). Se observa la distribuciůn de las bacterias sobre la
superficie de las cťlulas, con escasa o nula adhesiůn sobre el cubreobjeto.
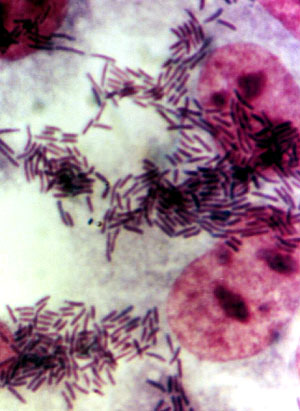
Figura 7. Patrůn de adherencia agregativa (1 000x). Las bacterias forman acķmulos entre sŪ, sobre las
cťlulas y sobre la superficie del cubreobjeto.
La tabla 1 muestra los resultados de PCR para AAF/I y de adherencia agregativa en
el ensayo en cťlulas HEp-2. Ocho cepas de las 18 que presentaron el patrůn de
adherencia agregativa portaron el gen de AAF/I. Las 10 cepas que presentaron
adherencia agregativa pero fueron negativas para AAF/I estarŪan indicando que
otros factores, fimbriales o no, podrŪan estar involucrados en la adherencia. Cinco
cepas positivas para AAF/I no presentaron el fenotipo agregativo, lo que seŮala la
posibilidad de existencia de otras condiciones para la expresiůn de la fimbria de
adherencia.

Tabla 1. Comparaciůn de los resultados de PCR para AAF/I PCR y del patrůn de adherencia agregativa
en el ensayo en cťlulas HEp-2.
La tabla 2 compara el resultado de EAST1 PCR y el ensayo en HEp-2. Mientras que
25 cepas portaron el gen de EAST1, sůlo 13 de ťstas expresaron el patrůn de
adherencia agregativa en el ensayo en HEp-2, lo cual parece estar en relaciůn con
el hecho de que la presencia del gen de EAST1 fue encontrado en otras categorŪas
de E. coli diarreigťnicas como EPEC y EHEC. Cinco cepas que presentaron
el fenotipo agregativo en el ensayo en HEp -2 fueron negativas para EAST1.

Tabla 2. Comparaciůn de los resultados de PCR para EAST 1 PCR y del patrůn de adherencia
agregativa en el ensayo en cťlulas HEp-2.
La tabla 3 compara la presencia de uno o ambos genes con el ensayo en HEp-2.
Treinta y dos cepas portan los genes, elevando considerablemente la sensibilidad
de la reacciůn de PCR. El fenotipo agregativo se observů en 17 de las 32 muestras
portadoras de los genes; en general las cepas EAST1 positivas fueron las que
carecŪan de dicho fenotipo.
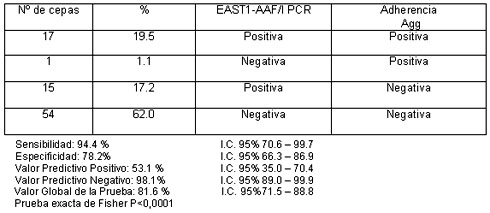
Tabla 3. Comparaciůn de los resultados de PCR para AAF/I/EAST 1 PCR y del patrůn de adherencia
agregativa en el ensayo en cťlulas HEp-2.
Discusiůn
Escherichia coli diarreigťnica (DEC) representa un blanco elusivo a la
hora del diagnůstico debido a que no resulta fŠcilmente distinguible de las cepas
que no portan factores de virulencia y que son habitantes normales del intestino
humano y de los animales.
En el primer trabajo realizado por nuestro grupo,25 se detectů 21%
de cepas EAEC, clasificadas sobre la base de su patrůn de adherencia. Esto
despertů un interťs especial por investigar la distribuciůn y relaciůn epidemiolůgica
de estas cepas en nuestra comunidad. Con el propůsito de desarrollar una
metodologŪa rŠpida, sensible y especŪfica que permitiera el estudio de un nķmero
considerable de cepas, se desarrollaron dos tipos de PCR, aplicables al diagnůstico
de EAEC. Se utilizaron primers descritos y probados por otros autores,
para identificar AAF/I y EAST1.27
Una de las desventajas de PCR como mťtodo de diagnůstico lo constituye el hecho
de que la observaciůn de la banda del producto de amplificaciůn otorga informaciůn
sobre el tamaŮo de una molťcula de ADN, pero no sobre su secuencia. Por ello es
que si se utiliza esta reacciůn como mťtodo de diagnůstico ķnico, deberŪa
acompaŮarse de un sistema que permita corroborar que el amplificado corresponde
a la secuencia esperada. Existen diferentes metodologŪas disponibles; una de ellas
es la de buscar un sitio de corte para alguna enzima de restricciůn dentro del sector
amplificado que permita distinguir dos fragmentos de tamaŮo conocido. Para el
caso de la PCR para AAF/I, los autores describieron un sitio de corte para la enzima
AluI, que fragmentaba el amplificado de 639 bp en dos partes de 391 bp y
239 bp. Para el amplificado del gen astA, para el cual no se habŪa descrito
ningķn sistema de confirmaciůn, se realizů una bķsqueda con el programa PCgene,
detectando un sitio diana para HhaI. Los resultados de las digestiones
enzimŠticas se muestran en la figura 3.
Para poder establecer la utilidad de PCR en el diagnůstico de EAEC se compararon
los resultados con los obtenidos por la prueba de referencia (ensayo de adherencia
en cťlulas HEp-2). En la figura 4 se observa la distribuciůn de los patrones de
adherencia. El patrůn agregativo apareciů, al igual que en el primer trabajo de
Ortiz,25 en 21% de las cepas. Si se refieren estos resultados a los
datos sobre los diferentes patůgenos aislados de coprocultivos en el Hospital Notti,
presentados en la Introducciůn, se observa que durante 1995 y 1996, perŪodo
durante el cual se realizů este trabajo, el porcentaje de EPEC fue del 20% en
promedio. De las 87 cepas estudiadas, 20% correspondieron a la categorŪa EAEC
clasificada sobre la base de la prueba de adherencia. Si se proyecta este dato al
total de patůgenos aislados durante los dos aŮos de estudio, EAEC tendrŪa una
prevalencia similar a la de Salmonella, que es aproximadamente del 3%,
lo cual permite postular la importancia de caracterizar las cepas de E. coli
por sus factores de patogenicidad, lo que a su vez podrŪa tener impacto
considerable en el conocimiento de la etiologŪa de los casos esporŠdicos de
diarrea.
En la tabla 1 se comparan los resultados entre PCR para AAF/I y el patrůn
agregativo, obteniťndose una sensibilidad del 44%. Se observa que 8 de las 18
cepas que presentaron el fenotipo agregativo eran portadoras de la fimbria I; las 10
cepas que presentaron adherencia agregativa pero fueron negativas para AAF/I, lo
que parece indicar que otros factores, fimbriales o no, podrŪan estar involucrados
en la adherencia. Cinco cepas, de las 13 que fueron positivas para AAF/I
presentaron un patrůn diferente al agregativo. Estos resultados podrŪan explicarse,
por un lado, por la subjetividad del ensayo de adherencia en cťlulas, y por otro, por
el requerimiento de otros factores, ademŠs de la presencia del gen estructural de la
fimbria, para que se produzca la adherencia.
En la tabla 2 se muestra la comparaciůn entre PCR para astA (proteŪna
EAST1) y el patrůn agregativo. Quince por ciento de las cepas resultaron portadoras
del gen astA y presentaron el patrůn agregativo, mientras que 6%
presentaron el patrůn agregativo pero no el gen astA. La prueba resultů
con una sensibilidad del 72%, considerablemente mayor que la demostrada por
AAF/I, reduciťndose la especificidad del 92.7% al 82.61%.
Se observa, ademŠs, que 13.7% de las cepas estudiadas fueron positivas para
astA y no presentaron adherencia agregativa. Existen evidencias, descritas
por diferentes autores, de que el gen astA tendrŪa una distribuciůn amplia
entre las cepas de E. coli diarreigťnicas, no encontrŠndose restringido sůlo
a EAEC. De hecho, fue hallado en DAEC y EPEC,28 en
ETEC20 y en EHEC,29-31 razůn por la cual fue
incluido como posible Escherichia coli diarreigťnica
(DEC).32
Para el diseŮo de la tabla 3 se utilizů como criterio considerar positivas las cepas
portadoras de AAF/I, de astA, o de ambos (prueba en paralelo). De este
modo se observa que el porcentaje de cepas clasificadas como positivas por ambas
pruebas es de 19.5%, bastante cercano al valor observado para el patrůn de
adherencia agregativa en la figura 4. La sensibilidad de la prueba fue 94.4% y la
especificidad 78.2%. El valor global, es decir la posibilidad de que la cepa sea
clasificada correctamente por la prueba, es de 81.6%.
Estos datos sugieren que la detecciůn de ambos genes es la que otorga mayor
utilidad a la prueba, por lo que se postula su empleo como mťtodo de tamizaje,
limitando el empleo del ensayo de adherencia, mŠs costoso y laborioso, a aquellas
cepas portadoras de los genes.27
Conclusiůn
La implementaciůn de tťcnicas que detectan factores de patogenicidad
especŪficos permitiů identificar EAEC en los coprocultivos de la poblaciůn infantil
estudiada, pone en evidencia la heterogeneidad que presentan las cepas
pertenecientes a esta categorŪa de E. coli diarreigťnicas y demuestra la
necesidad de mťtodos de diagnůstico complementarios a los que rutinariamente se
utilizan en los laboratorios bacteriolůgicos. La prevalencia estimada para EAEC fue
de 3%; si la bķsqueda se ampliara, realizŠndose en forma independiente del
serogrupo, este porcentaje podrŪa ser mayor. Teniendo en cuenta la importancia de
EAEC como patůgeno emergente se sugiere la implementaciůn del diagnůstico
diferencial por PCR y su posterior confirmaciůn por el mťtodo de referencia.
Los autores no manifiestan conflictos.
BIBLIOGRAFÕA
-
Nataro JP and Kaper JB. Diarrheagenic Escherichia coli. Clin.
Microbiol.Rev. 1998. 11: 142-201.
-
Gomes TA, Vieria MA, Abe CM y col. Adherence patterns and adherence-related
DNA sequences in Escherichia coli isolates from children with and without
diarrhea in Sao Paulo city, Brazil. J. Clin. Microbiol. 1998. 36: 3609-13.
-
Gilligan PH. Escherichia coli EAEC, EHEC; EIEC, ETEC. Clin. Lab.
Med.1999. 19(3):505-21.
-
Gioppo NM, ElŪas WP Jr, Vidotto MC y col. Prevalence of HEp-2 cell adherent
Escherichia coli and characterisation of enteroaggregative E. coli
and chain-like adherent E. coli isolated from children with and without
diarrhoea, in Londrina, Brazil. 2000. FEMS Microbiol Lett 190:293-8.
-
Levine MM, Bergquist EJ, Nalin DR y col. Escherichia coli strains that
cause diarrhoea but do not produce heat-labile or heat-stable enterotoxins and are
non-invasive. Lancet 1978. i:1119Ė1122.
-
Vial PA, Robins Browne R, Lior H y col. Characterization of enteroadherent-
aggregative Escherichia coli, a putative agent of diarrheal disease. J.
Infect. Dis.1988. 158:70Ė79.
-
Okeke IN y Nataro JP. Enteroaggregative Escherichia coli. The Lancet
Inf. Dis. 2001. 1: 304-13.
-
Rich Ch, Favre-Bonte S, Sapena F y col. Characterization of Enteroaggregative
Escherichia coli Isolates. FEMS Microbiol. Lett.1999. 173:55-61.
-
Hicks S, Candy DCA y Phillips AD. Adhesion of Enteroaggregative
Escherichia coli to pediatric intestinal mucosa In Vitro. Am. Soc.
Microb.1996. 64:4751-4760.
-
Knutton S, Shaw RK, Bhan MK y col. Ability of enteroaggregative
Escherichia coli strains to adhere in vitro to human intestinal
mucosa.Infect. Immun. 1992. 60:2083Ė2091.
-
Nataro JP, Steiner T y Guerrant RL. Enteroaggregative Escherichia coli.
Em. Infect. Dis. 1998. 4:251-261.
-
Czeczulin JR, Balepur S, Hicks S y col. Aggregative Adherence Fimbria II, a
second fimbrial antigen mediating aggregative adherence in Enteroaggregative
Escherichia coli. Am.Soc.Microb.1991. 65: 4135-4145.
-
Czeczulin JR, Whittam TS, Henderson IR y col. Phylogenetic analysis of EAEC
and diffusely adherent Escherichia coli. Infect. Immun. 1999. 67(6):2692-
9.
-
Savarino SJ, Fasano A, Robertson DC y col. Enteroaggregative Escherichia
coli elaborate a Heat-Stable Enterotoxin demonstrable in an In Vitro rabbit
intestinal model. J. Clin. Invest.1991. 87:1450Ė1455.
-
Savarino SJ, Fasano A, Watson J y col. Enteroaggregative Escherichia
coli Heat-Stable Enterotoxin 1 represents another subfamily of E. coli
Heat-Stable toxin. Proc. Natl. Acad. Sci. USA.1993. 90:3093Ė3097.
-
Zhou Z, Ogasawara J, Nishikawa Y y col. An outbreak of gastroenteritis in
Osaka, Japan due to Escherichia coli serogroup O166:H15 that had a
coding gene for enteroaggregative E. coli Heat-Stable Enterotoxin 1
(EAST1). Epidemiol. Infect. 2002. 128(3):363-71.
-
Eslava C, Navarro-GarcŪa F, Czeczulin JR y col. Pet, an autotransporter
enterotoxin from enteroaggregative Escherichia coli. Infect. Immun.1998.
66:3155-63.
-
Henderson IR, Hicks S, Navarro-GarcŪa F y col. Involvement of the
enteroaggregative Escherichia coli plasmid-encoded toxin in intestinal
damage. Infect. Immun. 1999. 67 (10): 5338-44.
-
Benjamin P, Federman M y Wanke C A. Characterization of an invasive
phenotype associated with enteroaggregative Escherichia coli. Infect.
Immun.1995. 63:3417Ė3421.
-
Yamamoto T Echeverria P y Yokota T. Drug resistance and adherence to human
intestines of enteroaggregative Escherichia coli. J. Infect.Dis. 1992.
165:744Ė749.
-
Cobeljic M, Miljkovic-Selimovic B, Paunovic-Todosijevic D y col.
Enteroaggregative Escherichia coli associated with an outbreak of
diarrhoea in a neonatal nursery ward. 1996. Epidemiol. Infect. 117:11Ė 16.
-
Eslava C, Villaseca J, Morales R y col. Identification of a protein with toxigenic
activity produced by Enteroaggregative Escherichia coli, abstr. B-105, p.
44. In Abstracts of the 93rd General Meeting of the American Society for
Microbiology 1993. American Society for Microbiology, Washington, D.C.
-
Baudry B, Savarino SJ, Vial P y col. A sensitive and specific DNA probe to
identify enteroaggregative Escherichia coli, a recently discovered diarrheal
pathogen. J. Infect. Dis.1990. 161:1249Ė1251.
-
Debroy C, Bright BD, Wilson RA y col. Plasmid-coded DNA fragment developed
as a specific gene probe for the identification of enteroaggregative Escherichia
coli . J. Med. Microbiol.1994. 41: 393-8.
-
Ortiz A, RŁttler M, GarcŪa B y col. Acumulaciůn de actina y adherencia a cťlulas
HEp-2 de cepas de Escherichia coli aisladas de niŮos con diarrea en
Mendoza, Argentina. Rev. Arg. Microbiol. 1998. 30:13 -19.
-
Schmidt H, Knop C, Franke S y col. Development of PCR for screening of
enteroaggregative Escherichia coli. J. Clin. Microbiol. 1995. 33: 701-5.
-
RŁttler ME, Renna NF, Ortiz A y col. Characterization of enteroaggregative
Escherichia coli strains isolated from children with acute diarrhea, in
Mendoza, Argentina. Rev. Arg. Microbiol.2002. 34: 167-170.
-
Yamamoto T y Nakazawa. Comparison of the nucleotide sequence of
enteroaggregative E. coli heat-stable enterotoxin 1 genes among diarrhea
associated E. coli. FEMS Microbiol. Lett.1997. 147: 89-95
-
Yamamoto I, Taneike I. The sequences of enterohemorraghic Escherichia
coli and Yersinia pestis that are homologous to the enteroaggregative
Escherichia coli heat-stable enterotoxin gene: cross-species transfer in
evolution. FEBS Lett 2000. 472(1): 22-6.
-
Lai XH, Wang SY y Uhlin BE. Expression of cytotoxicity by potential pathogens
in the standard Escherichia coli Collection of Reference (ECOR) strains.
Microbiol.1999. 145:3295-3303.
-
Yatsuyanagi J, Saito S, Miyajima Y y col. Characterization of atypical
enteropathogenic Escherichia coli strains harboring the astA gene
that were associated with a waterborne outbreak of diarrhea in Japan.J.Clin.
Microbiol.2003. 41: 2033-9.
-
Nishikawa Y, Zhou Z, Hase A y col. Diarrheagenic Escherichia coli
isolated from stools of esporadic cases of diarrheal ilness in Osaka City, Japan
between 1997 and 2000: Prevalence of Enteroaggregative E. coli Heat-
Stable Enterotoxin 1 Gene-Possessing E. coli. Jpn. J. Infect. Dis. 2002.
55(6):183-90.
|


![]()

