Introducción
Las hormonas tiroideas regulan el crecimiento lineal y el desarrollo del esqueleto
(1,2). El hipotiroidismo en la nińez dańa la osificación endocondral, llevando al
retraso completo de crecimiento y a edad ósea retardada; las anomalías revierten
mediante tratamiento de reemplazo (3) con tiroxina (T4). Por otro lado, la
tirotoxicosis en la nińez conduce al crecimiento acelerado, a edad ósea avanzada y
a baja estatura por causa del cierre prematuro del cartílago de crecimiento. En
casos severos, la craniostosis es el resultado del cierre prematuro de las suturas del
cráneo (4). En adultos, la tirotoxicosis es un riesgo establecido para pérdida ósea
acelerada y fracturas osteoporóticas (5-7). Estudios recientes sugieren que la
supresión de tirotrofina (TSH), sea debido a exceso de T4 endógeno o exógeno, es
un factor de riesgo para fracturas osteoporóticas en mujeres posmenopáusicas,
aunque la densidad mineral ósea (DMO) en este grupo de pacientes no aparece
disminuida (8,9). De este modo, las hormonas tiroideas parecen tener efectos
deletéreos sobre la calidad del hueso que no son cuantificados por técnicas
convencionales de densitometría ósea. A pesar de estas observaciones, la
investigación de la acción de la hormona tiroidea (3,5,3´-triiodotironina, T3) en
hueso es relativamente poco comprendida. En un estudio reciente, identificamos
que el número y la distribución de los mastocitos de la médula ósea se afectan por
el estado tiroideo en vivo (10). En el trabajo se resumen estos hallazgos, se
describen nuestros estudios recientes acerca del papel de la T3 sobre el desarrollo
del esqueleto y se comentan cómo los mastocitos han sido involucrados en la
regulación de la formación de hueso y el mantenimiento de la masa ósea.
Mastocitos de la médula ósea y estado tiroideo
Examinamos la metáfisis, los centros primarios esponjosos y de osificación en
cuatro grupos de ratas de 12 semanas de vida que habían sido tratadas durante las
6 semanas precedentes (10). Los mastocitos se identificaron a través de
histoquímica e inmunomarcación a lo largo de la médula ósea de todos los
animales. No se observó ninguna diferencia en el número y la distribución de los
mastocitos en animales con tirotoxicosis o hipotiroidismo tratado mediante
reemplazo de T4, comparados con controles eutiroideos, pero hubo elevado número
de mastocitos que se localizaron en las adyacencias de las metáfisis en ratas
hipotiroideas. También se halló en los mastocitos de la médula ósea la expresión de
receptores de hormona tiroidea (RT) proteínas α1, α2 y β1, lo cual
parece indicar que pueden ser capaces de responder directamente a la T3 (10).
żCuál es el significado de esta nueva observación?
En un estudio previo (11), se demostró que el hipotiroidismo causaba disfunción de
la osificación endocondral, la cual fue asociada con una alteración del ciclo de
retroalimentación en la expresión de los componentes del péptido relacionado con
el erizo de la India / con la parathormona (Prei/PTH) (12,13), sugiriendo que los
pasos de la proliferación de los condrocitos de la metáfisis y de la diferenciación
durante la formación de hueso son sensibles al estado tiroideo in vivo. La
metáfisis en el hipotiroidismo estaba totalmente desorganizada, contenía una
matriz anormal rica en proteoglucanos de heparán sulfato (HSPG) y diferenciación
condrocítica hipertrófica con falla de progresión. Además, la estructura trabecular
del hueso en ratas hipotiroideas estaba desorganizada y existían indicios de
disfunción en la angiogénesis de la metáfisis (11). La localización del elevado
número de mastocitos que mostraban expresión de RT en el tejido óseo esponjoso
primario en el hipotiroidismo, el sitio de la disfunción de la angiogénesis, sugiere la
participación del mastocito de la médula ósea en la regulación de la formación de
nuevos vasos sanguíneos durante la osificación endocondral dependiente de T3.
Hormonas tiroideas y desarrollo esquelético en ratones modificados
genéticamente
En estudios ulteriores, hemos investigado el papel de las hormonas tiroideas en el
desarrollo esquelético en ratones genéticamente modificados. Los ratones
RTα0/0, que carecen de todas las proteínas RTα expresadas en
el locus THRA, son eutiroideos y tienen expresión normal de la hormona hipofisaria
de crecimiento. Sin embargo, los ratones RTα0/0 muestran retardo
de crecimiento, osificación endocondral retardada y disfunción de la mineralización
esquelética con depósito anormal de matriz en la metáfisis [(14) y datos nuestros
no publicados]. La expresión y la actividad del recién identificado gen blanco de T3,
el receptor-1 del factor de crecimiento fibroblástico (fibroblastic growth factor
receptor-1, FGFR1), se encuentran reducidas en los RTα0/0
indicando que estos ratones muestran hipotiroidismo esquelético (15). También
hemos examinado la formación de hueso en ratones con resistencia a mutaciones
de hormona tiroidea (RHT) dirigidas a los genes THRA o THRB.
La RHT es una condición autosómica dominante consecuencia de mutaciones en el
gen THRB. La proteína mutante RTβ actúa como un represor dominante
negativo de RT de tipo salvaje (16). La condición se caracteriza por un complejo
fenotipo en el cual algunos tejidos (por ejemplo, hipófisis e hígado) muestran
manifestaciones de hipotiroidismo mientras otros (corazón), de tirotoxicosis. En el
hueso, el estado tiroideo no ha sido completamente evaluado (16,17). Analizamos
el desarrollo esquelético en ratones con mutaciones de la RHT, PV, dirigidos al gen
THRB por recombinación homóloga (18). Estos ratones presentaban RHT grave, con
niveles de T3, T4 y TSH marcadamente elevados (19). Los ratones homocigotas
RTβPV mostraron baja estatura con indicios paradójicos de
formación ósea avanzada. El crecimiento fue acelerado intraútero, pero disminuyó
en el período posnatal debido a la quiescencia de las metáfisis. Los ratones
RTβPVtambién mostraron formación ósea avanzada endocondral e
intramembranosa con incremento de la mineralización, aumento de la expresión de
FGFR1 y craniostosis (18). Estas son manifestaciones de tirotoxicosis juvenil (4).
Para aclarar el mecanismo de este fenotipo no usual, también caracterizamos a los
ratones RTα1PV, que alberga la misma mutación PV dirigida al gen
THRA (20). La mutación homocigota es letal, pero los ratones heterocigotas
RTα1PV/+ presentan retardo de crecimiento grave con desarrollo
esquelético marcadamente retardado y disfunción de la formación ósea cortical
(datos nuestros no publicados) en asociación con hormonas tiroideas circulantes
normales. Así, una mutación RTβ que causa RHT grave da como resultado
tirotoxicosis esquelética, mientras que la misma mutación en RTα1 causa
hipotiroidismo esquelético. Además demostramos que RTα1 se expresa 10 a
12 veces más en el hueso que RTβ (18) y estos hallazgos nos han llevado a
proponer que los diferentes fenotipos esqueléticos en ratones
RTα1PV y RTβPV resultan a partir de la diferente
expresión de RTα en el hueso (figura 1).
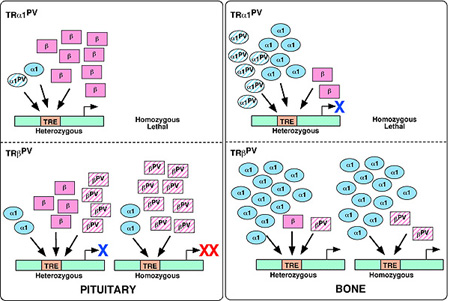
Figura 1. Mecanismo propuesto de fenotipos esqueléticos
divergentes en ratones RTα1PV y RTβPV.
Se muestran los efectos de las mutaciones
RTα1PV (paneles superiores) y RTβPV
(paneles inferiores) en la hipófisis (izquierda) y en el hueso (derecha). Los
receptores tiroideos se unen a los elementos de la respuesta T3 (TRE) en los
promotores de los genes blanco de T3 para activar la transcripción (flechas).
Las X muestran la inhibición de las respuestas dependientes de T3 por el RT
mutante PV. En la hipófisis del ratón RTα1PV/+, un órgano
en el cual predomina la expresión RTβ, los bajos niveles de la proteína
mutante RTα1PV no puede interferir eficientemente con
las acciones de RTβ con el resultado de que la hipófisis es eutiroidea y
estos ratones tienen niveles circulantes normales de hormonas tiroideas
(20). En contraste, en el esqueleto del ratón RTα1PV/+, un
tejido que expresa RTα, altos niveles relativos de
RTα1PV mutante interfieren con la función del RT de tipo
salvaje, dando como resultado un fenotipo hipotiroideo grave de retraso de
crecimiento y de osificación retardada. En los ratones homocigotas RTβ
PV/PV, por el contrario, elevados niveles de
RTβPV mutante en la hipófisis desorganizan eficientemente
proteínas seńalizadoras de RT de tipo salvaje y la hipófisis es fuertemente
resistente a las hormonas tiroideas, como lo refleja el aumento de 400 veces
de la TSH y 10 a 15 veces de T3 y T4 circulantes en estos ratones (19). En
el hueso, un tejido RTα, la situación es diferente. Los bajos niveles de
RTβPV mutante no pueden interferir con las proteínas de
RTα de tipo salvaje, las cuales son activadas por elevados niveles
circulantes de hormona tiroidea y el esqueleto muestra un fenotipo
tirotóxico. El fenotipo intermedio de los ratones heterocigotas
RTβ1PV/+ (18), que presenta sólo elevaciones de 2 a 3
veces de T4 y T3, es congruente con esta hipótesis, indicando que la
proporción relativa de RTα y β controla la respuesta T3
específica de tejido en órganos blanco individuales (18,48). Estas
consideraciones, junto con la información de los ratones mutantes
[(14,15,18) y observaciones no publicadas] demuestran que RTα es
esencial para el desarrollo esquelético normal y la mineralización ósea.
Pituitary, hipófisis. Bone, hueso. Heterozigous,
heterocigota. Homozigous, homocigota. Homozigous lethal,
homocigota letal.
Osificación endocondral y remodelación ósea
La osificación endocondral es un proceso por el cual se alcanza el desarrollo
esquelético, el crecimiento lineal y la curación de fracturas (21). Depende de la
proliferación organizada y la diferenciación de los condrocitos metafisarios, los
cuales sintetizan y depositan una matriz de cartílago rica en colágeno X, HSPG y
diversas proteínas marcadoras seńalizadoras, citoquinas y factores de crecimiento
(figura 2). El depósito anormal de matriz cartilaginosa visto en el hipotiroidismo
(11), la sensibilidad del ciclo de retroalimentación Prei/PTH al estado tiroideo (11) y
la participación del FCF y HSPG marcando vías en las acciones de la T3 durante el
desarrollo esquelético (15,22) indican, en conjunto, que la matriz cartilaginosa es
un mediador crítico de las respuestas esqueléticas a las hormonas tiroideas. La
proximidad de un número elevado de mastocitos de la médula ósea adyacente al
tejido óseo esponjoso primario en el hipotiroidismo (10) sugiere que éstos pueden
influir en la acción de la hormona tiroidea durante la osificación endocondral. En los
adultos, la integridad esquelética es mantenida por la remodelación ósea (figura 2),
un proceso continuo en el cual el hueso es resorbido por los osteoclastos y
reemplazado por los osteoblastos (23,24). Las actividades de ambos tipos celulares
están firmemente vinculadas y el proceso es mantenido por osteoblastos y
osteoclastos, los cuales se comunican unos con otros a través de vías autocrinas y
paracrinas reguladas por hormonas sistémicas [incluyendo estrógenos y hormonas
tiroideas (22,25)] y por factores de crecimiento circulantes y citoquinas.
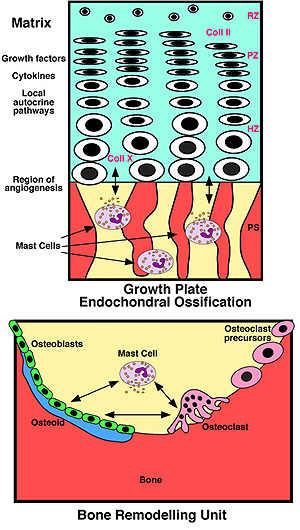
Figura 2. Osificación endocondral en la metáfisis y remodelación ósea
en el adulto. El crecimiento lineal ocurre a través de la osificación endocondral
en la metáfisis (izquierda). Los condrocitos de la zona de reserva (RZ ) sufren una
expansión clonal. Las células que proliferan secretan colágeno II (Coll II ) y se
organizan en columnas en la zona proliferativa (PZ ). Las células prehipertróficas se
diferencian y los condrocitos maduros en la zona hipertrófica (HZ ) finalmente sufren
apoptosis para dejar un andamio de matriz de colágeno X (Coll X ) que es
posteriormente degradada para facilitar la angiogénesis a partir del tejido óseo primario
esponjoso (PS ). La invasión de nuevos vasos sanguíneos permite a los osteoblastos
acceder al andamio de la matriz, liberar sustancia osteoide y mineralizar el hueso en
desarrollo. La coordinación de estos eventos es dirigida por una compleja matriz de
comunicaciones célula a célula y vías seńalizadoras autocrinas y paracrinas (21,22,23).
Estas vías afectan la matriz secretada, la cual participa del desarrollo de los contactos célula
a célula y de las redes locales seńalizadoras, así como actúan como reservorio para la
liberación de citoquinas y factores de crecimiento de acción local. Los mastocitos adyacentes
a la metáfisis en el hipotiroidismo se sitúan idealmente para influir en el proceso de la
osificación a través de la secreción de factores autocrinos adicionales. El ciclo de
remodelación (derecha) comienza con la activación de las células precursoras de
osteoclastos que se diferencian en osteoclastos maduros, los cuales entonces resorben el
hueso. Una vez alcanzada una cierta profundidad de resorción. Los osteoblastos invaden,
liberan sustancia osteoide y comienza la mineralización (22-24). La secuencia activación-
resorción-formación dura alrededor de 200 días y ocurre en sitios diferenciados
denominados unidades de remodelación ósea. Esta se lleva a cabo con diferentes índices en
el hueso trabecular y en el cortical y en diversas localizaciones anatómicas. El índice al cual
determinados sitios sufren remodelación es conocido como frecuencia de activación y es el
principal factor que determina el recambio óseo total. En el hipertiroidismo, los tiempos que
llevan la resorción ósea, el depósito de la matriz y la mineralización están acortados y la
frecuencia de activación está aumentada. Además, las actividades de los osteoclastos y los
osteoblastos están aumentadas y el ciclo de remodelación se reduce 50% (6). Estos
cambios son desproporcionados (las actividades de los osteoclastos y osteoblastos están
desacopladas, presumiblemente por alteración de las funciones de diferentes vía
seńalizadoras autocrinas) y conducen a un equilibrio negativo con pérdida de alrededor de
10% de hueso mineralizado por ciclo en el hipertiroidismo manifiesto. Los indicios
acumulados demuestran que los mastocitos pueden reunirse en regiones de remodelación
ósea activa, sugiriendo que pueden jugar un papel modulador en el mantenimiento de la
integridad esquelética.
Growth Plate Endochondral Ossification, osificación endocondral de la
metáfisis.
Matrix, matriz. Growth factors, factores de crecimiento. Cytokines,
citoquinas. Local autocrine pathways, vías locales autocrinas. Region of
angiogenesis, región de angiogénesis. Mast cells, mastocitos. Bone
Remodelling Unit, unidad de remodelación ósea. Osteoblasts, osteoblastos.
Osteoid, sustancia osteoide. Osteoclast, osteoclasto. Osteoclast
preccursors, precursores de osteoclastos.
Mastocitos
Los mastocitos sintetizan, almacenan y liberan un grupo de enzimas que degradan
la matriz extracelular, factores de crecimiento, citoquinas y moléculas de
seńalización (figura 3). Las enzimas que degradan la matriz extracelular y las
proteasas secretadas por los mastocitos incluyen triptasa, quimasas, proteasas
neutrales, serinproteasas, hidrolasas ácidas, catepsinas, metaloproteinasa-2 de
matriz (MPM-2; gelatinasa A) y MPM-9 (gelatinasa B) (26,27). La actividad de MPM-
1 (colagenasa intersticial), la cual es secretada por osteoblastos y condrocitos, es
activada por quimasa de los mastocitos y es dependiente de la heparina. Además
de las proteasas, los mastocitos secretan numerosas citoquinas pro-angiogénicas y
factores de crecimiento incluyendo FGF2, factor de crecimiento vascular endotelial
(VEGF), factor β de crecimiento transformante (TGFβ), factor ? de necrosis
tumoral (TNFα), leucotrienos y prostaglandinas D2 (28). Los mastocitos
activados secretan un grupo adicional de citoquinas y factores de crecimiento, que
incluyen interleuquina-1 (IL-1), IL-3, IL-4, IL-5, IL-6, IL-13, TNFα y factor
estimulante de colonias de granulocitos y macrófagos (GM-CSF) (28,29). Varios de
estos factores secretados actúan promoviendo la formación y la actividad de los
osteoclastos (GM-CSF, IL-1, IL-3, IL-6, TNFα) o aumentando el número y la
actividad (25,30,31).
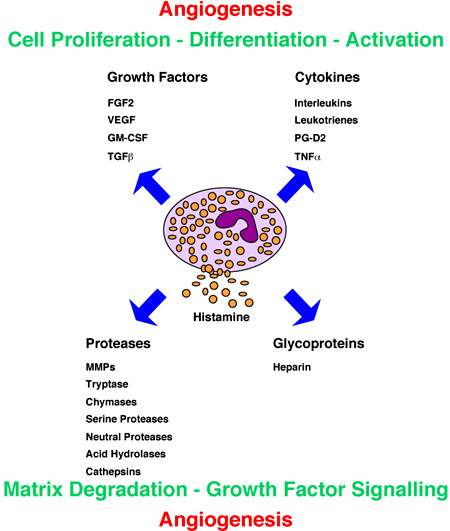
Figura 3. Los mastocitos secretan numerosos factores de crecimiento,
citoquinas, proteasas y glucoproteínas. Los mastocitos secretan un grupo de
factores que actúan localmente y regulan la proliferación, la diferenciación y la actividad
celular. Los mastocitos también secretan un amplio rango de proteasas que degradan la
matriz extracelular y facilitan la angiogénesis en una diversidad de tejidos (28).
Angiogenesis, angiogénesis. Cell Proliferation - Differentiation -
Activation, proliferación - diferenciación - activación celular. Growths
Factors, factores de crecimiento. FGF2, factor de crecimiento
fibroblástico. VEGF, factor de crecimiento endotelial vascular. GM-
CSF, factor de crecimiento de colonias de granulocitos y macrófagos.
TGFβ, factor de crecimiento transformante β.
Cytokines, citoquinas. Interleukins, interleuquinas.
Leukotrienes, leucotrienos. PG-D2, prostaglandinas D2.
TNFα, . Proteases, proteasas. MMPs,
metaloproteinasas de matriz. Tryptase, triptasa. Chymases,
quimasas. Serine Proteases, serinproteasas. Neutral
Proteases, proteasas neutrales. Acid Hydrolases, hidrolasas ácidas.
Cathepsins, catepsinas. Glycoproteins, glucoproteínas.
Heparin, heparina. Histamine, histamina. Matrix
Degradation - Growth Factor Signalling, matriz de degradación - factor de
crecimiento seńalizador.
żParticipan los mastocitos en la formación ósea?
Los mastocitos han sido firmemente involucrados en la angiogénesis en la médula
ósea y otros tejidos y pueden jugar un papel en la liberación de factores de
crecimiento, incluyendo FGF y citoquinas a partir de depósitos de la matriz
extracelular en donde están ligados a los HSPG (22,28,32,33). Así, se ha
demostrado que los mastocitos son importantes en la invasión de un tumor
maligno, en donde se acumulan en los márgenes de avance. De manera similar, en
la fibrodisplasia osificante progresiva, una alteración genética de osificación
progresiva heterotópica asociada con la producción no regulada de proteína 4 ósea
morfogenética, los mastocitos se encuentran en los márgenes de avance de
lesiones óseas maduras adyacentes a sitios de depósito de cartílagos (34). Los
procesos de la angiogénesis y las acciones de los mastocitos parecen ser
interdependientes. Por ejemplo, el FGF, que puede ser secretado por osteoblastos o
condrocitos o liberado a partir de la matriz metafisaria (32,33), induce
quimiomigración de los mastocitos a los sitios de neovascularización. Las proteasas
de los mastocitos degradan la matriz y los mismos mastocitos secretan factores
proangiogénicos (28). Además, los mastocitos y los condrocitos se comunican y los
mastocitos pueden regular la producción de proteoglucanos de los condrocitos y el
depósito de la matriz (35). Estas consideraciones indican que los mastocitos tienen
la oportunidad de regular la osificación endocondral y el desarrollo esquelético. Esto
representa un nuevo ámbito para futuras investigaciones.
Mastocitos y recambio óseo
Los mastocitos también han sido involucrados en la regulación del recambio óseo y
el mantenimiento de la masa ósea en los adultos. Producen y secretan la
glucoproteína heparina y la histamina monoamina básica. La heparina se une y
puede secuestrar a los FGF (22) y otros factores de crecimiento, y es indispensable
para la unión funcional de los FGF con los receptores de FGF (36). También
incrementa el número y la actividad de los osteoclastos e induce osteopenia
(37,38), probablemente, aumentando la resorción ósea. De modo similar, la
histamina ha sido involucrada en la aparición de osteopenia, bajo la hipótesis de
que los mastocitos actúan como factores accesorios para la resorción ósea (39). La
histamina se sintetiza en los mastocitos por decarboxilación de la histidina y se
almacena en los gránulos de los lisosomas. La supresión de la histidina
decarboxilasa (HDC) en ratones HDC-/-lleva a niveles tisulares
indetectables de histamina y disminuye la degranulación mastocitaria (40). Los
ratones HDC-/- crecen normalmente aunque se observa en animales
mayores un incremento del grosor de la cortical femoral y del hueso trabecular
vertebral. Este fenotipo osteoporótico se asocia con la ausencia de osteoclastos
positivos para fosfatasa ácida resistente al tartrato (TRAP) en tejido óseo primario
esponjoso. Los ratones HDC-/- también presentan un incremento de la
síntesis renal de vitamina D, lo que puede mitigar la pérdida ósea en la deficiencia
de histamina. La mutación HDC-/- también protege contra la pérdida
ósea cortical y trabecular inducida por la ooforectomía a través de su efecto
combinado de aumentar la formación ósea y de reducir la resorción ósea (40). Los
estudios de Dobigny y Saffar han sugerido que la histamina ejerce su acción sobre
los osteoclastos a través de receptores de histamina H1 y H2 (39), aunque otros
han sugerido que los efectos de la histamina pueden ser indirectos. Sin embargo,
niveles elevados de histamina circulante han sido asociados con osteoporosis y
parámetros normales o disminuidos de formación ósea. Además, puede probarse
que los antagonistas de receptores de histamina son útiles para la prevención y el
tratamiento de la osteoporosis solos o en combinación con calcio y suplementos de
vitamina D (40,41).
En un modelo en ratas de resorción ósea sincronizada, los bloqueantes de
receptores H1 y H2 redujeron la pérdida ósea. La actividad de los bloqueantes H1
redujo la activación y la actividad osteoclásticas, mientras que la de los bloqueantes
H2 redujeron el tamańo de la población de osteoclastos (39). A los 30 días de
seguimiento de ratas ooforectomizadas, cuando se estableció la osteopenia, los
mastocitos se acumularon en la médula ósea y se asociaron con un número elevado
de osteoclastos que mostraron marcada actividad. El aumento concomitante de
mastocitos y osteoclastos seńala su intervención en la pérdida ósea inducida en la
ooforectomía (42) y ello puede involucrar un efecto indirecto del mastocito sobre el
reclutamiento de la célula precursora de osteoclasto (43). Posteriores estudios de
este grupo (41), en los cuales las ratas ooforectomizadas fueron tratadas con
cimetidina, un antagonista del receptor H2, revelaron que ésta impedía
parcialmente la pérdida ósea en estas ratas, al evaluar cambios en el volumen,
número y grosor trabecular; y el aumento del número de osteoclastos trabeculares.
Los autores seńalaron que la histamina parece estar involucrada en la
osteoclastogénesis. Ellos fueron más lejos, al determinar que la PTH causaba rápida
liberación de histamina mastocitaria y aumentaba el número de osteoclastos en
ratas. Las observaciones sugieren que los mastocitos pueden estimular el
reclutamiento de osteoclastos en condiciones de recambio óseo aumentado (41),
una característica particular de la pérdida ósea inducida por tirotoxicosis (6). Un
reciente estudio del análisis de chips de ADN (microarray) (44) del
programa transcripcional durante la osteoclastogénesis inducida en células de
médula ósea de murina por el factor estimulante de colonias de macrófagos (M-
CSF) y el activador del receptor del ligando NFκB (RANKL) también reveló un
posible papel para la histamina en la función del osteoclasto. En estos estudios, el
M-CSF estimulaba potencialmente la diferenciación osteoclástica y la expresión del
activador del receptor de NFκB (RANK). La estimulación de células con
RANKL indujo la expresión de receptores de histamina H2. Estos datos indican que,
durante la diferenciación osteoclástica, la célula parece volverse sensible al RANKL,
desarrollándose sinergia entre el M-CSF y el RANKL (44). Parece que una respuesta
a la sinergia entre el M-CSF y el RANKL es la expresión de la inducción del receptor
H2, presumiblemente permitiendo a los osteoclastos comprometidos responder a la
histamina.
Indicios adicionales avalan que los mastocitos juegan un papel en el mantenimiento
de la masa ósea en el hombre. El 70% de los pacientes con mastocitosis sistémica,
una condición de proliferación anormal de la médula ósea y los mastocitos,
presenta lesiones osteolíticas y osteoescleróticas con osteoporosis manifiesta en el
tercio de los pacientes y el 16% , fracturas (45,46). Se han documentado elevado
recambio y remodelación del hueso en la mastocitosis sistémica y la osteoporosis
puede ser una característica presente en la mastocitosis restringida a la médula
ósea. Además, el número de mastocitos en la médula ósea puede incrementarse en
mujeres osteoporóticas posmenopáusicas. Los mastocitos también pueden jugar un
papel en la osteoporosis idiopática masculina. En un estudio con 48 pacientes en
esta condición, 9% de los hombres tenía infiltración de médula ósea por células
anormales, algunas de las cuales se ubicaban cerca de la superficie ósea. Los
niveles urinarios de N-metilhistamina se correlacionaban con el número de
mastocitos de la médula ósea y lo hacían en forma negativa con la DMO (47). Sin
embargo, la cantidad de mastocitos en la etiología de la osteoporosis permanece
marcadamente desconocida por varias razones. No se mide en forma rutinaria la
N-metilhistamina en pacientes con osteoporosis, no se les han realizado biopsias y,
aun si las biopsias fueran hechas, la tinción con azul de toluidina para identificar los
mastocitos no se lleva a cabo (47).
Conclusiones
En resumen, recientemente identificamos que un elevado número de mastocitos se
acumula en las adyacencias del cartílago de crecimiento metafisario en ratas
hipotiroideas. Estos hallazgos se asociaron con disgenesia del cartílago en
crecimiento, depósito anormal de matriz extracelular y defectos en la formación
ósea, la diferenciación hipertrófica condrocítica y la angiogénesis metafisaria
(10,11). Varios estudios recientes, que investigaron las relaciones funcionales entre
los mastocitos y la osificación endocondral o entre los mastocitos y la actividad de
los osteoclastos han involucrado al mastocito en la regulación del desarrollo
esquelético y la masa ósea. Estos hallazgos intrigantes sugieren que el mastocito
juega un papel que contribuye a la patogenia de la osteoporosis y abre un nuevo
campo de investigación para estudiar enlaces entre la biología del mastocito y la
homeostasis esquelética.
BIBLIOGRAFÍA
-
Reiter EO, Rosenfeld RG. 1998. Normal and aberrant growth. In Williams
textbook of endocrinology. J.D. Wilson, D.W. Foster, H.M. Kronenberg, and P.R.
Larsen, editors. W.B. Saunders Company, Philadelphia, PA. 1427-1507
-
Harvey CB, O'Shea PJ, Scott AJ, Robson H, Siebler T, Shalet SM, Samarut
J, Chassande O, Williams GR 2002 Molecular mechanisms of thyroid hormone
effects on bone growth and function. Mol Genet Metab 75:17-30
-
Rivkees SA, Bode HH, Crawford JD 1988 Long-term growth in juvenile
acquired hypothyroidism: the failure to achieve normal adult stature. N Engl J
Med 318:599-602
-
Segni M, Leonardi E, Mazzoncini B, Pucarelli I, Pasquino AM 1999 Special
features of Graves' disease in early childhood. Thyroid 9:871-877
-
Williams GR. 2002. Thyroid disease and osteoporosis. In The Oxford
Textbook of Endocrinology and Diabetes. J.A. Wass, S.M. Shalet, E. Gale, and
S.A. Amiel, editors. Oxford University Press, Oxford, UK. 677-683
-
Mosekilde L, Eriksen EF, Charles P 1990 Effects of thyroid hormones on
bone and mineral metabolism. Endocrinol Metab Clin North Am 19:35-63.
-
Greenspan SL, Greenspan FS 1999 The effect of thyroid hormones on
skeletal integrity. Ann Intern Med 130:750-758
-
Bauer DC, Nevitt MC, Ettinger B, Stone K 1997 Low thyrotropin levels are
not associated with bone loss in older women: a prospective study. J Clin
Endocrinol Metab 82:2931-2936.
-
Bauer DC, Ettinger B, Nevitt MC, Stone KL 2001 Risk for fracture in
women with low serum levels of thyroid-stimulating hormone. Ann Intern Med
134:561-568
-
Siebler T, Robson H, Bromley M, Stevens DA, Shalet SM, Williams GR 2002
Thyroid status affects number and localisation of thyroid hormone receptor
expressing mast cells in bone marrow. Bone 30:259-266
-
Stevens DA, Hasserjian RP, Robson H, Siebler T, Shalet SM, Williams GR
2000 Thyroid hormones regulate hypertrophic chondrocyte differentiation and
expression of parathyroid hormone-related peptide and its receptor during
endochondral bone formation. J Bone Miner Res 15:2431-2442
-
Vortkamp A, Lee K, Lanske B, Segre GV, Kronenberg HM, Tabin CJ 1996
Regulation of rate of cartilage differentiation by Indian hedgehog and PTH-
related protein. Science 273:613-622
-
Lanske B, Karaplis AC, Lee K, Luz A, Vortkamp A, Pirro A, Karperien M,
Defize LHK, Ho C, Mulligan RC, Abou-Samra AB, Juppner H, Segre GV, Kronenberg
HM 1996 PTH/PTHrP receptor in early development and Indian hedgehog-regulated
bone growth. Science 273:663-666
-
Gauthier K, Plateroti M, Harvey CB, Williams GR, Weiss RE, Refetoff S,
Willott JF, Sundin V, Roux JP, Malaval L, Hara M, Samarut J, Chassande O 2001
Genetic analysis reveals different functions for the products of the thyroid
hormone receptor alpha locus. Mol Cell Biol 21:4748-4760
-
Stevens DA, Harvey CB, Scott AJ, O'Shea PJ, Barnard JC, Williams AJ,
Brady G, Samarut J, Chassande O, Williams GR 2003 Thyroid hormone activates
fibroblast growth factor receptor-1 in bone. Mol Endocrinol 17:1751-1766
-
Weiss RE, Refetoff S 2000 Resistance to thyroid hormone. Rev Endocr
Metab Disord 1:97-108
-
Weiss RE, Refetoff S 1996 Effect of thyroid hormone on growth. Lessons
from the syndrome of resistance to thyroid hormone. Endocrinol Metab Clin
North Am 25:719-730
-
O'Shea PJ, Harvey CB, Suzuki H, Kaneshige M, Kaneshige K, Cheng S-y,
Williams GR 2003 A thyrotoxic skeletal phenotype of advanced bone formation in
mice with resistance to thyroid hormone. Mol Endocrinol 17:1410-1424
-
Kaneshige M, Kaneshige K, Zhu X, Dace A, Garrett L, Carter TA,
Kazlauskaite R, Pankratz DG, Wynshaw-Boris A, Refetoff S, Weintraub B,
Willingham MC, Barlow C, Cheng S 2000 Mice with a targeted mutation in the
thyroid hormone beta receptor gene exhibit impaired growth and resistance to
thyroid hormone. Proc Natl Acad Sci USA 97:13209-13214
-
Kaneshige M, Suzuki H, Kaneshige K, Cheng J, Wimbrow H, Barlow C,
Willingham MC, Cheng S-y 2001 A targeted dominant negative mutation of the
thyroid hormone alpha 1 receptor causes increased mortality, infertility and
dwarfism in mice. Proc Natl Acad Sci USA 98:15095-15100
-
Kronenberg HM 2003 Developmental regulation of the growth plate. Nature
423:332-336
-
Bassett JHD, Williams GR 2003 The molecular actions of thyroid hormone
in bone. Trends Endocrinol Metab 14:356-364
-
Boyle WJ, Simonet WS, Lacey DL 2003 Osteoclast differentiation and
activation. Nature 423:337-342
-
Harada S-i, Rodan GA 2003 Control of osteoblast function and regulation
of bone mass. Nature 423:349-355
-
Jilka RL 1998 Cytokines, bone remodeling, and estrogen deficiency: a
1998 update. Bone 23:75-81
-
Irani AA, Schechter NM, Craig SS, Deblois G, Schwartz LB 1986 Two types
of human mast cells that have distinct neutral protease compositions. Proc
Natl Acad Sci USA 83:4464-4468
-
Fang KC, Wolters PJ, Steinhoff M, Bidgol A, Blount JL, Caughey GH 1999
Mast cell expression of gelatinases A and B is regulated by kit ligand and
TGF-beta. J Immunol 162:5528-5535
-
Hiromatsu Y, Toda S 2003 Mast cells and angiogenesis. Microsc Res Tech
60:64-69
-
Schwartz LB, Austen KF 1984 Structure and function of the chemical
mediators of mast cells. Progr Allergy 134:271-321
-
Liggett W, Shevde N, Anklesaria P, Sohoni S, Greenberger J, Glowacki J
1993 Effects of macrophage colony-stimulating factor and granulocyte-
macrophage colony-stimulating factor on osteoclastic differentiation of
hematopoietic progenitor cells. Stem Cells 11:398-411
-
Jilka RL, Hangoc G, Girasole G, Passeri G, Williams DC, Abrams JS, Boyce
B, Broxmeyer H, Manolagas SC 1992 Increased osteoclast development after
estrogen loss: mediation by interleukin-6. Science 257:88-91
-
Ornitz DM 2000 FGFs, heparan sulfate and FGFRs: complex interactions
essential for development. Bioessays 22:108-112
-
Ornitz DM, Marie PJ 2002 FGF signaling pathways in endochondral and
intramembranous bone development and human genetic disease. Genes Dev 16:1446-
1465
-
Gannon FH, Glaser D, Caron R, Thompson LDR, Shore EM, Kaplan FS 2001
Mast cell involvement in fibrodysplasia ossificans progressiva. Hum Pathol
32:842-848
-
Stevens RL, Somerville LL, Sewell D, Swafford JR, Caulfield JP, Levi-
Schaffer F, Hubbard JR, Dayton ET 1992 Serosal mast cells maintain their
viability and promote the metabolism of cartilage proteoglycans when
cocultured with chondrocytes. Arth Rheum 35:325-335
-
Schlessinger J, Plotnikov AN, Ibrahimi OA, Eliseenkova AV, Yeh BK, Yayon
A, Linhardt RJ, Mohammadi M 2000 Crystal structure of a ternary FGF-FGFR-
heparin complex reveals a dual role for heparin in FGFR binding and
dimerization. Mol Cell 6:743-750
-
Muir JM, Hirsh J, Weitz JI, Andrew M, Young E, Shaughnessy SGA 1997
Histomorphometric comparison of the effects of heparin and low-molecular-
weight heparin on cancellous bone in rats. Blood 89:3236-3242
-
Chowdhury MH, Hamada C, Dempster DW 1992 Effects of heparin on
osteoclast activity. J Bone Miner Res 7:771-777
-
Dobigny C, Saffar J-L 1997 H1 and H2 histamine receptors modulate
osteoclastic resorption by different pathways: evidence obtained by using
receptor antagonists in a rat synchronized resorption model. J Cell Physiol
173:10-18
-
Fitzpatrick LA, Buzas E, Gagne TJ, Nagy A, Horvath C, Ferencz V, Mester
A, Kari B, Ruan M, Falus A, Barsony J 2003 Targeted deletion of histidine
decarboxylase gene in mice increases bone formation and protects against
ovariectomy-induced bone loss. Proc Natl Acad Sci USA 100:6027-6032
-
Lesclous P, Guez D, Saffar JL 2002 Short-term prevention of osteoclastic
resorption and osteopenia in ovariectomized rats treated with the H2 receptor
antagonist cimetidine. Bone 30:131-136
-
Lesclous P, Saffar JL 1999 Mast cells accumulate in rat bone marrow
after ovariectomy. Cells Tissues Organs 164:23-29
-
Lesclous P, Guez D, Saffar JL 2001 Time-course of mast cell accumulation
in rat bone marrow after ovariectomy. Calc Tiss Inter 68:297-303
-
Cappellen D, Luong-Nguyen N-H, Bongiovanni S, Grenet O, Wanke C, Susa M
2002 Transcriptional program of mouse osteoclast differentiation geverned by
the macrophage colony-stimulating factor and the ligand for the receptor
activator of NFkappaB. J Biol Chem 277:21971-21982
-
Johansson C, Roupe G, Lindstedt G, Mellstrom D 1996 Bone density, bone
markers and bone radiological features in mastocytosis. Age Ageing 25:1-7
-
Compston JE 2002 Bone marrow and bone: a functional unit. J Endocrinol
173:387-394
-
Brumsen C, Papapoulos SE, Lentjes EGWM, Kluin PM, Tamdy NAT 2002 A
potential role for the mast cell in the pathogenesis of idiopathic
osteoporosis in men. Bone 31:556-561
-
Zhang X-Y, Kaneshige M, Kamiya Y, Kaneshige K, McPhie P, Cheng S-Y 2002
Differential expression of thyroid hormone receptor isoforms dictates the
dominant negative activity of mutant beta receptor. Mol Endocrinol 16:2077-
2092)
|


![]()
