Introducción
Los beneficios clínicos de los antihistamínicos orales para el tratamiento de los
trastornos alérgicos fueron establecidos desde hace muchos ańos y actualmente se
consideran los agentes principales para el alivio de los síntomas asociados con estas
enfermedades. Sin embargo, los antihistamínicos clásicos de primera generación,
aunque eficaces en la terapia de los trastornos alérgicos, se asociaron con efectos
adversos no deseados, como sedación y deterioro de la función cognitiva, incluso
del rendimiento psicomotor, memoria y atención.1-2 Además, la
disminución cognitiva puede causar detrimento en las actividades de la vida diaria
tales como el rendimiento escolar y laboral, la capacidad para conducir y muchas de
las tareas diarias que requieren alto grado de concentración y alerta. Por ejemplo,
la alteración del sistema nervioso central (SNC) puede afectar la capacidad
individual para conducir u operar maquinarias, así como la productividad laboral o
escolar. La mayor incidencia de accidentes de tránsito y caídas en los ancianos se
asoció con la administración de agentes antihistamínicos.2-4 Se cree
que las acciones farmacológicas no deseadas de los antihistamínicos de primera
generación se deben a su falta de especificidad por el receptor H1 y
a su capacidad para cruzar la barrera hematoencefálica, así como a su bloqueo del
receptor H1 cerebral mediante agonismo inverso.
Los antihistamínicos de nueva generación están notablemente libres de efectos
adversos a nivel del SNC en las dosis terapéuticas recomendadas para el alivio
sintomático y el control de la urticaria y los trastornos alérgicos perennes.
Recientemente, escribimos un artículo en el cual seńalamos que el antihistamínico
de última generación fexofenadina, en dosis supraclínica de 360 mg estuvo exento
de efectos adversos según diversas pruebas psicométricas.5 Por el
contrario, hay indicios de que con dosis superiores a las terapéuticas recomendadas
de 10 mg de loratadina o 10 mg de cetirizina se producen reacciones
adversas.6-8
La penetración de un antihistamínico en el SNC puede determinarse objetivamente
por medio de pruebas psicométricas específicamente elaboradas y tomografía por
emisión de positrones (PET). En vista de las preocupaciones generales acerca del
cumplimiento excesivo del tratamiento y la posibilidad de efectos adversos a nivel
del SNC, analizamos los datos actualmente disponibles sobre las alteraciones
provocadas por los antihistamínicos, medidas objetivamente por medio de las
pruebas psicométricas y la ocupación del receptor H1
(H1RO) en el cerebro mediante los estudios por PET.
Pruebas psicométricas
La inclusión de un grupo placebo y un grupo control positivo son críticos para
la metodología y diseńo de pruebas psicométricas a fin de validar su sensibilidad. Es
más importante aun incorporar las variaciones de dosis supraclínicas de los
compuestos para examinar el impacto de los niveles plasmáticos incrementados de
drogas debido a sobredosis o al cumplimiento excesivo del tratamiento.
Las consecuencias psicofarmacológicas de un antihistamínico sobre el SNC pueden
determinarse mediante un conjunto de herramientas para la valoración objetiva de
la sedación y el deterioro.9 Entre las pruebas objetivas más
frecuentemente utilizadas se encuentran el umbral crítico de fusión de oscilación de
la luz (CFF), el tiempo de reacción para la elección (CRT), las tareas continuas de
rastreo (CTT) y la prueba de reacción de frenado en la ruta (BRT).
La reacción de despertar del SNC y, en particular, la capacidad para discriminar
“pedacitos” distintos de información sensorial pueden evaluarse objetivamente por
medio del CFF. La cantidad de información que el cerebro puede procesar con
respecto al tiempo se mide por medio de la discriminación de la titilación de la luz a
partir de la fusión y viceversa cuando se observa una serie de diodos emisores de
luz.5 Se demostró que esta prueba es sensible para medir cambios
en la función del SNC luego de la administración de compuestos psicoactivos tales
como antidepresivos, ansiolíticos, cafeína, hipnóticos, neurotrópicos,
antihistamínicos y agentes fitofarmacéuticos.10-11 Las drogas que
provocan cambios en la velocidad psicomotora pueden medirse mediante CRT,
donde a partir de una posición central de inicio, los individuos deben apagar una de
seis luces encendidas al azar, al tocar el botón de respuesta apropiado. Con la
utilización de este esquema es posible medir los tres componentes del tiempo de
reacción: el tiempo de reacción total (TRT) desde el comienzo del estímulo hasta la
terminación de la respuesta; el tiempo de reacción motora (MRT), el tiempo que
toma mover el dedo entre el inicio y los botones de respuesta y el tiempo de
reacción de reconocimiento o de procesamiento (RRT) obtenido por la sustracción
del MRT al TRT.9 El tercer método de valoración, CTT, es una tarea
interactiva confiable y sensible de la función sensoriomotora que implica el rastreo
de una flecha en movimiento sobre una unidad de pantalla visual (VDU). La prueba
también incluye una medida de atención dividida del tiempo de reacción
periférica.5 Finalmente, pruebas como conducir un vehículo en la
ruta pueden brindar información extremadamente útil sobre el impacto día tras día
de diversos agentes sobre el SNC. El tiempo de reacción de frenado de un vehículo
en la ruta es una medida de algunas de las funciones cognitivas y psicomotoras
involucradas en el manejo de un automóvil, como la eficacia de la atención. Se
mide el tiempo requerido por una persona para pisar el pedal de freno en respuesta
a una luz encendida al azar en el techo del auto, la cual simula la luz de freno del
vehículo que va delante.
Recientemente demostramos que la fexofenadina, en dosis supraclínica de 360 mg,
estuvo exenta de efectos adversos sobre el SNC.5 A esta conclusión
se llegó en un estudio a doble ciego, controlado con placebo, en el cual los efectos
agudos del clorhidrato de fexofenadina a 360 mg sobre diversos aspectos de la
función psicomotora y cognitiva se compararon con los producidos por el placebo y
un control positivo con 30 mg de prometazina en 14 voluntarios
sanos.5 La fexofenadina no se distinguió del placebo en ninguna de
las pruebas subjetivas y objetivas hasta 7 horas después de su administración. De
acuerdo con lo esperado, todas las mediciones fueron peores luego de la
administración de prometazina, lo que confirma la sensibilidad del conjunto de las
pruebas. La prometazina produjo una reducción global en los umbrales de CFF en
comparación con el placebo (p < 0.05) y hubo un incremento global significativo en
RRT, MRT y TRT (p < 0.05), índices de alteraciones en el SNC. Tanto la exactitud
del rastreo como los aspectos del tiempo de reacción de CTT empeoraron
significativamente (p < 0.05) luego de la administración de prometazina.
Concluimos que el clorhidrato de fexofenadina a 360 mg estuvo exento de efectos
adversos sobre el SNC en dosis de hasta tres veces las comúnmente usadas para la
rinitis alérgica estacional (RAE) y del doble de las utilizadas para la urticaria
idiopática crónica (UIC). En Europa se recomiendan dosis diarias de clorhidrato de
fexofenadina de 120 mg y 180 mg para RAE y UIC, respectivamente.
Metaanálisis
Recientemente se llevaron a cabo dos metaanálisis para valorar los efectos
sedantes, psicomotores y cognitivos de los antihistamínicos.12,13 Se
incluyeron en estos metaanálisis solamente los datos provenientes de estudios con
un diseńo de tipo doble ciego, controlados con placebo y un control positivo
realizados en voluntarios sanos y publicados entre 1965 y 2000. Esto fue necesario
para asegurar que sólo se analizasen las mediciones lo suficientemente sensibles
como para valorar el impacto de los antihistamínicos.12,13
A fin de comparar los diferentes antihistamínicos se ideó un índice
empeoramiento/no empeoramiento (E/NE) para determinar las alteraciones
inducidas por drogas; el número de mediciones objetivas que demostraron
deterioro se compararon con un número similar de valoraciones de los mismos
estudios que no demostraron disminución de las funciones del
SNC.12 Los hallazgos del primer metaanálisis demostraron que los
antihistamínicos de nueva generación ofrecieron un perfil de seguridad más
favorable, con menos sedación y alteraciones de las funciones del SNC que sus
predecesores. Sin embargo, no todos estos antihistamínicos estuvieron
completamente exentos de acciones a nivel del SNC. Cuando se categorizaron los
efectos de los antihistamínicos sobre el SNC, los de primera generación como la
difenhidramina, tuvieron un índice que tendía a infinito, ya que todas las pruebas
psicométricas de las bases de datos demostraron las alteraciones producidas por
estas drogas. Los antihistamínicos de nueva generación mostraron más instancias
de no deterioro; sus índices E/NE fueron más bajos, aunque hubo un alto grado de
variabilidad entre estos agentes. Por ejemplo, el índice para cetirizina fue 0.17 y
para loratadina 0.36. Por el contrario, el clorhidrato de fexofenadina a 80 a 240 mg
tuvo un cociente de 0 para el deterioro cognitivo, ya que ninguna de las pruebas
psicométricas utilizadas con esta droga detectó alteraciones cuantificables.
El segundo metaanálisis determinó el índice de deterioro proporcional (PIR) para
cada antihistamínico; de modo que comparó las alteraciones producidas por un
antihistamínico individual con las provocadas por cada uno de los otros
antihistamínicos para los cuales hubo datos disponibles.13 Los
cálculos del PIR demostraron que los antihistamínicos de primera generación como
difenhidramina y prometazina, provocaron dos a tres veces más alteraciones en la
función del SNC que el promedio de la clase y avalaron los resultados del primer
metaanálisis. Si bien la loratadina y la cetirizina produjeron menos deterioro que el
promedio, éste aún se observó para algunas dosis. Por el contrario, no hubo
indicios de disminución en la función del SNC con fexofenadina en la bibliografía
examinada, aun con dosis tan altas como 360 mg.
Si bien los hallazgos de estos metaanálisis mostraron que tanto la cetirizina como la
loratadina tuvieron índices de empeoramiento más bajos respecto de los
antihistamínicos de primera generación, fue evidente que las alteraciones en la
función del SNC aumentaron en función de la dosis administrada. Esto constituye
una consideración importante en el caso de pacientes que utilizan una dosis mayor
a la prescrita, ya que en la bibliografía se informaron casos de cumplimiento
excesivo del tratamiento.14 Es más importante aun que muchos de
los antihistamínicos clásicos son actualmente de venta libre y, por ende, es difícil
controlar o monitorear la adhesión a la terapia.
Debido a que al momento de realizarse el metaanálisis descrito en este artículo no
había publicaciones disponibles sobre los antihistamínicos de nueva generación
desloratadina y levocetirizina, éstos no fueron incluidos. Más recientemente, se
publicaron datos que describieron la ausencia de alteraciones en el SNC con estos
dos agentes en las pruebas psicométricas.15,16 Sin embargo, estos
hallazgos deben interpretarse con precaución ya que sólo se investigaron los
efectos con las dosis recomendadas y también es necesario examinarlos con dosis
más altas, como se analizó en este artículo.
Indices de deterioro
A fin de comparar el porcentaje de H1RO, según los datos
derivados de los estudios de PET con aquellos obtenidos a partir de las pruebas
psicométricas, las valoraciones psicométricas analizadas en el metaanálisis fueron
convertidas a un valor porcentaje (cuanto mayor la alteración en la función del SNC
producida por el antihistamínico, mayor el porcentaje de índice de deterioro):

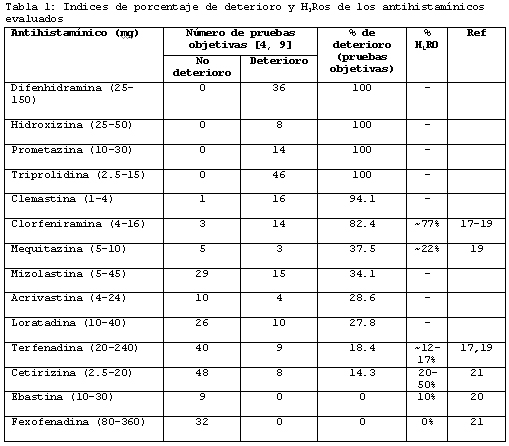
El porcentaje de índice de deterioro mostró que hubo diferencias desde el punto de
vista de la capacidad de los antihistamínicos para disminuir la función psicológica
(tabla 1). En esta comparación se incluyeron solamente los antihistamínicos que
fueron evaluados tanto en las pruebas psicométricas (metaanálisis) como en los
estudios de PET; no pudieron examinarse todos los antihistamínicos debido a que
los datos provenientes de las PET fueron limitados. Desde el punto de vista del
porcentaje de deterioro, los antihistamínicos de primera generación, como la
difenhidramina, se asociaron con más empeoramiento en la mayoría de las
pruebas, con puntajes entre 80% y 100%. Los antihistamínicos de nueva
generación, como cetirizina y loratadina se relacionaron con alteraciones en algunas
pruebas, generalmente con dosis más altas que las clínicamente recomendadas; sin
embargo, sus porcentajes de índice de deterioro fueron menores que los
observados con los agentes de primera generación. Por el contrario, la fexofenadina
y la ebastina no se asociaron con ninguna alteración en la función del SNC, con un
porcentaje de índice de deterioro de 0 (tabla 1).12,13
Ocupación de los receptores H1 en el cerebro mediante las
imágenes de PET
Además de las pruebas psicométricas, la capacidad de los antihistamínicos
para unirse a los receptores H1 cerebrales puede determinarse
mediante las imágenes obtenidas por PET. Por medio de esta técnica de imágenes,
la 11C-doxepina, un marcador radiactivo, puede utilizarse para
unirse a los receptores de histamina en el cerebro, lo que permite la visualización
del receptor durante el procedimiento. De este modo, la administración de un
antihistamínico que cruce la barrera hematoencefálica desplazará la
11C-doxepina y el receptor ya no podrá ser visualizado. Esto
equivale a la ocupación del receptor por el antihistamínico y seńala su penetración
en el cerebro.
Diversos estudios evaluaron la H1RO central con dosis únicas de
antihistamínicos en voluntarios sanos japoneses.17-21 En conjunto,
los hallazgos de estos estudios indican que los antihistamínicos de primera
generación, como es esperable, demostraron mayores tasas de ocupación en
comparación con los agentes de nueva generación (tabla 1).17-21
Con respecto a los antihistamínicos de nueva generación, Tashiro y col.
demostraron que la fexofenadina no ocupó los receptores H1 en la
corteza cerebral en comparación con la cetirizina, que produjo ocupación de estos
receptores entre 20% y 50% (p < 0.01) según la región cerebral.21
Además, diversos ensayos mostraron que la mequitazina, la terfenadina y la
cetirizina tienen tasas de ocupación de 12% a 50%17,19,21
comparadas con la clorfeniramina, que tiene una tasa de ocupación de
aproximadamente 77%.17,19 Es interesante destacar que no hay
pruebas de ocupación del receptor H1 cerebral por fexofenadina en
ninguno de los datos de PET disponibles actualmente (tabla 1).
Más recientemente se determinó el grado de lipofilia de seis antihistamínicos
(fexofenadina, loratadina, desloratadina, cetirizina, difenhidramina y
clorfeniramina) mediante la medición de sus coeficientes de
partición.22 Con excepción de la fexofenadina, los restantes cinco
antihistamínicos presentaron coeficientes de partición altos, lo que sugiere que la
fexofenadina tendría menor propensión a cruzar la barrera hematoencefálica. Sin
embargo, es necesaria la realización de estudios adicionales para confirmar estos
hallazgos y establecer la capacidad de los antihistamínicos para penetrar en el
cerebro.
Clasificación de los antihistamínicos
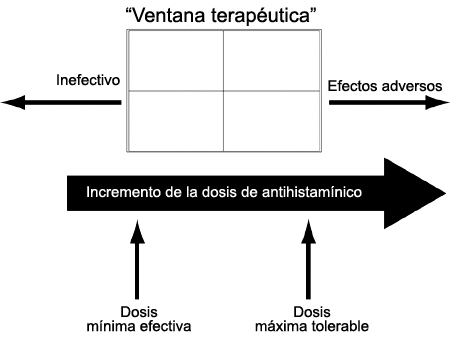
La fexofenadina es un ejemplo de un antagonista de los receptores
H1 con una ventana terapéutica extremadamente amplia. Se define
ventana terapéutica a la relación eficacia/seguridad del agente, de modo que su
espectro representa las dosis que son efectivas sin producir efectos secundarios
indeseables (figura 1). El límite inferior de la ventana terapéutica se define como la
dosis más baja asociada con un efecto farmacológico beneficioso, mientras que el
límite superior representa la dosis más alta tolerada sin reacciones farmacológicas
adversas. Esta ventana puede ser amplia o estrecha según la efectividad y la
toxicidad de la droga. Una ventana terapéutica amplia es beneficiosa ya que implica
que grandes poblaciones pueden ser tratadas en forma efectiva sin sufrir efectos
adversos.23 La dosis mínimamente efectiva del clorhidrato de
fexofenadina es de 20 mg dos veces por día24-26 y aun cuando se
administren dosis de 360 mg una vez por día (2 a 3 veces más la dosis diaria total
usualmente recomendada), esta droga permanece exenta de efectos sobre el
SNC.5
Sobre la base de los datos provenientes de las pruebas psicométricas y las
imágenes de PET analizados en este artículo, parecen haber distintas clases de
antihistamínicos de acuerdo con su capacidad para cruzar la barrera
hematoencefálica y el grado de deterioro que provocan sobre el SNC. Se propuso el
siguiente sistema de clasificación de los antihistamínicos orales (tabla 2). Las
drogas de clase C penetran rápidamente en el cerebro y tienen una tasa elevada de
ocupación de los receptores H1, con consecuencias en la capacidad
de los pacientes para realizar las actividades diarias y en su sistema cognitivo. Las
drogas de clase B muestran evidencias de una penetración cerebral relacionada con
la dosis y de H1RO, aunque no de la magnitud observada con los
agentes de clase C. También producen alteraciones vinculadas con las dosis en las
pruebas psicométricas objetivas que son pertinentes para las tareas de la vida
diaria. Por último, las drogas de clase A no tuvieron consecuencias demostrables en
el rendimiento y, de acuerdo con los exámenes de PET, no penetran en el cerebro.
No presentaron impacto cuantificable en la ejecución de las tareas de la vida diaria.

Resumen
Si bien los antihistamínicos de nueva generación se asociaron con menores
efectos adversos sobre el SNC, no todos pueden usarse en dosis mayores a las
recomendadas, en particular en pacientes que muestran un cumplimiento excesivo
de la terapia. Esto tiene consecuencias para las personas que manejan u operan
maquinarias o en la realización de muchas tareas diarias que requieren alto grado
de concentración y alerta. Sobre la base de las pruebas clínicas disponibles hasta la
fecha, provenientes de las pruebas psicométricas y las imágenes de PET analizadas
en este artículo, la fexofenadina no parece tener efecto sedante ni empeorar la
función del SNC. Claramente, los datos presentados aquí sugieren que la
fexofenadina puede utilizarse en los individuos involucrados en actividades que
requieren destreza. Finalmente, los antihistamínicos pueden clasificarse por su
capacidad para cruzar la barrera hematoencefálica y el grado de deterioro
producido en el SNC; la fexofenadina parece ser la opción más segura desde el
punto de vista de los efectos sobre el SNC.
BIBLIOGRAFÍA
-
Passalacqua G, Scordamaglia A, Ruffoni S et al. Sedation from
H1 antagonists: evaluation methods and experimental results.
Allergol Immunopathol (Madrid) 1993; 21:79-83.
-
Cookson J, Taylor D, Katona C. Use of drugs in psychiatry: 5th edition. London:
Gaskell, 2002:408.
-
Starmer G. Antihistamines and highway safety. Ann Accident Prevention 1985;
17:311-317.
-
Warren RA, Simpson HM, Hilchie J et al. Drugs detected in fatally injured
drivers in the province of Ontario. In: Goldberg L, ed. Alcohol, drugs and traffic
safety. Stockholm, Sweden: Almqvist & Wiksell, 1981:203-217.
-
Hindmarch I, Shamsi Z, Kimber S. An evaluation of the effects of high-dose
fexofenadine on the central nervous system: a double-blind, placebo-controlled
study in healthy volunteers. Clin Exp Allergy 2002; 32:133-139.
-
Bradley CM, Nicholson AN. Studies on the central effects of the H1-antagonist,
loratadine. Eur J Clin Pharmacol. 1987; 32(4):419-421.
-
Gaillard AW, Gruisen A, De Jong R. The influence of antihistamines on human
performance. Eur J Clin Pharmacol 1988; 35(3):249-253.
-
ZYRTEC® (cetirizine hydrochloride). Prescribing Information. Pfizer Labs
Division of Pfizer Inc, NY, NY 10017. 2003.
-
Hindmarch I. Psychomotor function and psychoactive drugs. Br J Clin
Pharmacol 1980; 10:189-209.
-
Hindmarch I. Critical Flicker Fusion Frequency (CFFF): The effects of
psychotropic compounds. Pharmacopsychiatria 1982; 15:44-48.
-
Hindmarch I. A 1,4-benzodiazepine, temazepam (K 3917), its effect on some
psychological parameters of sleep and behaviour. Arzneimittelforschung 1975;
25:1836-1839.
-
Hindmarch I, Shamsi Z. Antihistamines: models to assess sedative properties,
assessment of sedation, safety and other side-effects. Clin Exp Allergy 1999;
29(Suppl 3):133-142.
-
Shamsi Z, Hindmarch I. Sedation and antihistamines: A review of inter-drug
differences using proportional impairment ratios. Hum Psychopharmacol Clin Exp
2000; 15:S3-S30.
-
Ramaekers JG, Vermeeren A. All antihistamines cross blood-brain barrier. BMJ
2000; 321(7260):572.
-
Nicholson AN, Handford AD, Turner C, Stone BM. Studies on performance and
sleepiness with the H1-antihistamine, desloratadine. Aviat Space Environ Med
2003; 74:809-815.
-
Gandon JM, Allain H. Lack of effect of single and repeated doses of
levocetirizine, a new antihistamine drug, on cognitive and psychomotor functions in
healthy volunteers. Br J Clin Pharmacol 2002; 54:51-58.
-
Yanai K, Ryu JH, Watanabe T et al. Histamine H1 receptor occupancy in human
brains after single oral doses of histamine H1 antagonists measured by positron
emission tomography. Br J Pharmacol 1995; 116:1649-1655.
-
Yanai K, Ryu JH, Watanabe T et al. Positron emission tomographic study of
central histamine H1-receptor occupancy in human subjects treated with
epinastine, a second-generation antihistamine. Methods Find Exp Clin Pharmacol
1995; 17(SC):64-69.
-
Yanai K, Okamura N, Tagawa M, et al. New findings in pharmacological effects
induced by antihistamines: from PET studies to knock-out mice. Clin Exp Allergy
1999; 29(Suppl 3):29-36.
-
Tagawa M, Kano M, Okamura N, et al. Neuroimaging of histamine H1-receptor
occupancy in human brain by positron emission tomography (PET): a comparative
study of ebastine, a second-generation antihistamine, and (+)-chlorpheniramine, a
classical antihistamine. Br J Clin Pharmacol 2001; 52:501-509.
-
Tashiro M, Mochizuki H, Iwabuchi K et al. Roles of histamine in regulation of
arousal and cognition: functional neuroimaging of histamine H1 receptors in human
brain. Life Sci 2002; 72:409-414.
-
Tejani-Butt S, Yaroslavsky I. Determining the membrane permeability of newer
antihistamines: implications for CNS function and safety. Proceedings of the 22nd
EAACI congress 2003:276 (Abstract 959).
-
Howarth PH. The concept of the therapeutic window in the choice of
H1-receptor antagonist. Adv Stud Med (submitted 2003).
-
Russell T, Stoltz M, Weir S. Pharmacokinetics, pharmacodynamics, and
tolerance of single- and multiple-dose fexofenadine hydrochloride in healthy male
volunteers. Clin Pharmacol Ther. 1998; 6:612-621.
-
Nelson HS, Reynolds R, Mason J. Fexofenadine HCl is safe and effective for
treatment of chronic idiopathic urticaria. Ann Allergy Asthma Immunol. 2000;
84:517-22.
-
Finn AF Jr, Kaplan AP, Fretwell R, Qu R, Long J. A double-blind, placebo-
controlled trial of fexofenadine HCl in the treatment of chronic idiopathic urticaria.
Allergy Clin Immunol. 1999; 104:1071-8.
|



![]()

