La terapia con probióticos se emplea cada vez con mayor frecuencia para la prevención y terapéutica de diversas infecciones y síndromes clínicos que afectan principalmente el tracto gastrointestinal. El término probióticos implica la administración de microorganismos vivos en número suficiente para ejercer un efecto fisiológico benéfico en el huésped, definición consensuada en la reunión de expertos de ISAPP.1 En los últimos ańos se vio una verdadera eclosión de publicaciones en esta área puntual de investigación, como metaanálisis y revisiones que sintetizan el efecto benéfico de los probióticos en las diarreas asociadas a antibióticos,2 del viajero y por rotavirus,3 y resultados positivos pero no definitivos sobre la administración de probióticos para la enfermedad de Crohn4 o en alergias atópicas.5
Al mismo tiempo, en el mercado alimentario se incrementó la disponibilidad de una muy extensa gama y variedad de productos probióticos y alimentos funcionales elaborados por empresas internacionales o regionales que proclaman una serie de efectos benéficos sobre el huésped, algunas veces no demostrados en ensayos clínicos.
Si bien el concepto de reconstitución de la microbiota indígena se estudió en profundidad, y se demostró su efectividad en el tracto gastrointestinal,6- 8 este concepto se traslada al restablecimiento del equilibrio ecológico del tracto urogenital para participar así en la prevención de infecciones. Las infecciones que afectan este tracto incluyen aquellas de transmisión sexual (sífilis, gonorrea, HIV, etc.) como las que se producen como consecuencia del ascenso de la microflora perineal, influidas tanto por factores exógenos (tratamientos hormonales, antibioticoterapias, inmunosupresores) como endógenos (embarazo, menarca, inmunodeficiencias primarias). La incidencia de cada una de ellos es significativa porque producen desde esterilidad hasta distintos efectos sobre la salud, tanto de la mujer embarazada como del feto. Asimismo, es cada vez mayor el número de mujeres que sufren infecciones del tracto urinario (UTI) a lo largo de su vida, o bien en la etapa prepuberal o posmenopáusica.
Sobre la base de los antecedentes descritos, nuestro grupo comenzó a investigar sobre la posibilidad de emplear la bacterioterapia con BAL para la prevención y tratamiento de infecciones urogenitales. Debido a que existe una especificidad de huésped en muchos de los componentes de la microbiota indígena,9 nos dedicamos a aislar y seleccionar lactobacilos vaginales de origen humano que pudieran ser empleados para la prevención de infecciones urogenitales como una alternativa válida para el empleo de antibióticos, antimicóticos y/o antiparasitarios, que producen efectos adversos y depleción de la microbiota indígena con las consecuencias concomitantes. Una vez aislados los lactobacilos de vagina de mujeres de nuestro medio realizamos el relevamiento de sus propiedades benéficas o probióticas que permitieran su empleo como reconstituyentes de la microbiota indígena y prevención de infecciones.10 Se seleccionaron aquellos microorganismos con una superficie hidrofóbica que les permitiera una mejor adherencia a la membrana de las células epiteliales, o bien a la capa de glucoproteínas mucosas que las recubre, que varía según el estadio del ciclo hormonal. Luego, se seleccionaron los lactobacilos que pudieran producir grandes cantidades de sustancias antagónicas frente a patógenos urogenitales: ácidos orgánicos (por ej. ácido láctico), peróxido de hidrógeno o bacteriocinas.11- 14 La capacidad de producir peróxido de hidrógeno se empleó como característica determinante de selección, en base a algunos trabajos publicados en los que se demuestra que pacientes normales tienen prevalencia de lactobacilos H202+ en vagina, mientras que esta población está deplecionada o disminuida en pacientes con síndromes infecciosos.15-17 La propiedad de producir bacteriocinas en lactobacilos vaginales no fue publicada previamente, por lo que la descripción de Lactobacillus salivarius, productor de una bacteriocina termoestable que inhibe varios patógenos genitales13 fue uno de los hallazgos más interesantes de nuestro grupo. Ello nos permitiría combinar bacterias vivas con sustancias inhibidoras para su aplicación en el diseńo de un producto farmacéutico.
Debido a que todo producto a ser aplicado en seres humanos debe ser probado en animales de experimentación, se trabajó en la implementación de un modelo experimental murino para estudiar la capacidad de colonización de lactobacilos al ser inoculados intrauretralmente. Así, determinamos que en ratones hembra adultas (cepa BALB/c) de dos meses de edad, la dosis óptima debía ser de alrededor de 107 células viables durante tres días para colonizar el tracto urinario, los que permanecían en el tracto hasta el día 7 posinoculación.18-20 Debían ser reinoculadas para lograr un tiempo más largo de colonización. Demostramos que no producen efectos adversos o colaterales en ninguno de los órganos del tracto urinario, ni modificaciones estructurales o ultraestructurales.21 Son capaces de prevenir la infección por Escherichia coli uropatógeno, en mayor grado si son aplicados preventivamente que terapéuticamente.22 Y si se administran junto con antibióticos22 o con hormonas23 la respuesta frente al patógeno es más intensa, ya que E. coli desaparece del tracto más rápidamente y sin producir un efecto tan agresivo en el huésped. Por otra parte, la administración intravaginal de lactobacilos no produce modificaciones histológicas al ser administrados en el modelo experimental murino.24
El disponer de una serie de lactobacilos probióticos o benéficos implica además el estudio de sus propiedades tecnológicas para su inclusión en un producto de aplicación vaginal. Un producto efectivo para recolonizar el tracto vaginal, de aplicación local, debe contener microorganismos vivos en número no inferior a 107 bacterias, lo que implica obtener una gran cantidad de biomasa microbiana. Para ello se evaluaron los medios de cultivo y condiciones físico- químicas óptimas que permitieran un mayor rendimiento microbiano,25 como la liofilización en presencia de diferentes componentes y excipientes de productos farmacéuticos,26-28 para lograr una vida de estante extendida del producto. Por otra parte, se evaluaron las condiciones óptimas de producción de sustancias antagónicas para diseńar productos combinados conteniendo al mismo tiempo bacterias vivas y sustancias inhibidoras de patógenos.29-32 Así, se determinó que las condiciones óptimas de producción de bacteriocina de L. salivarius son similares a las condiciones de crecimiento.30 Mientras que las condiciones óptimas de producción de peróxido de hidrógeno y de autoagregación son diferentes de las de crecimiento, ya que el metabolito oxidante se produce en mayores concentraciones en agitación, situación en la que inhibe más efectivamente S. aureus, microorganismo responsable del síndrome del shock tóxico en usuarias de tampones.31,32 Las concentraciones e isómeros de ácido láctico producido por los lactobacilos son diferentes según las condiciones de crecimiento, como la capacidad de autoaglutinar.32
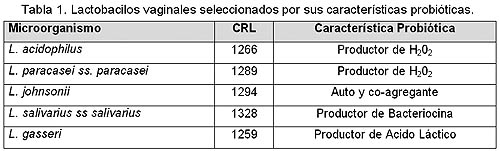
Los resultados de nuestro grupo permitieron la selección de lactobacilos probióticos (resumidos en la tabla 1) con características benéficas que incluyen: capacidad de adherencia a epitelios y mucosas, producción de ácido láctico, peróxido de hidrógeno, bacteriocinas, autoagregación, y sin producir efectos adversos en el modelo animal murino. Estos microorganismos podrán ser incluidos en un producto farmacéutico de aplicación local para la prevención de infecciones urogenitales.
La aplicación clínica de estos productos y su efectividad recién se encuentran en su etapa inicial, con escasas publicaciones en el tema. Si bien este tipo de productos están disponibles en el mercado farmacéutico mundial, no se publicaron las características de los microorganismos ni los efectos beneficiosos o detrimentales en el huésped, con algunas escasas excepciones. El grupo de Reid y col., en Canadá, demostró la efectividad y las propiedades de L. fermentum y L. rhamnosus en la prevención de las infecciones urinarias y en vaginosis bacterianas.33-36 Otros investigadores están estudiando y realizando ensayos clínicos para evaluar la efectividad de diferentes microorganismos ante la vaginosis bacteriana.37-47
Los pocos ensayos clínicos publicados dan idea de la promisoria efectividad de la prevención y tratamiento de algunos síndromes específicos por cepas específicas de lactobacilos, lo que sería óptimo para evitar las terapias antimicrobianas con sus concomitantes efectos adversos sobre la salud del huésped.
Las posibilidades de investigación en esta área puntual son amplísimas, básicamente por la característica GRAS de los lactobacilos, lo que permite en teoría su administración sin que sean sujeto de control de determinadas agencias. Pero es necesario profundizar en el conocimiento de los efectos de la administración prolongada de lactobacilos en el tracto urogenital, si es que producen algún tipo de efecto adverso, si tienen algún efecto sobre los parámetros de alta calidad de vida que se emplean como marcadores poblacionales, cuál es el efecto que producen en la mujer embarazada, en qué momento hay que administrarlos, cuál es la dosis y el tiempo óptimos de administración, etc.
Los autores no manifiestan “conflictos de interés”.
BIBLIOGRAFÍA
-
Reid G, Sanders ME, Gaskins R et al. New Scientific paradigms for probiotics
and prebiotics. Journal of Clinical Gastroenterology 2003; 37:108-118.
-
Cremonini F, Di Caro S, Nista EC et al. Metaanalysis: The effect of probiotic
administration on antibiotic-associated diarrhea. Aliment Pharmacol Ther 2002;
16:1461-1467.
-
Szajewska H, Mrukowics JZ. Probiotics in the treatment and prevention of acute
infectious diarrea in infants and children: a systematic review of published
randomized, double blind, placebo controlled trials. J Pedriatr Gastroentl Nutr 2001;
33(Supl2):S17-25.
-
Sartor RB. Probiotic therapy of intestinal inflammation and infections. Curr Opin
Gastroenterol 2005; 21:44-50.
-
Weston S, Halbert AR, Richmond P, Prescott SL. Effect of probiotics on atopic
dermatitis: a randomised controlled trial. Arch Dis Child 2005; 29.
-
Gill HS, Guarner F. Probiotics and humal health: a clinical perspective. Postgrad
Med J 2004; 80:516-526.
-
Sullivan A, Nord CE. Probiotics and gastrointestinal diseases. J Intern Med
2005; 257:78-92.
-
De Roos NM, Katan MB. Effects of probiotic bacteria on diarrea, lipid
metabolism and carcinogenesis: a review of papers published between 1988 and
1998. Am J Clin Nutr 2000; 71:405-411.
-
Savage DC, Kotarski SF. Models for study the specificity by which lactobacilli
adhere to murine gastric epithelium. Inf and Immun 1979; 26:966-973.
-
Ocańa VS, Bru E, De Ruiz Holgado AP, Nader-Macías ME. Surface
characteristics of lactobacilli isolated from human vagina. J Gen Appl Microbiol
1999; 45:203-12.
-
Ocańa VS, De Ruiz Holgado AP, Nader-Macías ME. Selection of vaginal
H2O2-generating Lactobacillus for probiotic
use. Current Microbiol 1999; 38:279-84.
-
Ocańa VS, De Ruiz Holgado AP, Nader-Macías ME. Growth inhibition of
Staphylococcus aureus by H2O2-producing
Lactobacillus paracasei subsp. paracasei isolated from the human
vagina. FEMS Immunol Med Microbiol 1999; 23:87-92.
-
Ocańa VS, De Ruiz Holgado AP, Nader-Macías ME. Characterization of a
bacteriocin-like substance produced by a vaginal Lactobacillus salivarius strain. Appl
Env Microbiol 1999; 65:5631-35.
-
Juárez Tomas MS, Ocańa VS, Wiesse B, Nader-Macías ME. Growth and Lactic
acid production by vaginal Lactobacillus acidophilus CRL 1259, and
inhibition of uropathogenic Escherichia coli. J Of Medical Microbiology
2003; 52:1117-1124.
-
Hillier SL, Krhonh MA, Rabe LK, Klebanoff S, Eschenbach D. The normal vaginal
flora, H202-producing lactobacilli and bacterial
vaginosis in pregnant women, Clin Inf Diseases 1993; 16(S4):S273-281.
-
Redondo-López V, Cook RL, Sobel JD. Emerging role of lactobacilli in the
control and maintenance of the vaginal bacterial microflora. Rev Infect Dis 1990;
12:856-872.
-
Esenbach Klebanoff SJ, Hillier SL, Eschenbach DA, Waltersdorph AM. Control of
the microbial flora of the vagina by H2O2-generating
lactobacilli. J Inf Dis 1991; 164:94-100.
-
Nader Macías ME, López Bocanera ME, Silva Ruiz C, Pesce de Ruiz Holgado A.
Isolation of lactobacilli from the urogenital tract of mice. Elaboration of beads for
their inoculation. Microbiologie-Aliments-Nutrition 1992; 10:43-7.
-
Silva Ruiz C, Nader-Macías ME, López Bocanera ME, Ruiz Holgado A.
Lactobacillus fermentum administered in suspensions and in agarose beads to mice:
a comparative study. Microbiologie Aliments Nutrition 1993; 11:391-397.
-
Nader-Macías ME, Silva-Ruiz C, López-Bocanera ME, Pesce-Ruiz Holgado A.
Behaviour of lactobacilli on prevention and therapeutic effects on urinary tract
infections (UTI) in mice. Anaerobe 1996; 2:85-93.
-
Silva de Ruiz C, Rey R, Nader-Macías ME. Structural and ultrastructural studies
of the urinary tract of mice inoculated with Lactobacillus fermentum.
British Journal of Urology 2003; 91:878-882.
-
Silva Ruiz C, Lopez Bocanera ME, Nader Macias ME, Pesce de Ruiz Holgado A.
Effect of lactobacilli and antibiotics on E. coli urinary tract infections in
mice. Biol Pharmac Bull 1996; 19(1):88-93.
-
Silva Ruiz C, Rey R, Nader Macías ME. Experimental administration of estradiol
on the colonization of Lactobacillus fermentum and Escherichia coli
in the urogenital tract of mice. Bio Pharm Bull 2001; 24:127-134.
-
Vintini E; Ocańa V, Nader-Macias ME. Effect of lactobacilli administration in the
vaginal tract of mice: evaluation of side effects and local immune response by local
administration of selected strains. Methods Mol Biol 2004; 268:401-410.
-
Juárez Tomás MS, Bru de Labanda E, de Ruiz Holgado AP, Nader-Macías ME.
Estimation of vaginal probiotic lactobacilli growth parameters with the application of
the Gompertz model. Can J Microbiol 2002; 48:82-92.
-
Juárez Tomás MS, Ocańa V, Nader-Macías ME. Viability of vaginal probiotic
lactobacilli during refrigerated and frozen storage. Anaerobe 2004; 10:1-5.
-
Zárate G, Juárez Tomas MS, Nader-Macias ME. Effect of some pharmaceutical
excipiente on the survival of probiotic vaginal lactobacilli. (2005) In press.
-
Zárate G, Nader-Macias. Viability and biological properties of probiotic vaginal
lactobacilli after lyophilization and refrigerated storage into gelatin capsules. (2005)
In press.
-
Juárez Tomás MS, Bru E, Nader-Macías ME. Comparison of the growth and
hydrogen peroxide production by vaginal probiotic lactobacilli under different
culture conditions. Am J Obstet Gynecol 2003; 188:35-44.
-
Juárez Tomás MS, Bru E, Wiese B, de Ruiz Holgado AAP, Nader-Macías ME.
Influence of pH, temperature and culture media on the growth and bacteriocin
production of vaginal Lactobacillus salivarius CRL 1328. J Appl Microbiol 2002; 93
(4):714-724.
-
Ocańa VS, Nader-Macias ME. Vaginal Lactobacilli: self and co-aggregating
ability. British Journal of Biomedical Sciences 2002; 59:183-190.
-
Juárez Tomás MS, Wiese B, Nader-Macias ME. Effects of culture conditions on
the growth and auto-aggregation ability of vaginal Lactobacillus johnsonii
CRL 1294. (2005) In press.
-
Reid G, Bruce A, Taylor M. Influence of three days antimicrobial therapy and
Lactobacilli vaginal suppositories on recurrence of urinary tract infections. Clin
Therap 1992; 14:11-16.
-
Baerheim S, Larsen E, Di Granes A. Vaginal application of lactobacilli in the
prophylaxis of recurrent lower urinary tract infections in women. Scand J Prim
Health Care 1994; 12:239-242.
-
Raz R, Stamm W. A controlled trial of intravaginal estriol in postmenopausal
women with recurrent urinary tract infections. New Eng J of Medicine 1993;
329:753-756.
-
Parent J, Bossens M, Bayot D, et al. Therapy of bacterial vaginosis using
exogenously applied lactobacillus acidophilus and a low dose of estriol. Drug Res
1996; 46:68-73.
-
Mc Groarty J. Probiotic use of lactobacilli in the human female urogenital tract.
FEMS Microb and Medical Microbiology 1993; 6:251-264.
-
Reid G, Burton J. Use of Lactobacillus to prevent infection by pathogenic
bacteria. Microbes and Infection 2002; 4:319-324.
-
Boris S, Barbes C. Role played by lactobacilli in controlling the population of
vaginal pathogens Microbes and Infection 2000; 2:543-546.
-
Reid G, Bruce AW. Selection of Lactobacillus strains for urogenital probiotic
applications. J Infect Dis 2001; 183(Suppl 1):S77-80.
-
Reid G, Jass J, Sebulsky T, McCormick J. Potential uses of probiotics in clinical
practice. Clin Microbiol Rev 2003; 16(4):658-72.
-
Reid G, Beuerman D, Heinemann C, Bruce AW. Probiotic Lactobacillus dose
required to restore and maintain a normal vaginal flora. FEMS Immunol Med
Microbiol 2001; 32:37-41.
-
Reid G, Bruce AW. Selection of lactobacillus strains for urogenital probiotic
applications. J Infect Dis 2001; 183(suppl 1):S77-S80.
-
Gardiner G, Heinemann C, Beuerman D, Bruce AW, Reid G. Persistence of
Lactobacillus fermentum RC-14 and L. rhamnosus GR-1, but not
L. rhamnosus GG in the human vagina as demonstrated by randomly
amplified polymorphic DNA (RAPD). Clin Diagn Lab Immunol 2002; 9:92-96.
-
Reid G, Cook RL, Bruce AW. Examination of strains of lactobacilli for properties
which may influence bacterial interference in the urinary tract. J Urol
1987;138:330-335.
-
Reid G. Probiotic agents to protect the urogenital tract against infection. Am J
Clin Nutr 2001; 73(suppl):437S-443S.
-
Reid G, Charbonneau D, Erb J, Kochanowski B, Beuerman D, Poehner R, Bruce
AW. Oral use of Lactobacillus rhamnosus GR-1 and L. fermentum
RC-14 significantly alters vaginal flora: randomized, placebo-controlled trial in
64 healthy women. FEMS Immunol Med Microbiol 2003; 35:131-134.
|


![]()
