 Resumen
Introducción: Los medicamentos antiinflamatorios no esteroides representan la clase terapéutica más utilizada para el tratamiento de enfermedades inflamatorias, pero su uso está asociado con diversos efectos adversos. Por lo tanto, la búsqueda de nuevas estrategias terapéuticas antiinflamatorias seguras y eficaces es un problema actual. El extracto lipídico obtenido de los frutos de Acrocomia crispa (D-005) inhibe la actividad in vitro de las enzimas ciclooxigenasa-2 y 5-lipooxigenasa. Objetivo: Investigar los efectos del D-005 en modelos experimentales de inflamación aguda y crónica. Materiales y métodos: Se evaluó la administración oral de D-005 en el edema de la oreja inducido por xileno en ratones y en pleuresía inducida por carragenina en ratas (modelos de inflamación aguda), así como en el granuloma inducido por pellet de algodón en ratas (modelo de inflamación crónica). Resultados: La administración oral de D-005 (5, 25, 50, 100 y 200 mg/kg) previno de forma significativa y dependiente de la dosis la formación del edema y el aumento de la actividad de la enzima mieloperoxidasa inducidos por el xileno. Del mismo modo, redujo el volumen de los exudados pleurales inducidos por carragenina, así como la actividad de mieloperoxidasa, sin modificar la concentración total de proteínas en los exudados pleurales. Además, el D-005 (25 y 100 mg/kg) administrado durante seis días disminuyó el peso húmedo y seco del granuloma inducido por algodón. Conclusiones: La administración oral del D-005 previene significativamente la inflamación aguda y crónica en modelos clásicos de inflamación en roedores, sugiriendo su beneficio potencial para tratar procesos inflamatorios.
Resumen
Introducción: Los medicamentos antiinflamatorios no esteroides representan la clase terapéutica más utilizada para el tratamiento de enfermedades inflamatorias, pero su uso está asociado con diversos efectos adversos. Por lo tanto, la búsqueda de nuevas estrategias terapéuticas antiinflamatorias seguras y eficaces es un problema actual. El extracto lipídico obtenido de los frutos de Acrocomia crispa (D-005) inhibe la actividad in vitro de las enzimas ciclooxigenasa-2 y 5-lipooxigenasa. Objetivo: Investigar los efectos del D-005 en modelos experimentales de inflamación aguda y crónica. Materiales y métodos: Se evaluó la administración oral de D-005 en el edema de la oreja inducido por xileno en ratones y en pleuresía inducida por carragenina en ratas (modelos de inflamación aguda), así como en el granuloma inducido por pellet de algodón en ratas (modelo de inflamación crónica). Resultados: La administración oral de D-005 (5, 25, 50, 100 y 200 mg/kg) previno de forma significativa y dependiente de la dosis la formación del edema y el aumento de la actividad de la enzima mieloperoxidasa inducidos por el xileno. Del mismo modo, redujo el volumen de los exudados pleurales inducidos por carragenina, así como la actividad de mieloperoxidasa, sin modificar la concentración total de proteínas en los exudados pleurales. Además, el D-005 (25 y 100 mg/kg) administrado durante seis días disminuyó el peso húmedo y seco del granuloma inducido por algodón. Conclusiones: La administración oral del D-005 previene significativamente la inflamación aguda y crónica en modelos clásicos de inflamación en roedores, sugiriendo su beneficio potencial para tratar procesos inflamatorios.
 Abstract
Abstract
Introduction: Non-steroidal anti-inflammatory drugs represent the most used therapeutic class for the treatment of inflammatory diseases, but their use is associated with various adverse effects. Therefore, the search for new safe and effective anti-inflammatory therapeutic strategies is a current problem. The lipid extract obtained from the fruits of Acrocomia crispa (D-005) inhibits the in vitro activity of the enzymes cyclooxygenase-2 and 5-Lipoxygenase. Objective: To investigate the effects of D-005 in experimental models of acute and chronic inflammation. Materials and methods: Oral administration of D-005 was evaluated on ear edema induced by xylene in mice and on carrageenan-induced pleurisy in rats (acute inflammation models), as well as on cotton pellet-induced granuloma in rats (chronic inflammation model). Results: Oral administration with D-005 (5, 25, 50, 100 and 200 mg/kg) significantly and dose-dependently prevented the formation of edema and the increased activity of the myeloperoxidase enzyme induced by xylene. In the same way, it reduced the volume of the carrageenan-induced pleural exudates, as well as the myeloperoxidase activity, without modifying the total protein concentration in the pleural exudates. Furthermore, D-005 (25 and 100 mg/kg) administered for six days decreased the wet and dry weight of the cotton-induced granuloma. Conclusions: Oral administration of D-005 significantly prevents acute and chronic inflammation in classical models of inflammation in rodents, suggesting its potential benefit in treating inflammatory processes.
Artículo completo
EFECTOS ANTIINFLAMATORIOS DEL EXTRACTO LIPIDICO DEL FRUTO DE ACROCOMIA CRISPA (PALMA COROJO)
(especial para SIIC © Derechos reservados)
Introducción
La inflamación es un factor etiológico importante en el desarrollo y la progresión de diferentes enfermedades crónicas como la artritis reumatoidea, la aterosclerosis, la osteoartritis, el asma bronquial, la hiperplasia prostática benigna, la dermatitis atópica, el cáncer y la colitis ulcerosa. Por esta razón, el uso de agentes antiinflamatorios efectivos para el tratamiento de los trastornos inflamatorios agudos y crónicos ha aumentado en las últimas décadas, teniendo en cuenta el aumento considerable de la esperanza de vida y, en consecuencia, la mayor incidencia de enfermedades relacionadas con la edad avanzada.1-6
Los antiinflamatorios no esteroides (AINE) (aspirina, indometacina, naproxeno e ibuprofeno), cuya acción antiinflamatoria se sustenta principalmente en la inhibición de la enzima ciclooxigenasa (COX) son la clase terapéutica más comúnmente prescrita. Sin embargo, la marcada eficacia antiinflamatoria de estos agentes se acompaña de numerosos efectos adversos relacionados principalmente con la relación preferencial sobre las isoenzimas COX-1 o COX-2. En este sentido, los agentes con un mayor grado de selectividad sobre la COX-2 se han asociado con una mayor tasa de eventos adversos cardiovasculares relacionados con la dosis, mientras que los agentes con un mayor grado de inhibición sobre la COX-1 son los principales responsables de los trastornos gastrointestinales. Además, los agentes con mayor selectividad sobre COX-1 inhiben la producción de prostaglandinas gastroprotectoras y desplazan el metabolismo del ácido araquidónico hacia la vía de la 5-lipoxigenasa (5-LOX) con la consiguiente sobreproducción de leucotrienos (proinflamatorios y gastrotóxicos).7-10
Por esta razón, la búsqueda de nuevas estrategias terapéuticas antiinflamatorias seguras y eficaces es un problema actual.
En este contexto, los inhibidores duales de las enzimas COX y 5-LOX (licofelona, lyprinol y tepoxalina) con un mayor perfil de seguridad y tolerabilidad constituyen una importante alternativa terapéutica antiinflamatoria.11-13
El D-005, extracto lipídico del fruto de Acrocomia crispa, palma endémica de Cuba, consiste en una mezcla reproducible de ácidos grasos, principalmente oleico, palmítico, láurico y mirístico, mientras que los ácidos palmitoleico, caprílico, cáprico y esteárico están en una proporción menor.14 Un estudio previo mostró que el D-005 inhibe la actividad de las enzimas COX-2 y 5-LOX,15 sin embargo, la evaluación de los efectos antiinflamatorios in vivo de D-005 no se ha investigado previamente. El objetivo de este estudio fue investigar los efectos de D-005 en modelos experimentales de inflamación aguda y crónica.
Materiales y métodos
Animales
Ratas Sprague Dawley adultas machos (200 a 280 g) y ratones OF-1 jóvenes machos (20 a 30 g), del Centro Nacional de Animales de Laboratorio (CENPALAB, La Habana, Cuba), se adaptaron durante siete días a condiciones de laboratorio (20 a 250C, 60 ± 5% de humedad relativa y 12 horas de ciclos de luz/oscuridad), con libre acceso al agua y comida estándar para roedores (CENPALAB).
Los experimentos con animales se realizaron de acuerdo con las directrices cubanas de manipulación de animales y el Código Cubano de Buenas Prácticas de Laboratorio (BPL), que siguen las normas internacionales sobre este tema.
El protocolo de estudio y el uso de animales fueron aprobados antes de comenzar el estudio por un comité de ética animal independiente.
Administración y dosis
El D-005 (Laboratorio de Química del Centro de Productos Naturales, Centro Nacional de Investigación Científica, La Habana, Cuba) se suspendió en Tween 65/H2O (2%), y la aspirina (Farmacuba, La Habana, Cuba) se disolvió en goma de acacia (1%). Todos los tratamientos se administraron mediante sonda gástrica a través de la vía oral a 5 ml/kg de peso corporal.
La carragenina (BDH Chemical Ltd Poole, Inglaterra) (agente proinflamatorio) y el citrato de sodio (Caledon Laboratories Ltd, Georgetown, Canadá) se disolvieron en solución salina al 1 y 3.15%, respectivamente. El xileno (Merck, Darmstadt, Alemania) se utilizó en su forma pura.
Edema de oreja de ratón inducido por xileno
Los ratones se aleatorizaron en ocho grupos (10 individuos por grupo): un grupo control negativo tratado por vía oral con el vehículo y siete grupos tratados con xileno: un control positivo (tratado con el vehículo), cinco tratados con D-005 (5, 25, 50, 100 y 200 mg/kg) y un grupo con aspirina, sustancia de referencia, de 100 mg/kg. Todos los tratamientos se administraron como dosis única una hora antes de la inducción de la inflamación.
La inflamación fue inducida por la aplicación tópica de xileno puro (30 µl) en la superficie dorsal de la oreja derecha de los roedores.16 Dos horas después, los animales fueron sacrificados en una atmósfera de halotano y ambas orejas fueron cortadas y pesadas en una balanza analítica.
La formación de edema se calculó por la diferencia entre los pesos de la oreja derecha (con edema) y de la oreja izquierda (sin edema) (DO).
Posteriormente, se obtuvo el homogeneizado de las orejas para la determinación de la actividad mieloperoxidasa (MPO).
Pleuresía inducida por carragenina en ratas
Las ratas se aleatorizaron en ocho grupos (10 ratas por grupo): un grupo de control negativo inyectado con solución salina en la cavidad pleural y siete grupos tratados con carragenina: un control positivo (tratado con el vehículo), cinco con D-005 (5, 25, 50, 100 y 200 mg/kg) y un grupo con aspirina como sustancia de referencia de 100 mg/kg.
Todos los tratamientos se administraron como dosis única una hora antes de la inducción de la lesión.
Para la inducción del edema pleural, las ratas se anestesiaron con halotano y se les administró 0.3 ml de una inyección intrapleural de carragenina al 1%.17 Cinco horas después de la inyección, las ratas se anestesiaron en atmósfera de halotano y se sacrificaron mediante el sangrado completo de la aorta abdominal.
Para obtener los exudados pleurales se realizó una incisión en la cavidad pleural y se añadió 1 ml de citrato de sodio (3.15%), que se homogeneizó con los exudados, se recogió con pipetas automáticas y se añadió a los tubos plásticos graduados.
El fluido recogido se midió en tubos de plástico graduados, para los cuales se sustrajo el volumen de citrato de sodio agregado (1 ml). Los exudados contaminados con sangre fueron desechados.
El porcentaje de inhibición del edema se calculó de la siguiente manera: Inhibición = 100 - (VT/VC) x 100 (%), donde VT y VC representan el volumen de exudados pleurales en ratas tratadas y de control, respectivamente.
Ulteriormente se utilizó el exudado pleural para cuantificar la actividad de la MPO y las proteínas totales.
Granuloma inducido por pellet de algodón
Las ratas fueron aleatorizadas en seis grupos (10 ratas por grupo): un grupo control tratado con vehículo, cuatro con D-005 (5, 25 y 100 mg/kg) y uno con aspirina (sustancia de referencia) de 100 mg/kg. Todos los tratamientos se administraron como dosis repetida durante seis días, 24 horas después de la inducción de la inflamación.
Los animales se anestesiaron con tiopental (30 mg/kg, ip) y se les realizó una incisión en la mitad dorsolateral, creando un túnel subcutáneo, donde se colocó inmediatamente un pellet de algodón estéril (50 mg de peso).18 De inmediato, se suturaron las heridas y se aplicó un antiséptico local. Veinticuatro horas después de la última administración, los animales se sacrificaron en una atmósfera de halotano y los granulomas se extrajeron cuidadosamente.
Para determinar el peso húmedo de los granulomas, una vez extraídos del animal, se pesaron en una balanza analítica. El peso del pellet de algodón (50 mg) se restó del peso total. Posteriormente, para determinar el peso seco, los granulomas se colocaron en estufa (60°C) durante 24 horas, hasta alcanzar un peso constante. El peso del pellet de algodón (50 mg) se restó del peso del granuloma seco.
El porcentaje de inhibición se expresó tomando como referencia el peso del granuloma del grupo control.
Determinación de la actividad mieloperoxidasa
La actividad de la mieloperoxidasa (MPO) se midió en exudado pleural y en homogeneizado de oreja, de acuerdo con el Manual de Enzimas Worthington.19
Las muestras se sonicaron durante 10 segundos, se congelaron y descongelaron a -20 a 30°C, tres veces. Después, las muestras se centrifugaron a 12 000 rpm durante 25 minutos a 4°C y se usó el sobrenadante para la determinación de MPO. En resumen, se mezclaron 625 ml de tampón fosfato (50 mmol/l, pH = 6) que contenía 0.167 mg/ml de diclorhidrato de O-dianisidina con 250 ml de muestra y 125 ml de peróxido de hidrógeno (0.0005%).
Los cambios en la absorbancia a 460 nm se midieron en un espectrofotómetro durante dos minutos. La actividad de MPO se expresó como unidades (U)/mg de proteína en el exudado.
Una unidad de MPO se define como la degradación de 1 µmol de peróxido por minuto a 25°C, que se cuantifica mediante la siguiente fórmula:
U/mg de proteína = DA min x Vol cubeta /8.3 x Vol muestra x 10
(DA min, variación de absorbancia; Vol cubeta, volumen final de la cubeta; Vol muestra, volumen de muestra agregada)
Determinación de proteínas totales
Las concentraciones de proteínas totales se evaluaron mediante una modificación del método de Lowry.20
Análisis estadístico
Los datos se expresaron como la media ± EE. Las comparaciones estadísticas entre los grupos control y tratado se realizaron con la prueba de la U de Mann-Whitney. Se estableció a priori un valor alfa de 0.05. Todos los análisis se llevaron a cabo utilizando el software de estadísticas para Windows (versión 6.0; StatSoft, Tulsa, OK, EE. UU.). La relación dosis/efecto se realizó mediante la prueba de regresión lineal y correlación utilizando el programa Origin (Origin Lab Corporation; EE. UU., Versión 8).
Resultados
La Tabla 1 muestra los resultados de los efectos del D-005 sobre el edema y la actividad de la enzima MPO en la oreja de los ratones. La aplicación tópica de xileno en la oreja derecha del ratón indujo la formación de edema y aumentó significativamente la actividad de MPO en el grupo control positivo en comparación con el grupo control negativo (sin daño). La aspirina redujo significativamente la formación de edema y la actividad de la enzima MPO.
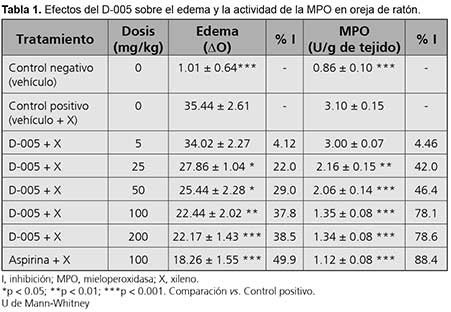
La administración oral de dosis únicas de D-005 (5-200 mg/kg) redujo significativamente el edema y la actividad enzimática de MPO, de modo dependiente de la dosis sobre ambas variables (r = 0.986; p = 0.002; r = 0.976; p = 0.004 edema y MPO, respectivamente). La dosis de 5 mg/kg no modificó ninguna de estas variables, mientras que 100 mg/kg produjo el mayor porcentaje de inhibición (38% y 78% en edema y MPO, respectivamente). La DE50 calculada para el edema y la actividad de la MPO fue de 20.01 y 21.9 mg/kg, respectivamente.
La Tabla 2 muestra los efectos del D-005 sobre el volumen de exudado pleural, el incremento de la actividad de MPO y sobre la concentración de proteínas totales, inducidos por carragenina.
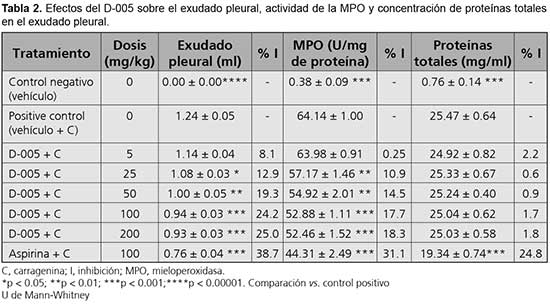
El grupo control positivo (con carragenina) presentó un aumento significativo en el volumen de exudados pleurales, en la actividad enzimática de MPO y en la concentración de proteínas totales en el exudado pleural, con respecto al grupo control negativo (sin carragenina), mientras que la aspirina redujo significativamente este aumento.
La administración oral única de D-005 (5-200 mg/kg) redujo significativamente y dependiente de la dosis el exudado pleural (r = 0.974; p = 0.005) y la actividad de MPO (r = 0.978; p = 0.004), sin modificar la concentración de proteínas totales en el exudado pleural. La dosis menor ensayada de 5 mg/kg no modificó estas variables. Por su parte, la dosis de 100 mg/kg produjo un 24.2% de inhibición sobre el exudado pleural y un 17.7% sobre la actividad de MPO, no siendo superior con 200 mg/kg. La DE50 calculada para el volumen de exudado pleural y la actividad de MPO fue de 22.92 y 19.15 mg/kg, respectivamente.
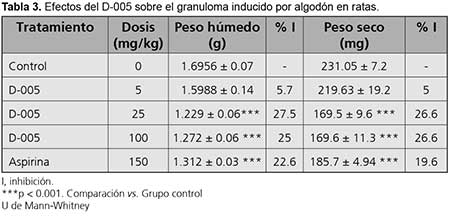
La Tabla 3 muestra los efectos de la administración oral de dosis repetidas de D-005 (5, 25 y 100 mg/kg) sobre el granuloma inducido por pellets de algodón.
Las dosis de 25 y 100 mg/kg redujeron de forma moderada, significativa y no dependiente de la dosis el peso húmedo y seco del granuloma, mientras que la dosis de 5 mg/kg no produjo modificaciones significativas (5.7%). La aspirina redujo moderada y significativamente el peso húmedo y seco del granuloma.
Discusión
La inflamación aguda inducida por la aplicación tópica de xileno a la oreja del ratón (modelo de edema neurogénico) se caracteriza por una irritación que conduce a una acumulación local de fluidos con la consiguiente formación de edema y un aumento en la actividad de la enzima MPO, que se ha asociado directamente con la concentración de neutrófilos en el tejido inflamado.21,22
Las características de este modelo se reprodujeron en nuestras condiciones experimentales y son similares a los resultados referidos por otros autores.21,23 Por otra parte, la aspirina redujo significativamente el aumento del edema y la actividad de MPO, lo que corrobora la validez de nuestros resultados.
El D-005 a 5-200 mg/kg previno de modo dependiente de la dosis la formación del edema y el incremento de la actividad de la MPO, inducida por la aplicación tópica de xileno. La dosis mínima efectiva fue 25 mg/kg, ya que la dosis más baja de 5 mg/kg no produjo modificaciones significativas sobre estas variables, mientras que 100 mg/kg fue la dosis efectiva máxima, ya que la dosis mayor evaluada (200 mg/kg) no produjo ningún efecto adicional.
La inyección intercostal de carragenina en ratas, con la consecuente formación del exudado pleural inflamatorio en el espacio pleural implica la activación de enzimas que participan en el metabolismo del ácido araquidónico: 5-LOX y COX, con una mayor contribución de COX, específicamente la isoforma tipo I (COX-1). Esta isoforma es la responsable de la vasodilatación y del aumento de la permeabilidad vascular que le confiere al exudado originado un origen vasogénico, fundamentalmente.24-26
Por tanto, el hecho de que la inyección con carragenina en el grupo control positivo produjera un aumento significativo en el volumen de exudado pleural, en la actividad de la enzima MPO y en la concentración de proteínas totales en comparación con el grupo control negativo, y que la aspirina, sustancia de referencia, redujo significativamente dicho aumento, corrobora la validez de este modelo y los resultados obtenidos en nuestras condiciones experimentales.
El D-005 no modificó la concentración de proteínas totales en el exudado pleural en comparación con el grupo control positivo, lo que se corresponde con su mecanismo de acción que no involucra la inhibición de COX-1.15 La aspirina redujo significativamente la concentración de proteínas, de acuerdo con sus efectos como un clásico inhibidor inespecífico de la COX,27 pero con una relación preferencial sobre la actividad de la COX-1,28 una enzima básicamente responsable del aumento típico de la permeabilidad vascular en este modelo.26
La administración oral de D-005 (5-200 mg/kg) previno de forma dependiente de la dosis el aumento del exudado pleural y la actividad de MPO, inducida por la inyección de carragenina, de manera similar a los efectos observados en la inflamación inducida por xileno. La dosis de 25 mg/kg fue la dosis efectiva mínima y 100 mg/kg la dosis efectiva máxima. Sin embargo, la eficacia del D-005 en este modelo fue menor que la lograda en el modelo de inflamación inducida por xileno, mientras que la potencia según la DE50 fue similar en ambos modelos de inflamación aguda.
El mecanismo antiinflamatorio del D-005 podría constituir la base de su eficacia moderada en este modelo experimental de pleuresía inducida por carragenina, ya que el D-005 no modifica la actividad enzimática de COX-1,15 la cual tiene un papel importante en la fisiopatología de este modelo.25,26,29
Por otra parte, se ha documentado la relación directamente proporcional entre la actividad de MPO y la concentración de neutrófilos en el tejido inflamado, desde el espacio vascular hasta el intersticial, y su papel en el desarrollo de la inflamación aguda, por lo que una inhibición de la MPO presupone una disminución en la migración de leucocitos.30 Por tanto, los efectos de D-005 sobre la actividad enzimática de MPO en ambos modelos podrían explicar, al menos en parte, la razón de su eficacia en la inflamación aguda. Tales efectos están asociados con su inhibición de la actividad enzimática de 5-LOX, que reduce la formación de leucotrienos B4, un potente agente quimiotáctico de neutrófilos.30
El implante subcutáneo de pellets de algodón en ratas indujo la formación de granulomas en los animales del grupo de control, cuantificados mediante los pesos húmedo y seco. La aspirina, sustancia de referencia, redujo significativamente ambas variables, lo que corrobora la validez del modelo en nuestras condiciones experimentales.
El tratamiento oral con D-005 (25-100 mg/kg), durante seis días, redujo moderada y significativamente el peso húmedo y seco del granuloma, lo que demostró su efecto antiinflamatorio en este modelo clásico de inflamación crónica.
La eficacia del D-005 en este modelo no fue dependiente de la dosis, ya que la dosis de 25 mg/kg se comportó como la dosis efectiva mínima y al mismo tiempo como la dosis efectiva máxima porque 5 mg/kg no modificaron el peso de los granulomas, y 100 mg/kg, la dosis mayor ensayada, no produjo una eficacia superior. Este resultado corrobora la eficacia antiinflamatoria moderada del D-005, similar a la alcanzada en los modelos de inflamación aguda.
Ha sido documentado que el modelo del granuloma inducido por pellets de algodón tiene lugar en tres fases: la primera, transudativa, definida como el aumento del peso húmedo del granuloma, que se produce en las primeras tres horas; el segundo ocurre entre tres y 72 horas después de la implantación del pellet de algodón y se caracteriza por la extravasación de suero de la sangre al granuloma, y se define como una fase exudativa; y la tercera fase proliferativa, cuantificada como el aumento del peso seco del granuloma entre los días tres y seis del implante.29
Por lo tanto, la eficacia del D-005 para reducir la formación del granuloma está mediada por sus efectos en las tres fases, en correspondencia con su perfil de acción dual sobre las enzimas COX y 5-LOX.15
Estos resultados ponen de manifiesto el beneficio potencial del D-005 para el tratamiento y prevención de diversas patologías que involucran los procesos inflamatorios en su evolución y progresión.
Conclusiones
La administración oral de D-005 inhibió significativamente la inflamación aguda y crónica en modelos experimentales en roedores.
|
 Bibliografía del artículo
Bibliografía del artículo
1. Kuo D, Ding J, Cohn IS, Zhang F, Wei K, Rao DA, Sokhi UK, Shanaj S, Oliver DJ, Echeverria AP, DiCarlo EF, Brenner MB, Bykerk VP, Goodman SM, Raychaudhuri S, Ratsch G, Ivashkiv LB, Donlin LT. HBEGF macrophages in rheumatoid arthritis induce fibroblast invasiveness. Science Translational Medicine 11:1-13, 2019.
2. Fredman G, Tabas I. Boosting inflammation resolution in atherosclerosis: the next frontier for therapy. The American Journal of Pathology 187:1211-1221, 2017.
3.Mantovani A. The inflammation-cancer connection. The FEBS Journal 285:638-640, 2018.
4. Flores BM, O'Connor A, Moss AC. Impact of mucosal inflammation on risk of colorectal neoplasia in patients with ulcerative colitis: a systematic review and meta-analysis. Gastrointestinal Endoscopy 86:1006-1011, 2017.
5. Cianferoni A, Spergel J. Eosinophilic esophagitis: a comprehensive review. Clinc Rev Allerg Immunol 50:159-174, 2016.
6. Guo CG, Leung WK. Potential strategies in the prevention of nonsteroidal anti-inflammatory drugs-associated adverse effects in the lower gastrointestinal tract. Gut and Liver 14:179, 2020.
7. Scheiman JM. NSAID-induced gastrointestinal injury. Journal of Clinical Gastroenterology 50:5-10, 2016.
8. Sevinsky RE, Stewart DW, Harirforoosh S. Nonsteroidal anti-inflammatory drugs: Is there a link between cardiovascular and renal adverse effects? Journal of Integrative Nephrology and Andrology 4:1, 2017.
9. Gerbino PP. Emerging evidence in NSAID pharmacology: important considerations for product selection. Am J Manag Care 21:S139-S147, 2015.
10. Tziona P, Theodosis-Nobelos P, Rekka E. Medicinal chemistry approaches of controlling gastrointestinal side effects of non-steroidal anti-inflammatory drugs. Endogenous protective mechanisms and drug design. Medicinal Chemistry 13 408-420, 2017.
11. Sukumaran S, Pittman KB, Patterson WK, Dickson J, Yeend S, Townsend A, Broadbridge V, Price TJ. A phase I study to determine the safety, tolerability and maximum tolerated dose of green-lipped mussel (Perna canaliculus) lipid extract, in patients with advanced prostate and breast cancer. Annals of Oncology 21:1089-1093, 2010.
12. Cegielska-Perun K, Marczuk E, Bujalska-Zadroøny M. Novel inhibitors of leukotrienes synthesis in a treatment of inflammatory pain. Acta Poloniae Pharmaceutica 74:1043, 2017.
13. Rodriguez BO, Legleu CEC, De León Fierro LG, Sosa KFC, Luján RC, Longoria RJN. Suplementos nutricionales en el tratamiento y la prevención del dolor muscular tardío: una revisión sistemática. Retos 35: 407, 2019.
14. González V, Sierra R, Mas R, Pérez Y, Oyarzábal A, Rodríguez E, Molina V, Menéndez RG. Patent No. WO 2013/189467 A2. (2015).
15. Pérez Y, Oyarzábal A, Sierra R, Mas R, Molina V, Jiménez S, González V. Inhibition of cyclooxygena se (COX) and 5-lipoxygenase (5-LOX) by D-005 (A lipid extract of Acrocomia crispa fruits). Boletín Latinoamericano y del Caribe de Plantas Medicinales y Aromáticas, 16:319-328, 2017.
16. Ravelo Y, Molina V, Jiménez S, Oyarzábal A, Pérez Y, Más R. Effect of oral administration of D-004, a lipid extract from Roystonea regia fruits, on xylene-induced ear oedema in mice. Lat Am J Pharm 30: 1744-1748, 2011.
17. Oyarzábal A, Molina V, Ravelo Y, Pérez Y, Jiménez J. Effects of D-004, a lipid extract of the Roystonea regia fruits, on carrageenan-induced pleurisy in rats. BAOJ Pharm Sci 3:046, 2017.
18. Zamora Z, Molina V, Mena L, Nodal C. Efecto anti-inflamatorio de la terapia combinada del D-002 y lyprinol en un modelo de inflamación crónica. Revista CENIC. Ciencias Biológicas 48:6, 2017.
19. Manual WE. Worthington Biochemical Corp. Freehold, NJ, 43 (1972).
20. Markwell MAK, Haas SM, Bieber LL, Tolbert N. A modification of the Lowry procedure to simplify protein determination in membrane and lipoprotein samples. Analytical Biochemistry 87:206, 1978.
21. Eidi A, Oryan S, Zaringhalam J, Rad M. Antinociceptive and anti-inflammatory effects of the aerial parts of Artemisia dracunculus in mice. Pharmaceutical Biology 54:549, 2016.
22. Wang J. Neutrophils in tissue injury and repair. Cell and Tissue Research 371:531, 2018.
23. Lee YY, Saba E, Irfan M, Kim M, Yi-Le Chan J, Jeon BS, Choi SK, Rhee MH. The anti-inflammatory and anti-nociceptive effects of Korean black ginseng. Phytomedicine 54:169-181, 2019.
24. Muller WA. Leukocyte-endothelial cell interactions in the inflammatory response. Laboratory Investigation 82: 521-534, 2002.
25. Nakano M, Denda N, Matsumoto M, Kawamura M, Kawakubo Y, Hatanaka K, Harada Y. Interaction between cyclooxygenase (COX)-1-and COX-2-products modulates COX-2 expression in the late phase of acute inflammation. Eur J of Pharmacol 559:210-218, 2007.
26. Fausto MD, Jon Aster MD. Acute and chronic inflammation, 8th edition, (2009), Saunders Elsevier, Philadelphia.
27. Vane JR, Botting RM. The mechanism of action of aspirin. Thrombs Res 110:255-258, 2003.
28. Botting RM. Vane's discovery of the mechanism of action of aspirin changed our understanding of its clinical pharmacology. Pharmacol Rep 62:518-525, 2010.
29. Swingle KF, Shideman FE. Phases of the inflammatory response to subcutaneous implantation of a cotton pellet and their modification by certain antiinflammatory agents. J Pharmacol Exp Ther 183:226-234, 1972.
30. Van der Veen BS, De Winther M P, Heeringa P. Myeloperoxidase: molecular mechanisms of action and their relevance to human health and disease. Antioxid Redox Signal 11:2899-2937, 2009.
Artículos publicados por el autor
(selección):
:-
|
|






































